
| A. | 元素Y的最高正化合价为+6 | |
| B. | 简单离子半径的大小顺序为W>Q>Z>X>Y | |
| C. | 气态氢化物的稳定性:Q>W | |
| D. | 元素W的最高价氧化物对应的水化物酸性比Q的强 |
分析 短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X的气态氢化物极易溶于Y的氢化物中,则Y的氢化物作溶剂,且为氢化物,则Y的氢化物是H2O,所以Y是O元素,X的氢化物能溶于水,且X的原子序数小于Y,所以X是N元素;常温下,Z的单质能溶于W的最高价氧化物的水化物的稀溶液,却不溶于其浓溶液,铝、铁能溶于稀硫酸却不溶于浓硫酸,Z是短周期主族元素,所以Z是Al,W是S元素,Q属于短周期主族元素且原子序数大于S,所以Q是Cl元素,结合元素周期律来分析解答.
解答 解:短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X的气态氢化物极易溶于Y的氢化物中,则Y的氢化物作溶剂,且为氢化物,则Y的氢化物是H2O,所以Y是O元素,X的氢化物能溶于水,且X的原子序数小于Y,所以X是N元素;常温下,Z的单质能溶于W的最高价氧化物的水化物的稀溶液,却不溶于其浓溶液,铝、铁能溶于稀硫酸却不溶于浓硫酸,Z是短周期主族元素,所以Z是Al,W是S元素,Q属于短周期主族元素且原子序数大于S,所以Q是Cl元素,
A.Y是O元素,O元素没有正化合价,故A错误;
B.电子层数越多,其离子半径越大,电子层结构相同的离子,离子半径随着原子序数的增大而减小,X、Y、Z离子的电子层结构相同,且原子序数Z>Y>X,所以离子半径X>Y>Z,W、Q离子的电子层结构相同,且W的原子序数小于Q,所以离子半径W>Q,W、Q离子的电子层数大于X、Y、Z,则离子半径大小顺序是W>Q>X>Y>Z,故B错误;
C.W是S元素,Q是Cl元素,Cl元素的非金属性大于O元素,气态氢化物的稳定性大小为:Q>W,故C正确;
D.W的非金属性小于Q,则W的最高价氧化物的水化物的酸性小于Q,故D错误;
故选C.
点评 本题考查了原子结构和元素周期律的关系,题目难度中等,正确推断元素是解本题关键,结合元素周期律来分析解答即可,注意离子半径大小的比较方法,为易错点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
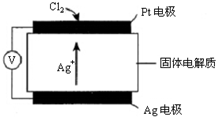 氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱,以及生产ClO2和氯的含氧酸盐(NaClO、NaClO3)等系列化工产品.
氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱,以及生产ClO2和氯的含氧酸盐(NaClO、NaClO3)等系列化工产品.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
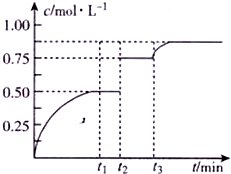 一定温度下,将1mo1X、1molY和1molW充入2L恒容密闭容器,发生反应X(g)+Y(g)?mZ(g)+W(s),t1时达到平衡.在t1、t2时刻分别改变影响反应的一个条件,测得容器中气体Z的浓度随时间变化如图所示.下列说法正确的是( )
一定温度下,将1mo1X、1molY和1molW充入2L恒容密闭容器,发生反应X(g)+Y(g)?mZ(g)+W(s),t1时达到平衡.在t1、t2时刻分别改变影响反应的一个条件,测得容器中气体Z的浓度随时间变化如图所示.下列说法正确的是( )| A. | 反应方程式中的m=2 | |
| B. | t2时刻改变的条件是加人了催化剂或加压 | |
| C. | t3时刻改变的条件是移去少里物质W | |
| D. | t3时刻改变的条件可能是增加了X的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知氢气的燃烧热为285.8kJ/mol,相应的热化学方程式为H2(g)+$\frac{1}{2}$O2(g)═H2O(g),△H=-285.8 kJ/mol | |
| B. | 中和相同体积、相同物质的量浓度的①硫酸,②盐酸和③醋酸所需相同浓度的NaOH溶液的体积关系:V1>V2=V3 | |
| C. | 稀氨水中部分粒子的浓度大小关系:c(NH3•H2O)>c(OH-)>c(NH${\;}_{4}^{+}$)>c(H+) | |
| D. | 1mol/LNaX和1mol/LNaY两种盐溶液中c(X-)═c(Y-)+c(HY),则HX为强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
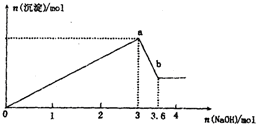 现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图.
现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
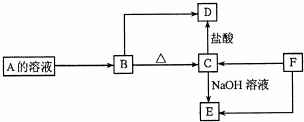
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com