
Ϊ̽��H2O2��SO2��Br2������ǿ����ijС��ͬѧ�������ʵ�飨�гּ�β������װ������ȥ���������Ѽ��飩��
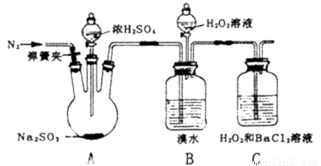
ʵ����� | ʵ������ |
i����A�з�Һ©���������μ�Ũ���� | A�������ݲ�����B�к���ɫ��ˮ��ɫ��C���а�ɫ���� |
ii��ȡC�г����������� | C�а�ɫ�������ܽ� |
iii����B�з�Һ©����������εμ�H2O2 | ��ʼʱ��ɫ�����Ա仯�������μ�H2O2��Һ��һ��ʱ����Һ��ɺ���ɫ |
��1��A�з�����Ӧ�Ļ�ѧ����ʽ�� ��
��2����ͬѧͨ��C�в�����ɫ�������ó����ۣ������ԣ�H2O2>SO2��
����ͬѧ��Ϊ���ܵó��˽��ۣ���Ϊ�ڵμ�Ũ����֮ǰӦ����һ���������ò����� ��
�ڱ�ͬѧ��Ϊ��Ӧ����B��C֮������ϴ��ƿD��D��ʢ�ŵ��Լ��� ��
��iii�е�������H2O2û�����Ա仯��������裺
�۵�1��H2O2�����ٲ�������Br-
�۵�2��B����δ��Ӧ��H2SO3
Ϊ��֤�۵�2��Ӧ���е�ʵ������������� ��
��4��ͨ������ȫ��ʵ�飬�ó����ۣ�H2O2��SO2��Br2��������ǿ������˳���� ��
��1��Na2SO3(��)��H2SO4(Ũ)=Na2SO4��SO2����H2O����2���ٴ��ɼУ�ͨ��N2�����ž�װ����
�����رյ��ɼУ���CCl4������NaHSO3��Һ������3��ȡ�����μ�H2O2��Һǰ��B����Һ���Թ��У����ȣ�������ͨ��Ʒ����Һ�У�Ʒ����Һ��ɫ����4��H2O2>Br2>SO2��
��������
�����������1����A��Ũ������Na2SO3�������ֽⷴӦ����SO2���壬�÷�Ӧ�Ļ�ѧ����ʽ��Na2SO3(��)��H2SO4(Ũ)=Na2SO4��SO2����H2O����������װ���к��п����������е�������SO2����Һ��Ҳ�ᷢ����Ӧ����������������ͬѧ��Ϊ���ܵó��˽��ۣ���Ϊ�ڵμ�Ũ����֮ǰӦ����һ���������ò����Ǵ��ɼУ�ͨ��N2�����ž�װ���ڿ����رյ��ɼУ��������嵥���лӷ��ԣ��嵥��Ҳ���Խ�SO2��������ͬ����ʵ���������Ա�ͬѧ��Ϊ��Ӧ����B��C֮������ϴ��ƿD����ȥ�ӷ�����������D��ʢ�ŵ��Լ���CCl4��NaHSO3��Һ������H2SO3���ȶ����������ֽ������Ư���Ե�SO2������Ϊ��֤�۵�2��Ӧ���е�ʵ������������ǣ�ȡ�����μ�H2O2��Һǰ��B����Һ���Թ��У����ȣ�������ͨ��Ʒ����Һ�У�Ʒ����Һ��ɫ����4�������ڷ���������ԭ��Ӧ����ǿ�������ɣ�����ͨ��ʵ��ó����ۣ�H2O2��SO2��Br2��������ǿ������˳����H2O2>Br2>SO2��
���㣺SO2�����ʵ�����Ʒ� ������ԭ��Ӧ���ɣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015���㽭ʡ����10���¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
��14�֣�Ϊ�о����ʲ�������Ũ����ķ�Ӧ��ijѧϰС����̼�ظ�(������̼�ĺϽ�)����������̽�����
��̽��һ��
��1�������£���ҵ������������ʢ�����Ũ���ᣬ��ԭ���� ��
��2����ȡ̼�ظ�6.0g����15.0mLŨ�����У����ȣ���ַ�Ӧ��õ���ҺX���ռ����������Y��
�ټ�ͬѧ��ΪX�г�Fe3+֮����ܺ���Fe2+����Ҫȷ�����е�Fe2+��Ӧѡ�� ��ѡ����ţ���a��KSCN��Һ����ˮ b�����ۺ�KSCN��Һ c��Ũ��ˮ d������KMnO4��Һ
����ͬѧȡ560mL(��״��)����Yͨ��������ˮ�У�Ȼ���������BaCl2��Һ�����ʵ�������ø������4.66g���ɴ˿���������Y��SO2�����������
д��̽�����г��ֵ��������ӷ�Ӧ����ʽ ��
��̽������
��������ʵ����SO2��������ķ�������ͬѧ��Ϊ����Y�л����ܺ���Q1��Q2�������壬����Q1���壬�ڱ�״���£��ܶ�Ϊ0.0893g��L-1��Ϊ�����������̽��ʵ��װ�ã�ͼ�мг�����ʡ�ԣ������й�������ȫ��Ӧ����
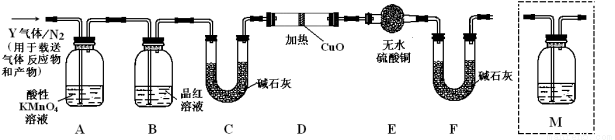
��3��װ��B���Լ��������� ��
��4������Y�����е�Q2������������ɵ� �����û�ѧ����ʽ��ʾ����
��5��Ϊȷ��Q2�Ĵ��ڣ�����װ��������ϴ��ƿM�� ��ѡ����ţ���
a��A֮ǰ b��A-B�� c��B-C�� d��C-D��
��6���������Y�к���Q1��Ԥ��ʵ������Ӧ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����֣���и����ϵ�һ�Σ�10�£��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪�����ȡ��塢�⡢��Ϊͬһ����Ԫ�أ������廯����AtBr���ɷ������·�Ӧ��
�� 2AtBr + 2Mg = MgAt2 + MgBr2 �� AtBr + 2NH3 = NH4Br + AtNH2
������������Ӧ���й�˵������ȷ���ǣ� ��
A����������Ӧ����������ԭ��Ӧ
B����Ӧ����MgAt2���������������ǻ�ԭ����
C����Ӧ����AtBr�������������ǻ�ԭ��
D��MgAt2�Ļ�ԭ������MgBr2��ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ10��������ѧ�Ծ��������棩 ���ͣ�ѡ����
����ȩ����������Ʊ�1��������Ϊ�ᴿ����������ȩ���ʵ�1�����������������·�ߣ�

��֪��������ȩ�뱥��NaHSO3��Һ��Ӧ�����ɳ����������ѵķе���34�棬������ˮ����1���������ܣ���1�������ķе���118�档�����1��4�ֱ���( )
A����ȡ�����ˡ��������� B�����ˡ���Һ��������ȡ
C�����ˡ������ˡ����� D�����ˡ���Һ�����ˡ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ10��������ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������ΰ��ջ��������������ʺͷǵ���ʵ�˳�����е�һ����( )
A�����ۡ�CuO��HClO��Cu
B��ˮ������Na2O��CaO��6SiO2��AgO��SO3
C��KAl(SO4)2��12H2O��KClO3��NH3��H2O��CH3CH2OH
D����ͨ������H2O��Fe(SCN)3��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ�����и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʵ�ת���ڸ�����������ʵ�ֵ���
��NaAlO2(aq) AlCl3
AlCl3 Al
Al
��NH3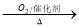 NO
NO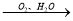 HNO3
HNO3
��NaCl��������Һ�� NaHCO3
NaHCO3 Na2CO3
Na2CO3
��FeS2 SO3
SO3 H2SO4
H2SO4
A���ڢ� B���٢� C���ڢ� D���ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ�����и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и�����������©��������ƿ�۵ζ��ܢܷ�Һ©������ƽ����Ͳ�߽�ͷ�ιܢ�������ƿ�����������ʷ������
A���٢ۢ� B���ڢޢ� C���٢ܢ� D���ܢޢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ����9�µڶ��νο���ѧ�Ծ��������棩 ���ͣ�ѡ����
����˼ά�ǻ�ѧ�����г��õ�һ��˼ά�����������йط�Ӧ����ʽ��������ȷ���� ( )
| ��֪ | ���� |
A | ��Fe����CuSO4��Һ�У�Fe+Cu2+��Cu+Fe2+ | ��Na���뵽CuSO4��Һ�У�2Na+Cu2+��Cu+2Na+ |
B | ϡ������Ba(OH)2��Һ��Ӧ�����ԣ� 2H++ SO42-+Ba2++2OH-��BaSO4��+2H2O | NaHSO4��Һ��Ba(OH)2��Һ��Ӧ�����ԣ� 2H++SO42-+Ba2++2OH-��BaSO4��+2H2O |
C | ����������Ӧ��2Fe+3Cl2��ȼ2FeCl3 | ���͵ⵥ�ʷ�Ӧ��2Fe+3I12��ȼ2FeI3 |
D | ��Ca(ClO)2��Һ��ͨ������CO2�� Ca2++2ClO- +CO2+H2O��CaCO3��+2HClO | ��Ca(ClO)2��Һ��ͨ������SO2�� Ca2++2ClO-+SO2+H2O��CaSO3��+2HClO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��ˮ�и�����ѧ�ڵ��Ĵμ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
������Һ���������ʵ���Ũ�ȹ�ϵ��ȷ����
A��25��ʱ��pH=7��NH4Cl��NH3��H2O�����Һ��c(H+)= c(OH��)= c(NH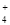 )=c(Cl��)
)=c(Cl��)
B��0.1mol/LNa2S��Һ��c(OH��)=c(H+)+c(HS��)+c(H2S)
C��25��ʱ��pH=2��HCOOH��pH=12��NaOH�������ϣ�c (HCOO��)+ c(H+)>c(Na+)+c(OH��)
D��0.1mol/LNa2CO3��Һ��0.1mol/L NaHCO3��Һ�������ϣ�2c(CO32-)+2c(HCO3-)+2c(H2CO3)=3c(Na+)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com