
 ��п�����ᷴӦ��ʵ���У�һ��ѧ���õ��Ľ�����±���ʾ��
��п�����ᷴӦ��ʵ���У�һ��ѧ���õ��Ľ�����±���ʾ��| ��� | п������/g | п����״ | �¶�/�� | ��ȫ�ܽ� ��ʱ��/s |
| A | 2 | ��Ƭ | 5 | 400 |
| B | 2 | ��Ƭ | 15 | 200 |
| C | 2 | ��Ƭ | 25 | 100 |
| D | 2 | ��Ƭ | 35 | t1 |
| E | 2 | ϸС���� | 15 | t2 |
| F | 2 | ��ĩ | 15 | t3 |
| G | 2 | ��Ƭ������������Cu�� | 35 | t4 |
���� �ɱ����е����ݿ�֪���Ӵ�������¶���Ӱ�췴Ӧ���������أ�
��1��A��B��C��D��Zn����״��ͬ���¶�����10�棬��Ӧʱ��Ϊԭ����һ�룻�ñ������ݻ���ʱ����¶ȵ�����ͼ��
��2���¶ȸߣ���Ӧ���ʿ죻
��3��D��G�У�G����ԭ��أ��ӿ췴Ӧ���ʣ�E��F�У�F��Ӵ������Ӧ���ʿ죻
��4�����ݽӴ������С�ó���Ӧ���ʵĿ�����
��� �⣺�ɱ����е����ݿ�֪���Ӵ�������¶���Ӱ�췴Ӧ���������أ�
��1��A��B��C��D��Zn����״��ͬ���¶�����10�棬��Ӧʱ��Ϊԭ����һ�룬��t1=100s��$\frac{1}{2}$=50s���ñ������ݻ���ʱ����¶ȵ�����ͼ��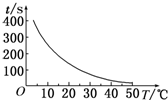 ��
��
�ʴ�Ϊ��50�� ��
��
��2���¶ȸߣ���Ӧ���ʿ죬�����ݿ�֪���÷�Ӧ�¶�����10�棬��ѧ��Ӧ���ʼӿ쵽ԭ����2����
�ʴ�Ϊ����Ӧ�¶�����10�棬��ѧ��Ӧ���ʼӿ쵽ԭ����2����
��3��D��G�У�G���п��γ�Cu-Znԭ��أ���Ӧ���ʼӿ죬��t1��t4��E��F�У�F����пΪ��ĩ״��������ϴ�Ӧ���ʼӿ죬��t2��t3��
�ʴ�Ϊ������G���п��γ�Cu-Znԭ��أ���Ӧ���ʼӿ죻����F����пΪ��ĩ״��������ϴ�Ӧ���ʼӿ죻
��4��B��E��F��F�Ӵ�������B�ĽӴ������С�����Է�Ӧ���ʴ�С˳��Ϊ��F��E��B����λʱ��������п������mB��mE��mF�Ӵ�С��˳��ΪmF��mE��mB��
�ʴ�Ϊ��mF��mE��mB��
���� ���⿼��Ӱ�컯ѧ��Ӧ���ʵ����أ�ע����Ʊ������¶ȡ��Ӵ�����ı仯Ϊ���Ĺ�ϵ�����ճ���Ӱ�����ؼ��ɽ����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֤����ˮ�����ʱ����������Һ�мӼ���ϡ���ᣬˮԡ5min����������������Һ | |
| B�� | ��������������Ԫ��ʱ�����������NaOH��Һ��ϣ�������ú��AgNO3��Һ | |
| C�� | �������Һ�м�ϡ������Ⱥ�NaOH�кͲ���������Ӧ����������Ƿ�ˮ�� | |
| D�� | ��ȥ���л��е��������ӣ�����Ũ��ˮ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ��ʵ | ԭ�� |
| A | ��Ư����Һ�Ի������� | ������������Ư����Һ�з����������� |
| B | ��̼������Һ����ˮ�� | ˮ�����ܽ�Ƚϴ������ת��Ϊ�ܽ�Ƚ�С������ |
| C | �����ʳ���ܱձ����������� | �⻯�ز��ȶ��ֽ⣬�Ӷ���ʧ��Ԫ�� |
| D | �ô�����Һϴ�Ӳ;߱������� | ̼��������֬�������ֽⷴӦ���ɿ����� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ | B�� | NaNO3��Һ | C�� | ���� | D�� | Na2CO3��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
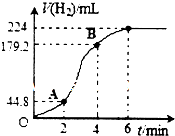 ij�о���ѧϰС�����о�Ӱ��п��ϡ���ᷴӦ���ʵ�����������±�����ʵ����Ƶ��й����ݣ�
ij�о���ѧϰС�����о�Ӱ��п��ϡ���ᷴӦ���ʵ�����������±�����ʵ����Ƶ��й����ݣ�| ʵ�� ��� | п������/g | п�� ״̬ | c��H2SO4��/mol•L-1 | V��H2SO4�� /mL | ��Ӧǰ��Һ���¶�/�� | ���Ӽ� |
| 1 | 0.65 | ��״ | 0.5 | 50 | 20 | �� |
| 2 | 0.65 | ��ĩ | 0.5 | 50 | 20 | �� |
| 3 | 0.65 | ��״ | 0.5 | 50 | 20 | 2��CuSO4��Һ |
| 4 | 0.65 | ��ĩ | 0.8 | 50 | 20 | �� |
| 5 | 0.65 | ��ĩ | 0.8 | 50 | 20 | 2��CuSO4��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ���� | �����£��Թ��������Լ���������/mL | ��������Һ��ɫ������ɫ����ʱ��/min | |||
| 0.6 mol/L H2C2O4��Һ | H2O | 3 mol/L ϡ���� | 0.05mol/L KMnO4��Һ | ||
| 1 | 3.0 | V | 2.0 | 3.0 | 1.5 |
| 2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
| 3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ܶ�����ԭ�������ĵ�����С | |
| B�� | ����������ˮ��Ӧ������������ˮ��Ӧ���ң�﨡�蘆���Ӧ��Ӧ������ | |
| C�� | ����ԭ�������ĵ�����������ʵ��۷е����� | |
| D�� | �����Ԫ�������ӵ�����������ԭ�������ĵ���������ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
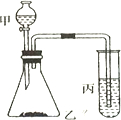 �Ƚ���̼����ķǽ�������ǿ������˳��������и������Լ���ѡ�������ʵ���Լ�����������װ����֤��Ľ��ۣ���ʾ��������ˮ����ʵ���Լ���Ũ���ᡢϡH2SO4������Na2SO3��Һ������ʯ��Na2CO3��ĩ��Na2SiO3��Һ��ʵ��װ�ã���ͼ��ʾ
�Ƚ���̼����ķǽ�������ǿ������˳��������и������Լ���ѡ�������ʵ���Լ�����������װ����֤��Ľ��ۣ���ʾ��������ˮ����ʵ���Լ���Ũ���ᡢϡH2SO4������Na2SO3��Һ������ʯ��Na2CO3��ĩ��Na2SiO3��Һ��ʵ��װ�ã���ͼ��ʾ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
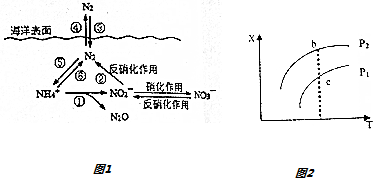
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com