
【题目】磷尾矿难溶于水,主要含Ca5(PO4)3F和CaCO3·MgCO3。某研究小组提出了用磷尾矿制备CaCO3、Mg(OH)2、P4和CO的方案,其工艺流程图如下:
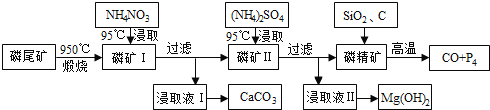
请回答下列问题:
(1)磷精矿[Ca5(PO4)3F]分解温度_______________(填“高于”、“低于” )950℃;
(2)NH4NO3溶液能从磷矿I中浸取出Ca2+的原因是________________,第一次浸取液用NH4NO3而不用的(NH4)2SO4原因是__________________________。
(3)磷精矿与SiO2、C发生反应时被还原的物质是_______________。
(4)其产物CO在工业上有重要的综合应用,现以CO、H2O、熔融Na2O组成的电池装置如图所示。
写出石墨Ⅰ电极上发生反应的电极反应式_______________,Na+向________(填写“石墨Ⅰ”或“石墨Ⅱ”)移动。
(5)CO也可由甲酸(HCOOH)制取,甲酸是易溶于水的一元弱酸。
①常温下关于1 L 0.1 mol·L-1 HCOONa溶液,下列关系不正确的是____________。
a.c(H+)·c(OH-)=1×10-14
b.c(H+)+c(HCOOH)=c(OH-)
c.c(Na+)=c(HCOOH)+c(HCOO-)
d.c(Na+)>c(H+)>c(HCOO-)>c(OH-)
②向1 L 0.1 mol·L-1 HCOONa溶液中加水稀释后,c(HCOOH)·c(OH-)的数值________(填写“增大”“减小”或“不变”)。
【答案】
(1)高于;
(2)NH4+水解使溶液呈酸性,H+能从磷矿I中浸取出Ca2+(或H+与CaO、Ca(OH)2反应生成Ca2+);CaSO4微溶于水,第一次若使用硫酸,不能完全浸取Ca2+
(3)Ca5(PO4)3F
(4)CO+O2-2e-=CO2;石墨Ⅱ;
(5)①d;②减小
【解析】
试题分析:磷尾矿[主要含Ca5(PO4)3F和CaCO3MgCO3]在950℃下煅烧,其中碳酸钙和碳酸镁分解,生成气体的成分为二氧化碳(CO2),磷矿Ⅰ的主要成分为Ca5(PO4)3F、CaO、MgO,NH4NO3溶液中铵离子水解呈酸性,可溶解CaO,得到的浸取液Ⅰ含有Ca2+,可生成CaCO3,磷矿Ⅱ含有Ca5(PO4)3F、MgO,加入硫酸铵浸取,浸取液Ⅱ含有镁离子,可生成氢氧化镁,磷精矿加入二氧化硅、C等,在高温下发生4Ca5(PO4)3F+18SiO2+30C![]() 2CaF2+30CO+18CaSiO3+3P4。
2CaF2+30CO+18CaSiO3+3P4。
(1)根据流程图,在950℃煅烧是磷精矿[Ca5(PO4)3F]未分解,因此磷精矿的分解温度高于950℃,故答案为:高于;
(2)NH4+水解使溶液呈酸性,H+能从磷矿I中浸取出Ca2+;CaSO4微溶于水,第一次若使用硫酸,不能完全浸取Ca2+,因此第一次浸取液用NH4NO3而不用的(NH4)2SO4,故答案为:NH4+水解使溶液呈酸性,H+能从磷矿I中浸取出Ca2+;CaSO4微溶于水,第一次若使用硫酸,不能完全浸取Ca2+;
(3)根据流程图,磷精矿加入二氧化硅、C等,在高温下发生4Ca5(PO4)3F+18SiO2+30C![]() 2CaF2+30CO+18CaSiO3+3P4,反应中P元素化合价降低,被还原,被还原的物质是Ca5(PO4)3F,故答案为:Ca5(PO4)3F;
2CaF2+30CO+18CaSiO3+3P4,反应中P元素化合价降低,被还原,被还原的物质是Ca5(PO4)3F,故答案为:Ca5(PO4)3F;
(4)石墨Ⅰ为负极,电极反应式为CO+O2-2e-=CO2;原电池中阳离子向正极移动,因此Na+向石墨Ⅱ移动,故答案为:CO+O2-2e-=CO2;石墨Ⅱ;
(5)①a.常温下,水的离子积常数c(H+)·c(OH-)=1×10-14,正确;b.根据质子守恒,有c(H+)+c(HCOOH)=c(OH-),正确;c.根据物料守恒有c(Na+)=c(HCOOH)+c(HCOO-),正确;d.HCOONa溶液水解显碱性,水解程度一般较小,c(Na+)>c(HCOO-) >c(H+)>c(OH-),错误;故选d;
②向1 L 0.1 mol·L-1 HCOONa溶液中加水稀释后,促进水解,c(HCOO-) 减小,温度不变,水解常数不变,K=![]() , c(HCOOH)·c(OH-)减小,故答案为:减小。
, c(HCOOH)·c(OH-)减小,故答案为:减小。


科目:高中化学 来源: 题型:
【题目】下列关于SiO2和CO2的叙述中不正确的是
A.都是共价化合物
B.都是酸性氧化物,都能与强碱溶液反应
C.都能溶于水且与水反应生成相应的酸
D.SiO2可用于制光导纤维,干冰可用于人工降雨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组性质比较,不正确的是( )
A.酸性:HClO4>HBrO4>HIO4
B.碱性:NaOH>Mg(OH)2>Al(OH)3
C.稳定性:PH3>H2S>HCl
D.原子半径:Br>Cl>F
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确
A.石油、煤、天然气、油脂都属于化石燃料
B.油脂在碱性条件下的水解反应又称为皂化反应
C.分子式为(C6H10O5)n的淀粉和纤维素互为同分异构体
D.蔗糖是还原性糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】山梨酸是一种常见的食物添加剂,它是一种无色针状晶体或白色粉末,它的结构简式为CH3-CH=CH-CH=CH-COOH。下列关于山梨酸的叙述不正确的是
A.山梨酸易溶于乙醇
B.山梨酸能与氢气发生加成反应
C.山梨酸能和乙醇反应生成酯
D.1mol山梨酸能和金属钠反应生成1mol氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成尿素的反应2NH3(g)+CO2(g)=CO(NH2)2(尿素)+H2O(l) △H<0 分两步进行:①2NH3(g)+CO2(g)→NH4COONH2(s) △H1<0 ②NH4COONH2(s) →CO(NH2)2(尿素)+H2O(l) △H2>0。下列示意图中,能正确表示合成尿素过程中能量变化的是( )
A.  B.
B. 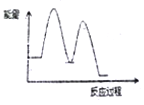 C.
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)一种新型的熔融盐燃料电池具有高发电效率而备受重视。现用Li2CO3和Na2CO3的熔融盐混合物做电解质,一极通入CO气体,另一极通入空气和CO2的混合气体,制得燃料电池。该电池工作时的负极反应式为_____________; 熔融盐中CO32-的物质的量在工作时__ (填“增大”、“减少”、“不变”)。
(2)如下图所示,A为电源,B为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,C、D为电解槽,其电极材料及电解质溶液见图。关闭K1,打开K2,通电后,B的KMnO4紫红色液滴向c端移动,则电源a端为_____极,通电一段时间后,观察到滤纸d 端出现的现象是:___________;
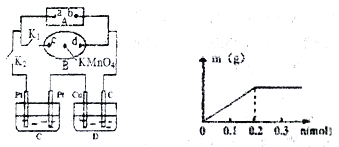
己知C装置中溶液为Cu(NO3)2和X(NO3)2,且均为0.1mol, D装置中的溶液为CuSO4溶液,打开K1,关闭K2,通电一段时间后,C装置阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如右图所示。则Cu2+、X3+氧化能力由大到小的顺序是__ ;D装置C 极的电极反应式为____________。
(3)最近,又有科学家制造出一种使用固体电解质的燃料电池,其效率更高。一个电极通入空气,另一个电极通入汽油蒸汽。其中固体电解质是掺杂了Y2O3(Y:钇)的ZrO2(Zr:锆)固体,它在高温下能传导O2—离子(其中氧化反应发生完全)。以丁烷(C4H10)代表汽油,①电池的正极反应式为________;②放电时固体电解质里的O2-离子的移动方向是向_______极移动(填正或负)。
(4)某同学利用反应Cu+2H+=Cu2++H2↑设计实验来制取氯化铜溶液。该同学设计的装置应该为______。(填“原电池”或“电解池”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com