
【题目】氮化镓( GaN)是制造SG芯片的材料,氮化铝LED灯可发出紫外光。回答下列问题:
(1) Ga的价电子排布式为____,该基态原子占据最高能级的电子云轮廓图形状为________。
下列状态的铝中,电离最外层的一个电子所需能量最小的是____(填字母)。
![]()
(2)8 -羟基喹啉铝常用于发光材料及电子传输材料,可由LiAlH4与 合成。LiAlH4中阴离子的空间构型为_____________,
合成。LiAlH4中阴离子的空间构型为_____________, 所含元素中电负性最大的是____(填元素符号),N的杂化方式为________________
所含元素中电负性最大的是____(填元素符号),N的杂化方式为________________
(3)金属晶体Al、Ga的熔点分别为660℃、30℃,Al比Ga熔点高的原因是____________
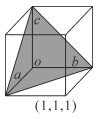
(4)氮化镓为六方晶胞,结构如右图所示。该晶体密度为ρg/cm3,晶胞参数a=b≠c(单位:pm),a、b夹角为120°,阿伏加德罗常数的值为NA,则晶胞参数c=____pm(用含a、ρ、NA的代数式表示)。

(5)在立方晶胞中,与晶胞体对角线垂直的面在晶体学中称为(1,1,1)晶面。如右图,该立方晶胞中(1,1,1)晶面共有____个。
【答案】4s24p1 哑铃形 D 正四面体 O sp2 Al和Ga均为金属晶体,且二者的价电子数相同,但Al的原子半径比Ga的原子半径小,所以Al的熔点高 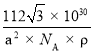 8
8
【解析】
(1)Ga位于第四周期IIIA族,价电子为最外层电子,电子占据最高能级为4p能级;
(2)利用价层电子对数进行分析AlH4-的空间构型;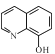 中含有元素的是C、H、N、O,然后判断电负性大小;利用杂化轨道数等于价层电子对数,判断杂化方式;
中含有元素的是C、H、N、O,然后判断电负性大小;利用杂化轨道数等于价层电子对数,判断杂化方式;
(3)Al、Ga为金属晶体,通过比较金属键的强弱,分析金属晶体熔沸点高低;
(4)利用晶胞的密度计算参数;
(5)根据晶面的含义分析;
(1)Ga位于第四周期IIIA族元素,Ga的价电子为最外层电子数,价电子排布式为4s24p1;电子占据最高能级为4p,电子云轮廓图形状为哑铃形或纺锤形;
A.为基态Al失去两个电子后的状态,电离最外层的一个电子为Al原子的第三电离能;
B. 为基态Al失去一个电子后的状态,电离最外层的一个电子为Al原子的第二电离能;
C. 为基态Al3+,2p能级全充满,较稳定,电离最外层的一个电子为Al原子的第四电离能;
D. 为Al原子的核外电子排布的激发态;
电离最外层的一个电子所需要的能量:基态大于激发态,而第一电离能<第二电离能<第三电离能<第四电离能,则电离最外层的一个电子所需能量最小的D;
(2)阴离子是AlH4-,中心原子Al含有4个σ键,孤电子对数为![]() =0,价层电子对数为4,空间构型为正四面体形;
=0,价层电子对数为4,空间构型为正四面体形; 中含有元素为C、H、O、N,同周期从左向右电负性逐渐增大,同主族从上到下电负性逐渐减小,因此电负性最大的是O;根据结构简式,N有2个σ键,1对孤电子对,即杂化方式为sp2;
中含有元素为C、H、O、N,同周期从左向右电负性逐渐增大,同主族从上到下电负性逐渐减小,因此电负性最大的是O;根据结构简式,N有2个σ键,1对孤电子对,即杂化方式为sp2;
(3)Al、Ga为金属晶体,影响其熔点的是金属键,金属键与价电子、原子半径有关,Al和Ga均为金属晶体,且二者的价电子数相同,但Al的原子半径比Ga的原子半径小,所以Al的熔点高;
(4)Ga位于顶点和体内,个数为![]() =2,N位于棱上和体内,个数为
=2,N位于棱上和体内,个数为![]() =2,该晶胞的质量为
=2,该晶胞的质量为![]() g,晶胞的体积为(a×10-10)2sin60°×c×10-10cm3,根据密度的定义得出ρg/cm3=
g,晶胞的体积为(a×10-10)2sin60°×c×10-10cm3,根据密度的定义得出ρg/cm3=![]() g÷[(a×10-10)2sin60°×c×10-10cm3],解得c=
g÷[(a×10-10)2sin60°×c×10-10cm3],解得c=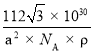 pm;
pm;
(5) 在立方晶胞中,与晶胞体对角线垂直的面在晶体学中称为(1,1,1)晶面,有8个顶点,即有8个这样的面,该立方晶胞中(1,1,1)晶面共有8个。


科目:高中化学 来源: 题型:
【题目】某化学课外活动小组拟用铅蓄电池为直流电源,进行电絮凝净水的实验探究,设计的实验装置如图所示。下列说法正确的是

A.Y电极反应为Pb+SO42--2e-=PbSO4
B.每消耗103.5gPb, 理论上电解池阴极上有1molH2生成
C.该电解池的总反应为2Al+6H2O![]() 2Al(OH)3+3H2↑
2Al(OH)3+3H2↑
D.若污水为含有Cr2O72-工业酸性废水,为将其转化为Cr3+除去,可让铁电极连接铅蓄电池的正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化亚铜是一种附加值较高的铜类物质,下列流程是利用再生资源回收高品质氧化亚铜。某兴趣小组通过查阅资料得知CuCI可溶于![]() 浓度较大的体系,能被硝酸氧化,在碱性条件下易水解转化为
浓度较大的体系,能被硝酸氧化,在碱性条件下易水解转化为![]() ,
,![]() 在酸性条件下可歧化为
在酸性条件下可歧化为![]() 和Cu。据此设计了如下实验方案。下列说法正确是( )
和Cu。据此设计了如下实验方案。下列说法正确是( )

A.生成CuCl的离子方程式为![]()
B.为确保![]() 完全沉淀,应向含铜废液中加入过量的NaCl
完全沉淀,应向含铜废液中加入过量的NaCl
C.检验制得的![]() 中是否含有CuCl,可用硝酸银和硝酸
中是否含有CuCl,可用硝酸银和硝酸
D.可直接向含铜废液中加入葡萄糖,在碱性条件下制得![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA是阿伏加德罗常数的值,下列说法正确的是
A.若1molFeCl3跟水完全反应转化为氢氧化铁胶体后,其中胶体粒子的数目为NA
B.将一定量的Cl2通入FeBr2溶液中,当有1molBr-转化为Br2时,转移的电子数为NA
C.44.0g环氧乙烷中含有6.0NA个极性键
D.1molCaO2晶体中含离子总数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲图为一种新型污水处理装置,该装置可利用一种微生物将有机废水的化学能直接转化为电能;乙图是含Cr2O72-酸性废水的处理装置。将甲、乙两装置连接[Fe(Ⅱ)极与X极连接],可将Cr2O72-转化成Cr(OH)3沉淀而除去。下列说法错误的是
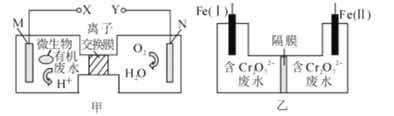
A.若废水中含有乙醛,则M极的电极反应为:CH3CHO+2H2O-8e-=2CO2↑+8H+,
B.电解一段时间后,在Fe(I)极附近有沉淀析出
C.装置乙的隔膜是阳离子交换膜
D.电路中每转移3 mol电子,最多有0.5 mol Cr2O72-被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
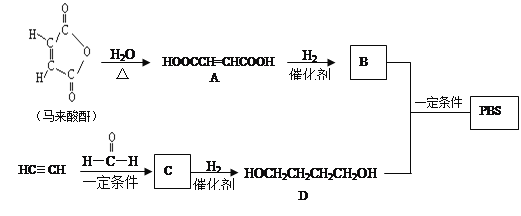
【题目】PBS是一种可降解的聚酯类高分子材料,可由马来酸酐等原料经下列路线合成:
(已知:![]() +
+
![]()
 )
)
(1)A→B的反应类型是____________;B的结构简式是______________________。
(2)C中含有的官能团名称是________;D的名称(系统命名)是____________。
(3)半方酸是马来酸酐的同分异构体,分子中含1个环(四元碳环)和1个羟基,但不含—O—O—键。半方酸的结构简式是___________________。
(4)由D和B合成PBS的化学方程式是______________________________________。
(5)下列关于A的说法正确的是__________。
a.能使酸性KMnO4溶液或溴的CCl4溶液褪色
b.能与Na2CO3反应,但不与HBr反应
c.能与新制Cu(OH)2反应
d.1molA完全燃烧消耗5molO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是一种药物合成中间体,其合成路线如下:
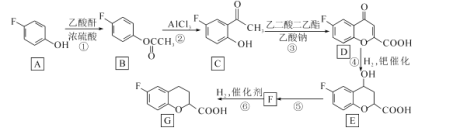
已知:乙酸酐的结构简式为![]() 。请回答下列问题:
。请回答下列问题:
(1)G中含氧官能团的名称是______________
(2)反应①的化学方程式为__________________
(3)反应⑤所需的试剂和条件是____,该反应类型是______________
(4)写出满足下列条件的C的同分异构体的结构简式________________________。
I.苯环上只有两种取代基;Ⅱ,核磁共振氢谱图中只有4组吸收峰;Ⅲ.能与NaHCO3溶液反应生成CO2。
(5)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。则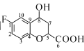 中的手性碳是____(填碳原子的数字标号)。
中的手性碳是____(填碳原子的数字标号)。
(6)设计以![]() 为原料制备
为原料制备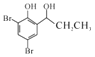 的合成路线(无机试剂任选)。
的合成路线(无机试剂任选)。
_____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分为Al2O3,还有少量杂质)中提取铝的工艺流程及步骤如下:
试回答下列问题。
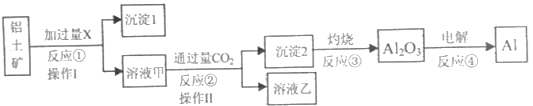
(1)试剂X为___;反应①的离子方程式为___。
(2)操作Ⅰ、操作Ⅱ均为___(填操作名称)。反应①②③④中属于氧化还原反应的是___(填数字序号)。
(3)反应②的离子方程式为___。
(4)金属铝与氧化铁的混合物在高温下会发生剧烈的反应,该反应的化学方程式为___。(5)电解熔融氧化铝制取金属铝,若有0.6mol电子发生转移,理论上能得到金属铝的质量是___g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将①50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:
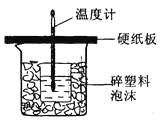
(1) 从实验装置上看,图中尚缺少的一种玻璃用品是__________________,烧杯间填满碎塑料泡沫的作用是_________________________________。
(2) 若将盐酸换成同浓度和同体积的醋酸,则求得的中和热数值_________(填“偏大”、“偏小’、“无影响”)
(3) 实验中改用40 mL 0.50 mol/L的盐酸跟50mL 0.55 mol/L的NaOH溶液进行反应,与上
述实验相比,所放出的热量_________(填“比①大”、 “比①小”或“相等”),理由是_____________________________________________;所求中和热的数值会________(填“相等”或“不相等”),理由是_______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com