
【题目】己知反应A+3B=2C+D,在某段时间内以A的浓度变化表示的化学反应速率为1 mol/(L.min),则此段时间内以C的浓度变化表示的化学反应速率为( )
A.0.5 mol/(L·min)B.1 mol/(L·min)C.2 mol/(L·min)D.3 mol/(L·min)
科目:高中化学 来源: 题型:
【题目】下列各组溶液中的各种溶质的物质的量浓度均为0.1 mol/L。①H2S溶液;②KHS溶液;③K2S溶液;④H2S和KHS混合溶液。 下列说法正确的是
A. 溶液pH从大到小的顺序是:③ > ② > ① > ④
B. 在KHS溶液中有:c(H+) + c(K+) = c(OH-) + c(HS-) + c(S2-)
C. c(H2S)从大到小的顺序是:① > ④ > ③ > ②
D. 在H2S和KHS混合溶液中有:c(H2S) + c(HS-) + c(S2-) = 2c(K+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,回答下列问题:
CuSO4+SO2↑+2H2O,回答下列问题:
(1)用“双线桥法”标出电子转移的方向和数目________________。
(2)请用化学式写出该反应中的还原剂是__________;氧化剂是__________;氧化产物是__________。
(3)还原剂和还原产物物质的量之比__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在恒容密闭容器中,能表示反应X(g)+2Y(g) ![]() 2Z(g)一定达到化学平衡状态的是( )
2Z(g)一定达到化学平衡状态的是( )
①X、Y、Z的物质的量之比为1∶2∶2
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成n mol Z,同时生成2n mol Y
A. ①② B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以软锰矿(主要成分为MnO2) 为主要原料制备高锰酸钾(KMnO4)的工艺流程如下:
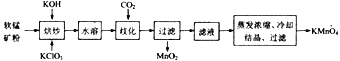
回答下列问题:
(1)原料软锰矿在使用之前通常需粉碎,其目的是_________________________________。
(2)“烘炒”时是将混合物放入某种材质的坩埚内,混合均匀,小火加热至熔融,有K2MnO4和KCl生成,则烘炒过程中发生反应的化学方程式为________________;“烘炒”时所用坩埚的材质可以选用_______(填字母)。
a.石英 b.氧化铝 c.硅酸盐陶瓷 d.铁
(3)已知水溶过程中无化学反应发生,通入CO2使反应体系呈中性或弱酸性即可发生歧化反应,则歧化时发生反应的氧化产物与还原产物的物质的量之比为_______________。
(4)对滤液进行蒸发浓缩时,温度不宜超过60℃,其原因是_________________;将蒸发温度控制在60℃左右的最佳操作方法是_______________________。
(5)流程中可以循环利用的物质是___________________。
(6)用CO2歧化法将K2MnO4转化为KMnO4属于传统工艺,现代工艺多采用电解法,即电解K2MnO4水溶液,电解槽中阳极发生的电极反应为_________________;与“CO2歧化法”相比,“电解法”的显著优点是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以芳香烃A(C7H8)为主要原料合成重要的医药中间体J的流程图如下:
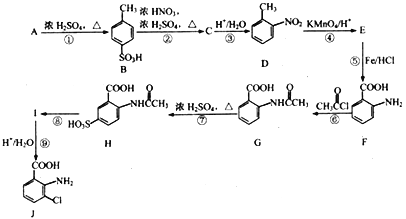
己知:① (-NH2易于被强氧化剂氧化)
(-NH2易于被强氧化剂氧化)
②![]()
③![]()
回答下列问题:
(1)A的结构简式为__________,其分子中不同化学环境的氢原子的个数比为__________。
(2)B→C 的化学方程式为_____________________,反应④的反应类型为__________。
(3)反应⑧所需试剂和条件为___________;E中含氧官能团的名称为_____________。
(4)反应⑥和⑦的顺序是否可以交换过来?__________(选填“是”或“否”)。分析⑥→⑨步的反应,其中反应⑥的主要目的是_____________________。
(5)K是J的同分异构体,其苯环上的取代基与J的相同但位置不同,则K可能的结构有__________种。
(6)请参照题中所示合成路线,以苯和![]() 为原料(无机试剂任选),设计制备
为原料(无机试剂任选),设计制备![]() 的合成路线__________。合成路线示例如下:CH3CH2OH
的合成路线__________。合成路线示例如下:CH3CH2OH![]() CH2=CH2
CH2=CH2![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在3种不同条件下,分别向容积为2L的恒容密闭容器中充入2molA和1molB,发生反应:2A(g)+B(g)![]() 2D(g)△H=QkJ/mol。相关条件和数据见下表:
2D(g)△H=QkJ/mol。相关条件和数据见下表:
实验编号 | 实验I | 实验II | 实验III |
反应温度/℃ | 700 | 700 | 750 |
达平衡时间/min | 40 | 50 | 30 |
n(D)平衡/mol | 1.5 | 1.5 | 1 |
化学平衡常数 | K1 | K2 | K3 |
下列说法正确的是
A. 升高温度能加快反应速率的原理是降低了反应的活化能,使活化分子百分数提高
B. 实验III达平衡后,保持其他条件不变,再向容器中通入1molA和1molD,平衡不移动
C. 实验III达平衡后容器内的压强是实验1的9/10倍
D. K3>K2>K1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲配制80 g质量分数为10%的氢氧化钠溶液,如图是配制该氢氧化钠溶液的实验操作示意图。

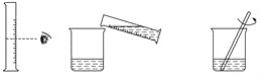
实验步骤
(1)计算:需要氢氧化钠固体__________g,水__________mL(水的密度为1 g·mL-1)。
(2)称量:用托盘天平称取氢氧化钠固体,用规格为__________(填“10mL”“50mL”或“100mL”)的量筒量取所需要的水,倒入盛有氢氧化钠的烧杯中。
(3)溶解:用玻璃棒搅拌,使氢氧化钠固体完全溶解。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com