
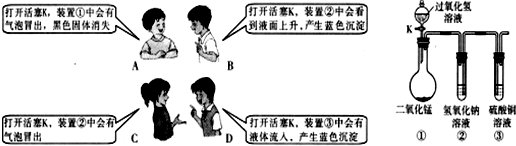
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据过氧化氢在二氧化锰的催化作用下会生成水和氧气,二氧化锰是该反应的催化剂,反应前后质量不变进行分析;
B、根据过氧化氢生成的氧气会增大装置②中的压强进行分析;
C、根据过氧化氢生成的氧气会增大装置②中的压强进行分析;
D、根据过氧化氢生成的氧气会增大装置②中的压强,将氢氧化钠排入装置③中,氢氧化钠和硫酸铜会生成氢氧化铜沉淀进行分析.
解答 解:A、过氧化氢在二氧化锰的催化作用下会生成水和氧气,二氧化锰是该反应的催化剂,反应前后质量不变,故A错误;
B、过氧化氢生成的氧气会增大装置②中的压强,所以装置②中的液面下降,故B错误;
C、过氧化氢生成的氧气会增大装置②中的压强,所以装置②中不会出现气泡,故C错误;
D、过氧化氢生成的氧气会增大装置②中的压强,将氢氧化钠排入装置③中,氢氧化钠和硫酸铜会生成氢氧化铜沉淀,故D正确.
故选D.
点评 本题考查了过氧化氢性质的实验验证,在解此类题时,首选分析题中的反应装置,然后结合方式的反应进行分析题目难度不大.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:填空题
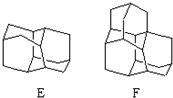 在石油中存在一种有机分子(D),X-射线衍射技术测得其结构高度对称,分子中碳原子的排列方式相当于金刚石晶胞中的部分碳原子排列,故D俗称金刚烷.图给出两种由2,3个D为基本结构单元“模块”像搭积木一样“搭”成的较复杂笼状烷的结构式.金刚烷(D)的结构式为
在石油中存在一种有机分子(D),X-射线衍射技术测得其结构高度对称,分子中碳原子的排列方式相当于金刚石晶胞中的部分碳原子排列,故D俗称金刚烷.图给出两种由2,3个D为基本结构单元“模块”像搭积木一样“搭”成的较复杂笼状烷的结构式.金刚烷(D)的结构式为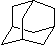 ,其中碳原子的杂化方式为sp3杂化,E的分子式为C14H20.在星际云中也发现一种高度对称的有机分子,分子式为(CH2)6N4,结构类似于金刚烷,俗称四氮金刚烷,它和金刚烷互为C(填标号).
,其中碳原子的杂化方式为sp3杂化,E的分子式为C14H20.在星际云中也发现一种高度对称的有机分子,分子式为(CH2)6N4,结构类似于金刚烷,俗称四氮金刚烷,它和金刚烷互为C(填标号).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碱性氢氧燃料电池的负极反应式:O2+2H2O+4e-=4OH- | |
| B. | 粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ | |
| C. | 用惰性电极分别电解熔融氯化钠和饱和食盐水时,阳极的电极反应式均为:2Cl--2e-=Cl2↑ | |
| D. | 钢铁发生吸氧腐蚀时的正极反应式:Fe-2e-=Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向NaAlO2溶液中通入足量的CO2:2AlO${\;}_{2}^{-}$+CO2+3H2O=2Al(OH)3↓+CO${\;}_{3}^{2-}$ | |
| B. | (NH4)2Fe(SO4)2溶液中加入少量氢氧化钡溶液:NH${\;}_{4}^{+}$+SO${\;}_{4}^{2-}$+Ba2++OH-=BaSO4↓+NH3•H2O | |
| C. | NH4Cl浓溶液中滴加浓NaOH溶液并加热:NH${\;}_{4}^{+}$+OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO${\;}_{3}^{-}$=3Fe3++NO↑+2H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在氧化还原反应中,还原剂一定是失去电子的反应物 | |
| B. | 在氧化还原反应中,非金属单质一定是氧化剂 | |
| C. | 某元素从化合态转变为游离态时,该元素一定被还原 | |
| D. | 金属阳离子被还原不一定得到金属单质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com