
【题目】某温度下,向4.0 L恒容密闭容器中充入2.0 mol PCl5,反应PCl5(g) ![]() PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
时间/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
下列说法正确的是( )
A.反应在前50 s的平均反应速率为v(PCl3)=0.006 4 mol/(L·s)
B.相同温度下,起始时向该容器中充入4.0 mol PCl3、4.0 mol Cl2,达到平衡时,PCl3的转化率小于80%
C.相同温度下,起始时向该容器中充入2.0 mol PCl5、0.4 mol PCl3和0.40 mol Cl2,达到平衡前v(正)>v(逆)
D.保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11 mol/L,则反应的ΔH<0
【答案】C
【解析】
A.反应在前50 s的平均速率为v(PCl3)=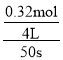 =0.0016 molL-1s-1,故A错误;
=0.0016 molL-1s-1,故A错误;
B.平衡后PCl3物质的量为0.4mol,则可列三段式:

可求出平衡常数K=![]() =0.025,PCl5的转化率为
=0.025,PCl5的转化率为![]() ×100%=20%。相同温度下,若起始时向容器中充入2.0molPCl3、2.0molCl2,和起始时充入2.0molPCl5达到等效平衡,平衡时PCl3的转化率为1-20%=80%。现在起始时充入4.0molPCl3、4.0molCl2,相当于在原平衡的基础上增大压强。增大压强,平衡向PCl5方向移动,PCl3的转化率增大,所以达到平衡时PCl3 的转化率大于80%,故B错误;
×100%=20%。相同温度下,若起始时向容器中充入2.0molPCl3、2.0molCl2,和起始时充入2.0molPCl5达到等效平衡,平衡时PCl3的转化率为1-20%=80%。现在起始时充入4.0molPCl3、4.0molCl2,相当于在原平衡的基础上增大压强。增大压强,平衡向PCl5方向移动,PCl3的转化率增大,所以达到平衡时PCl3 的转化率大于80%,故B错误;
C.相同温度下,起始时向容器中充入2.0molPCl5、0.40molPCl3和0.40molCl2,物质浓度分别为0.5mol/L,0.1mol/L,0.1mol/L,结合浓度商Qc=![]() =0.02<K=0.025,反应没有达到平衡状态,反应正向进行,达到平衡前v(正)>v(逆),故C正确;
=0.02<K=0.025,反应没有达到平衡状态,反应正向进行,达到平衡前v(正)>v(逆),故C正确;
D.升高温度,平衡时,c(PCl3)=0.11 molL-1,大于图表中PCl3浓度=![]() =0.1mol/L,说明升高温度,平衡正向移动,正反应为吸热反应,△H>0,故D错误;
=0.1mol/L,说明升高温度,平衡正向移动,正反应为吸热反应,△H>0,故D错误;
故选C。


科目:高中化学 来源: 题型:
【题目】一种钌(Ru)基配合物光敏染料敏化太阳能电池的工作原理及电池中发生的主要反应如图所示。下列说法错误的是

A. 电池工作时,光能转变为电能,X为电池的负极
B. 镀铂导电玻璃上发生氧化反应生成I-
C. 电解质溶液中发生反应:2Ru3++3I-![]() 2Ru2++I3-
2Ru2++I3-
D. 电池工作时,电解质溶液中I-和I3-的浓度基本不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研制出一种能在室温下高效催化空气中的甲醛氧化的催化剂,其反应如下:HCHO+O2 ![]() CO2+H2O。下列有关说法正确的是( )
CO2+H2O。下列有关说法正确的是( )
A.反应物和生成物都是非极性分子
B.HCHO 的空间构型为四面体形
C.HCHO、CO2 分子的中心原子的杂化类型不同
D.液态水中只存在一种作用力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
①二氧化硅可与NaOH溶液反应,因此可用NaOH溶液雕刻玻璃;
② 明矾溶于水可水解生成Al(OH)3胶体,因此可以用明矾对自来水进行杀菌消毒;
③ 可用蒸馏法、电渗析法、离子交换法等对海水进行淡化;
④ 从海带中提取碘只需用到蒸馏水、H2O2溶液和四氯化碳三种试剂;
⑤地沟油可用来制肥皂、提取甘油或者生产生物柴油;
⑥石英玻璃、Na2O·CaO·6SiO2、淀粉、氨水的物质类别依次为纯净物、氧化物、混合物、弱电解质。
A. ③⑤⑥ B. ①④⑤ C. 除②外都正确 D. ③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四硼酸钠的阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示。下列说法不正确的是( )
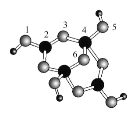
A.阴离子中三种元素的第一电离能:O>B>H
B.在Xm-中,硼原子轨道的杂化类型有sp2和sp3
C.配位键存在于4、5原子之间和4、6原子之间
D.m=2,NamX的化学式为Na2B4O5(OH)4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】EDTA(乙二胺四乙酸)是一种能与Ca2+、Mg2+等结合的螯合剂。某高三研究性学习小组在实验室制备EDTA,并用其测定某地下水的硬度。制备EDTA的实验步骤如下:
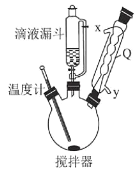
步骤1:称取94.5g(1.0mol)ClCH2COOH于1000mL三颈烧瓶中(如图),慢慢加入50%Na2CO3溶液,至不再产生无色气泡;
步骤2:加入15.6g(0.26mol)H2NCH2CH2NH2,摇匀,放置片刻,加入2.0mol·L-1NaOH溶液90mL,加水至总体积为600mL左右,温度计50℃加热2h;
步骤3:冷却后倒入烧杯中,加入活性炭脱色,搅拌、静置、过滤。用盐酸调节滤液至pH=1,有白色沉淀生成,抽滤,干燥,制得EDTA。测地下水硬度:取地下水样品250mL进行预处理后,用EDTA进行检测。实验中涉及的反应有M2+(金属离子)+Y4-(EDTA)=MY2-;M2+(金属离子)+EBT(铬黑T,蓝色)=MEBT(酒红色);MEBT+Y4-(EDTA)=MY2-+EBT(铬黑T)。
回答下列问题:
(1)步骤1中发生反应的离子方程式为_____。
(2)仪器Q的名称是_____,冷却水从_____接口(填“x”或“y”)流出。
(3)用NaOH固体配制上述NaOH溶液,配制时使用的仪器有托盘天平、药匙、烧杯、玻璃棒、_____和_____,需要称量NaOH固体的质量为_____。
(4)将处理后的水样转移到锥形瓶中,加入氨水-氯化铵缓冲溶液调节pH为10,滴加几滴铬黑T溶液,用0.0100mol·L-1EDTA标准溶液进行滴定。
①确认达到滴定终点的现象是_____。
②滴定终点时共消耗EDTA溶液15.0mL,则该地下水的硬度=_____度(水硬度的表示方法是将水中的Ca2+和Mg2+都看作Ca2+,并将其折算成CaO的质量,通常把1L水中含有10mgCaO称为1度)。
③若实验时装有EDTA标准液的滴定管只用蒸馏水洗涤而未用标准液润洗,则测定结果将_____ (填“偏大“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g) ![]() 2CO2(g)+S(l) ΔH<0,若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
2CO2(g)+S(l) ΔH<0,若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
A.平衡时,其他条件不变,升高温度可提高 SO2 的转化率
B.其他条件不变,缩小容器体积,平衡正反应方向移动,该反应的平衡常数不变
C.平衡前,充入氩气,容器内压强增大,反应速率加快
D.平衡时,其他条件不变,分离出硫,逆反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,三种盐的沉淀溶解平衡曲线如图所示,已知pM为阳离子浓度的负对数,pR为阴离子浓度的负对数,下列说法正确的是

A.Y点:![]() ,Z点:
,Z点:![]()
B.溶度积:Ksp(MnCO3)>Ksp(CaCO3)>Ksp(CaSO4)
C.X点对应的CaCO3溶液为不饱和溶液,可以继续溶解CaCO3
D.T℃时,![]() 的平衡常数K的数量级为103
的平衡常数K的数量级为103
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是用两个石墨作电极,电解饱和Na2SO4溶液的装置,U形管内的电解液中事先加有酚酞指示剂。回答下列问题:
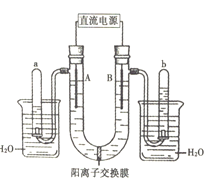
(1)根据图示中倒扣试管内的液面高度,判断直流电源左端为______极,Na+通过阳离子交换膜移动的方向为______(填“左→右”或“右→左”)。
(2)电解过程中,有关电极附近溶液颜色变化中正确的是______(填序号)。
①A管溶液由无色变为红色
②B管溶液由无色变为红色
③A管溶液不变色
④B管溶液不变色
(3)写出B管中发生的电极反应______。
(4)检验b管中气体的方法及现象是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com