
| A. | Ksp(AB2)小于Ksp(CD),则化合物AB2的溶解度一定小于化合物CD的溶解度 | |
| B. | 在氯化银的沉淀溶解平衡体系中,加入蒸馏水,氯化银的溶解度增大 | |
| C. | 在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘化银沉淀 | |
| D. | 在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,溶解平衡不移动 |
分析 A.由于AB2与CD分子组成形式不同,因此不能根据Ksp大小来比较溶解度的大小;
B.KSP只与温度有关,与浓度无关;
C.由于AgCl与AgI分子组成形式相同,故Ksp越大,溶解度越大,溶解度大的能转化为溶解度小;
D.稀盐酸能与CO32-反应,促进碳酸钙的沉淀溶解平衡向正方向移动.
解答 解:A.由于AB2与CD分子组成形式不同,因此不能根据KSP大小来比较溶解度的大小,故A错误;
B.KSP只与温度有关,与浓度无关,所以在氯化银的沉淀溶解平衡体系中加入蒸馏水,氯化银的Ksp不变,B错误;
C.由于AgCl与AgI分子组成形式相同,故Ksp越大,溶解度越大,溶解度大的能转化为溶解度小的,因为KSP(AgCl)大于KSP(AgI),故AgI的溶解度小,所以氯化银沉淀能转化为AgI黄色沉淀,故C正确;
D.碳酸钙的沉淀溶解平衡为:CaCO3(s)?Ca2+(aq)+CO32-(aq),加入稀盐酸能与CO32-反应,促进碳酸钙的沉淀溶解平衡向正方向移动,故D错误.
故选C.
点评 本题考查了溶解度大小的比较,影响Ksp的因素,沉淀溶解平衡的移动等,为高频考点,注意把握Ksp与溶解度的不同,把握难溶电解质溶解平衡的影响因素,题目难度一般.


科目:高中化学 来源: 题型:选择题
| A. | 15N中含有7个中子 | |
| B. | N2和N70属于同位素 | |
| C. | N5+中含有36个电子 | |
| D. | 若NH5为离子化合物,则其既含有离子键,又含有共价 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式:CH2CH2 | B. | 乙醇的分子式:CH3CH2OH | ||
| C. | 甲烷的结构式:CH4 | D. | 甲苯的键线式: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 恒温下,向一个4L的密闭容器中充入5.2molH2和2molN2,反应过程中对NH3的浓度进行检测,得到的数据如表所示:
恒温下,向一个4L的密闭容器中充入5.2molH2和2molN2,反应过程中对NH3的浓度进行检测,得到的数据如表所示:| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol•L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
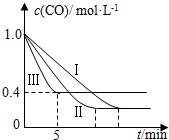 利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值.
利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值.| 编号 | 温度 | 压强 | c始(CO) | c始(H2O) |
| Ⅰ | 530℃ | 3MPa | 1.0mol•L-1 | 3.0mol•L-1 |
| Ⅱ | X | Y | 1.0mol•L-1 | 3.0mol•L-1 |
| Ⅲ | 630℃ | 5MPa | 1.0mol•L-1 | 3.0mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
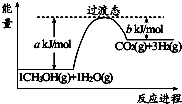
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 2NH3(g)△H=-92kJ•mol-1.
2NH3(g)△H=-92kJ•mol-1.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com