
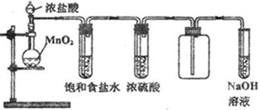
 ʵ���ҿ����ö������̺�Ũ���ᷴӦ��ȡ����������ʽ���£�MnO2+4HCl(Ũ)
ʵ���ҿ����ö������̺�Ũ���ᷴӦ��ȡ����������ʽ���£�MnO2+4HCl(Ũ)
| ||
. |


 ����ͼ���������������ϵ�д�
����ͼ���������������ϵ�д� ����ѧҵ���Ե�����ϵ�д�
����ѧҵ���Ե�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��.ʵ����ͨ���ö������̺�Ũ���ᷴӦ��ȡCl2��
(1)�÷�Ӧ�����ӷ���ʽΪ________________________________________________��
(2)�ס�����ͬѧ���������ַ�����ȡ������
�ף��ú�HCl
�ң���
������Ƶõ�Cl2(�����)_______________��
�ټױ��Ҷ� ���ұȼ� ��һ���� �����Ƚ�
��.��֪���з�ӦҲ��������������
��2KMnO4+16HCl(Ũ)![]() 2KCl+2MnCl2+5Cl2��+8H2O ��4HCl+O2
2KCl+2MnCl2+5Cl2��+8H2O ��4HCl+O2![]() 2Cl2+2H2O
2Cl2+2H2O
��2NaCl+2H2O![]() 2NaOH+H2��+Cl2��
2NaOH+H2��+Cl2��
���У�������ʵ������ȡCl2�ķ�Ӧ��_____________(����ţ���ͬ)�������ڹ�ҵ������Cl2�ķ�Ӧ��_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��.ʵ����ͨ���ö������̺�Ũ���ᷴӦ��ȡCl2��
��1���÷�Ӧ�����ӷ���ʽΪ____________________________________________��
��2���ס�����ͬѧ���������ַ�����ȡ������
�ף��ú�HCl 146 g��Ũ�����������������̷�Ӧ �ң���87 g��������������Ũ���ᷴӦ
������Ƶõ�Cl2������ţ�___________��
�ټױ��Ҷ� ���ұȼ� ��һ���� �����Ƚ�
��.��֪���з�ӦҲ��������������
��2KMnO4+16HCl(Ũ��![]() 2KCl+2MnCl2+5Cl2��+8H2O ��4HCl+O2
2KCl+2MnCl2+5Cl2��+8H2O ��4HCl+O2![]() 2Cl2+2H2O ��2NaCl+2H2O
2Cl2+2H2O ��2NaCl+2H2O![]() 2NaOH+H2��+Cl2��
2NaOH+H2��+Cl2��
���У�������ʵ������ȡCl2�ķ�Ӧ��_____________������ţ���ͬ���������ڹ�ҵ������Cl2�ķ�Ӧ��_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1��1. 5 mol H2O������Ϊ ���������������к��������������� ����ԭ�ӡ�
��2�������ʵ�����CO2��CO���������������� ��������ԭ�ӵĸ������������� ��
������������ͬ��ͬѹ�µ������������������ ��
��3������������ mL 0.2 mol/L NaOH��Һ�к�1 g���ʣ�����50 mL 0.2 mol/L
CuSO4��Һ����ҪCuSO4��5H2O �������������� g��
(4��ʵ���ҿ����ö������̺�Ũ���ᷴӦ��ȡ��������Ӧ�Ļ�ѧ����ʽ���£�
MnO2+4HCl��Ũ��Cl2��+MnCl2+2H2O
����0.1mol���ӷ���ת��ʱ���������������Ϊ������������ ����״������������Ӧ��MnO2������Ϊ������������ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�����ʡ�ܿ��������ظ�һ���ϣ����л�ѧ�Ծ��������棩 ���ͣ������
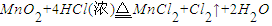 ��ͼ��ijѧ����Ƶ��������Ʊ�����Cl2������װ��ͼ������ͼ�е�װ�ú��й��Լ��ش��������⣮
��ͼ��ijѧ����Ƶ��������Ʊ�����Cl2������װ��ͼ������ͼ�е�װ�ú��й��Լ��ش��������⣮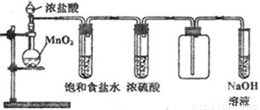
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com