
分析 将混合气体SO2和CO2依次通过①品红是检验二氧化硫气体的存在的;②二氧化硫具有还原性,用氧化剂酸性高锰酸钾,除去二氧化硫;③再通往品红,是验证二氧化硫是否除尽的;④通入澄清石灰水是检验二氧化碳气体存在的,由此分析解答.
解答 解:将混合气体SO2和CO2依次通过品红是检验二氧化硫气体的存在的;二氧化硫具有还原性,用氧化剂酸性高锰酸钾,除去二氧化硫;再通往品红,是验证二氧化硫是否除尽的;通入澄清石灰水是检验二氧化碳气体存在的;
①混合气体通入品红,现象是品红褪色,说明二氧化硫的存在,故答案为:品红褪色;检验二氧化硫的存在;
②通入酸性高锰酸钾,除去还原性的气体二氧化硫,观察到酸性高锰酸钾溶液褪色,作用是除去二氧化硫气体,故答案为:溶液褪色;除去二氧化硫;
③再通入品红,品红不褪色,说明二氧化硫已完全除尽,故答案为:品红不褪色;证明二氧化硫已完全除尽;
④通入澄清石灰水,石灰水变浑浊,说明存在二氧化碳气体,故答案为:石灰水变浑浊;证明存在二氧化碳气体.
点评 本题考查物质的检验与物质组成的测定、对实验装置的理解、元素化合物性质等知识,题目难度中等,掌握元素化合物的性质是解题的关键,注意掌握物质性质实验方案的设计原则,试题培养了学生的分析、理解能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| A. | W元素是硅元素 | |
| B. | 气态氢化物的稳定性:Y<R | |
| C. | X、W、Y的最高价氧化物的水化物酸性强弱顺序是X<Y<W | |
| D. | X、Y、W、R的原子半径由大到小的顺序为R>W>X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
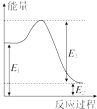 甲烷、一氧化碳和氢气、甲醇等既是重要的燃料也是重要的化工原料.
甲烷、一氧化碳和氢气、甲醇等既是重要的燃料也是重要的化工原料.| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能 (kJ•mol-1) | 348 | 413 | 436 | 358 | 1072 | 463 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 原子半径大小为:B>A>C | B. | 核电荷数:D>C>B>A | ||
| C. | A与D形成的化合物均是离子键 | D. | 生成的氢化物的稳定性为:D>A>B |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 六氟化氙(XeF6) | B. | 次氯酸(HClO) | C. | 三氟化硼(BF3) | D. | 氮气 (N2) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
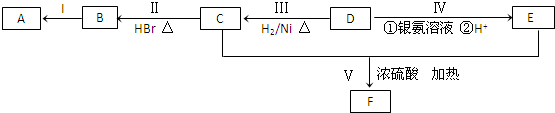
 .
. .
.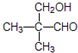 ;②
;② 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
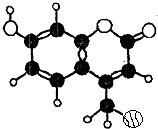 某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成.其一溴代物的分子球棍型如图所示,下列有关该溴代物的叙述正确的是( )
某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成.其一溴代物的分子球棍型如图所示,下列有关该溴代物的叙述正确的是( )| A. | ①②③ | B. | ③④⑤ | C. | ②③④ | D. | ②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该反应放出251.2 kJ的热量 | B. | 该反应吸收251.2 kJ的热量 | ||
| C. | 该反应放出125.6 kJ的热量 | D. | 该反应吸收125.6 kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl、FeCl3、Na2SO4、I2 | B. | NaCl、FeBr3、Na2SO4 | ||
| C. | NaCl、Fe2O3、Na2SO4 | D. | NaBr、FeCl3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com