
ĻņĆܱÕČŻĘ÷ÖŠ³äČėĪļÖŹAŗĶB£¬·¢Éś·“Ó¦aA£Øg£©+bB£Øg£©  cC£Øg£©”£·“Ó¦¹ż³ĢÖŠ£¬ĪļÖŹAµÄŗ¬Įæ£ØA£„£©ŗĶCµÄŗ¬Įæ£ØC£„£©ĖęĪĀ¶Č£ØT£©µÄ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
cC£Øg£©”£·“Ó¦¹ż³ĢÖŠ£¬ĪļÖŹAµÄŗ¬Įæ£ØA£„£©ŗĶCµÄŗ¬Įæ£ØC£„£©ĖęĪĀ¶Č£ØT£©µÄ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
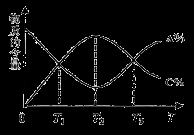
A£®øĆ·“Ó¦ŌŚT1”¢T3ĪĀ¶ČŹ±“ļµ½¹ż»ÆŃ§Ę½ŗā B£®øĆ·“Ó¦ŌŚT2ĪĀ¶ČŹ±“ļµ½¹ż»ÆŃ§Ę½ŗā
C£®øĆ·“Ó¦µÄÄę·“Ó¦ŹĒ·ÅČČ·“Ó¦ D£®ÉżøßĪĀ¶Č£¬Ę½ŗā»įĻņÕż·“Ó¦ ·½ĻņŅʶÆ
·½ĻņŅʶÆ
 æŚĖćĢāæؼÓÓ¦ÓĆĢā¼ÆѵĻµĮŠ“š°ø
æŚĖćĢāæؼÓÓ¦ÓĆĢā¼ÆѵĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğŗž±±Ź”ø߶žÉĻŌĀæ¼Ņ»»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚĪĀ¶ČT1ŗĶT2Ź±£¬·Ö±š½«0.50 mol CH4ŗĶ1.2mol NO2³äČė1 LµÄĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦£ŗ
CH4£Øg£©£«2NO2£Øg£© N2£Ø
N2£Ø g£©£«CO2£Øg£©£«2H2O£Øg£©”÷H=akJ/mol”£²āµĆÓŠ¹ŲŹż¾ŻČēĻĀ±ķ£ŗ
g£©£«CO2£Øg£©£«2H2O£Øg£©”÷H=akJ/mol”£²āµĆÓŠ¹ŲŹż¾ŻČēĻĀ±ķ£ŗ
ĪĀ¶Č | Ź±¼ä/min ĪļÖŹµÄĮæ | 0 | 10 | 20 | 40 | 50 |
T1 | n£ØCH4£©/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n£ØCH4£©/mol | 0.50 | 0.30 | 0.18 | x | 0.15 |
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®T1£¾T2£¬ĒŅa£¾0
B£®µ±ĪĀ¶ČĪŖT2”¢·“Ó¦½ųŠŠµ½40 minŹ±£¬ x£¾0.15
C£®ĪĀ¶ČĪŖT2Ź±£¬ČōĻņĘ½ŗāŗóµÄČŻĘ÷ÖŠŌŁ³äČė0.50 mol CH4ŗĶ1.2mol NO2£¬ÖŲŠĀ“ļµ½Ę½ŗāŹ±£¬n£ØN2£©=0.70mol
D£®ĪĀ¶ČĪŖT1Ź±£¬“ļĘ½ŗāŹ±CH4 µÄ×Ŗ»ÆĀŹ“óÓŚNO2µÄ×Ŗ»ÆĀŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
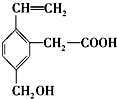
| A£® | ÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ« | |
| B£® | ÄÜ·¢Éśõ„»Æ·“Ó¦ | |
| C£® | ÄÜŌŚĶ×÷“߻ƼĮµÄĢõ¼žĻĀ·¢Éś“ß»ÆŃõ»Æ | |
| D£® | ÄÜÓė4moläåµ„ÖŹ·¢Éś¼Ó³É·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®£ØĘäĖüĪŽ»śĪļČĪŃ”£©
£®£ØĘäĖüĪŽ»śĪļČĪŃ”£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½šøÕŹÆÓėŹÆÄ« | B£® | D2ÓėH2 | ||
| C£® | COÓėCO2 | D£® | ${\;}_{17}^{35}$ClÓė${\;}_{17}^{37}$Cl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
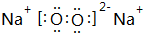
| A£® | ĶłŠĀÅäÖʵÄæÉČÜŠŌµķ·ŪČÜŅŗÖŠµĪ¼ÓµāĖ®£¬ČÜŅŗĻŌĄ¶É«£¬ÓĆCCl4²»ÄÜ“ÓÖŠŻĶČ”³öµā | |
| B£® | µ±ŠæĶźČ«Čܽāŗó£¬ĢśÓėĖį·“Ó¦²śÉśĒāĘųµÄĖŁĀŹ»įĻŌÖų¼õĀż£¬“ĖĻÖĻóæÉ×÷ĪŖÅŠ¶Ļ¶ĘŠæĢśĘ¤ÖŠŠæ¶Ę²ćŹĒ·ńĶźČ«±»·“Ó¦µōµÄŅĄ¾Ż | |
| C£® | ÖʱøĮņĖįŃĒĢśļ§¾§ĢåŹ±£¬×īŗóŌŚÕō·¢ĆóÖŠÕō·¢ÅØĖõČÜŅŗŹ±£¬Ö»ŠčŠ”»š¼ÓČČÖĮČÜŅŗ±ķĆę³öĻÖ¾§Ä¤ĪŖÖ¹£¬²»Äܽ«ČÜŅŗČ«²æÕōøÉ | |
| D£® | ĢįČ”ŗ£“ųÖŠµāŌŖĖŲŹ±£¬ĪŖ±£Ö¤I-ĶźČ«Ńõ»ÆĪŖI2£¬¼ÓČėµÄŃõ»Æ¼Į£ØH2O2»ņŠĀÖĘĀČĖ®£©¾łÓ¦¹żĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

| ŹµŃ鱹ŗÅ | ·“Ó¦Īļ | “߻ƼĮ |
| ¢Ł | 10mL 2% H2O2ČÜŅŗ | ĪŽ |
| ¢Ś | 10mL 5% H2O2ČÜŅŗ | ĪŽ |
| ¢Ū | 10mL 5% H2O2 ČÜŅŗ | 0.1gMnO2·ŪÄ© |
| ¢Ü | 10mL 5% H2O2 ČÜŅŗ+ÉŁĮæHClČÜŅŗ | 0.1gMnO2·ŪÄ© |
| ¢Ż | 10mL 5% H2O2 ČÜŅŗ+ÉŁĮæNaOHČÜŅŗ | 0.1gMnO2·ŪÄ© |
| µŚŅ»“Ī | µŚ¶ž“Ī | µŚČż“Ī | µŚĖÄ“Ī | |
| Ģå»ż£ØmL£© | 17.10 | 18.10 | 18.00 | 17.90 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆĖįŹ½µĪ¶Ø¹ÜĮæČ”20.0mLĖįŠŌøßĆĢĖį¼ŲČÜŅŗ | |
| B£® | ÓĆĆ×ĢĄÖ±½Ó¼ģŃéŹ³ŃĪÖŠŹĒ·ńÓŠµāŌŖĖŲ | |
| C£® | ÓĆ·ÓĢŖ¼ģŃé“æ¼īÖŠŹĒ·ńŗ¬ÓŠÉÕ¼ī | |
| D£® | ¶ą“ĪŃĪĪö»ņ¶ą“ĪÉųĪöµÄ·½·Ø·ÖĄėĢį“æµ°°×ÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
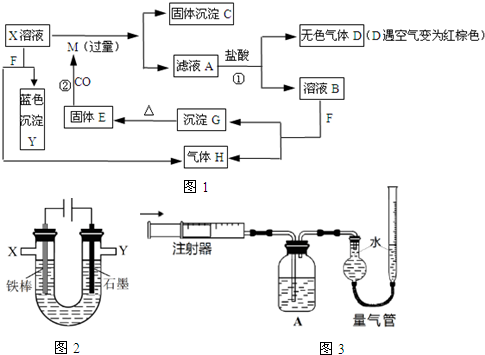
 £»GµÄ»ÆѧŹ½ĪŖFe£ØOH£©3£®
£»GµÄ»ÆѧŹ½ĪŖFe£ØOH£©3£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com