
【题目】有A、B、C、D四种元素,A元素的原子有三个电子层,最外层上有一个电子;B元素负2价阴离子的电子层结构与氩原子相同;C元素的原子核内无中子;D原子核外电子数比A原子核外电子总数多6个。
(1)C与D形成化合物的化学式_______,其在水中的电离方程式为_______。
(2)B离子的电子式_______,A离子的电子式_______。
(3)B原子的结构示意图_______,D离子的结构示意图_______。
【答案】HCl HCl=H++Cl- ![]() Na+
Na+ ![]()
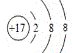
【解析】
由A元素的原子有三个电子层,最外层上有一个电子可知A为Na元素;由B元素负2价阴离子的电子层结构与氩原子相同可知B为S元素;由C元素的原子核内无中子可知C为H元素;由D原子核外电子数比钠原子核外电子总数多6个可知D为Cl元素。
(1)氢元素与氯元素形成的化合物为氯化氢,化学式为HCl,氯化氢在溶液中完全电离,电离出氯离子和氢离子,电离方程式为HCl=H++Cl-;
(2)硫原子得到2个电子形成硫离子,硫离子最外层有8个电子,电子式为![]() ;钠离子为阳离子,其电子式直接用离子符号表示,则钠离子的电子式为Na+;
;钠离子为阳离子,其电子式直接用离子符号表示,则钠离子的电子式为Na+;
(3)硫原子核外有16个电子,有3个电子层, 最外层有6个电子,原子的结构示意图为![]() ;氯原子得到1个电子形成氯离子,氯离子核外有18个电子,有3个电子层, 最外层有8个电子,原子的结构示意图为
;氯原子得到1个电子形成氯离子,氯离子核外有18个电子,有3个电子层, 最外层有8个电子,原子的结构示意图为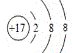 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列四种X溶液,均能跟盐酸反应,其中反应最快的是( )
A. 10 ℃ 3 mol·L-1的X溶液
B. 20 ℃ 3 mol·L-1的X溶液
C. 10 ℃ 2 mol·L-1的X溶液
D. 20 ℃ 2 mol·L-1的X溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(s)+3B(g)=2C(g)+D(g),经2 min后,B的浓度减少了0.6mol/L。下列反应速率的表示正确的是
A. 用A表示的反应速率是0.4 mol/(L·min)
B. 用C表示的反应速率是0.2 mol/(L·min)
C. 2 min末时的反应速率,用B表示是0.3 mol/(L·min)
D. 在这2 min内用B表示的反应速率的值是减小的,C表示的反应速率逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜与浓硝酸反应的方程式为:![]()
(1)在该反应中,被还原的元素是_______,氧化产物是_______。
(2)在方程式标出电子转移的方向和数目_______。
(3)若有32g铜参与反应,被还原的硝酸有_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法不正确的是
A. 标准状况下,2.24LHF与1.8gH2O分子所含电子数目均为NA
B. 14g用于考古测年的14C原子中含中子数为8NA
C. 钠与氧气反应生成1molNa2O2时,转移电子数目为2NA
D. 28g乙烯中含有的共价键数目为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.可逆反应2Cl2(g)+2H2O(g)![]() 4HCl(g)+O2(g)△H>0,在一定条件下达到平衡后,分别采取下列措施(填“增大”、“减小”或“不变”):
4HCl(g)+O2(g)△H>0,在一定条件下达到平衡后,分别采取下列措施(填“增大”、“减小”或“不变”):
(1)降低温度,Cl2的转化率 ________;v正 ________________;
(2)保持容器体积不变,加入He,则HCl的物质的量 _______________________.
(3)保持容器压强不变,加入He,则O2的体积分数 ______________________;
(4)若温度和体积不变,反应从Cl2和H2O开始至平衡,在这个变化过程中,容器内气体的密度 ____________,相对分子质量 ______________________.
Ⅱ.已知CO(g)、H2(g)、CH3OH(l)的燃烧热分别为283kJmol-1、286kJmol-1、726kJmol-1.
利用CO、H2合成液态甲醇的热化学方程式为____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g) + 3B(g) ![]() 2C(g) + 2D(g) 在四种不同情况下的反应速率分别为:①v(A)=0.45mol·L—1·min—1 ② v(B)=0.6mol·L-1·s-1 ③v(C)=0.4mol·L-1·s-1 ④v(D) =0.45mol·mol·L—1·min—1,该反应进行的快慢顺序为
2C(g) + 2D(g) 在四种不同情况下的反应速率分别为:①v(A)=0.45mol·L—1·min—1 ② v(B)=0.6mol·L-1·s-1 ③v(C)=0.4mol·L-1·s-1 ④v(D) =0.45mol·mol·L—1·min—1,该反应进行的快慢顺序为
A. ①>③=②>④ B. ①>②=③>④
C. ②>①=④>③ D. ④>②=③>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,某反应达平衡,平衡常数K=![]() 。恒容时,温度升高,H2浓度减小。下列说法正确的是
。恒容时,温度升高,H2浓度减小。下列说法正确的是
A、该反应的焓变为正值
B、恒温恒容下,增大压强,H2浓度一定减小
C、升高温度,逆反应速率减小
D、该反应化学方程式为CO+H2O=CO2+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元酸(H2A)在水中的电离方程式为H2A===H++HA-,HA-![]() H++A2-(25 ℃时Ka=1.0×10-2),下列有关说法中正确的是( )
H++A2-(25 ℃时Ka=1.0×10-2),下列有关说法中正确的是( )
A. H2A是弱酸
B. 稀释0.1 mol/L H2A溶液,因电离平衡向右移动而导致c(H+)增大
C. 在0.1 mol/L的H2A溶液中,c(H+)=0.12 mol/L
D. 若0.1 mol/L NaHA溶液中c(H+)=0.02 mol/L,则0.1 mol/L的H2A中c(H+)<0.12 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com