
【题目】现有CO和CO2的混合气体20克,其在标准状况下的体积为11.2L。据此回答下列问题:
(1)该混合气体总的物质的量为______,其平均摩尔质量为_______。
(2)混合气体中碳原子的个数为________。(用NA表示阿伏加德罗常数的值)
(3)若将该混合气体全部通过下图装置进行实验。

则:①气球中收集的气体是______,其质量为_______ 克
②从A瓶中获得沉淀质量的操作是_____、称量。
③若要证明A瓶溶液中的阳离子是否沉淀完全,其方法为_______。
【答案】 0.5mol 40g/mol 0.5NA CO 3.5克 过滤、洗涤、干燥 待A瓶中充分沉淀后,取上层清液少许于一支洁净试管中,再滴加稀硫酸溶液,若有白色沉淀产生,说明Ba2+未沉淀完全;反之,则Ba2+已沉淀完全。(其它合理答案也给分)
【解析】试题分析:本题以CO和CO2混合气体的研究为基础,考查物质的量计算、平均摩尔质量的计算、微粒数计算、CO及CO2的性质、物质的分离实验方案、离子检验等基础知识,考查考生有关物质的量的综合计算能力、实验分析能力和运用所学知识解决实际问题的能力。
解析:(1)设混合气体中CO为x mol,CO 为y mol,则28x+44y=20,x+y=11.2/22.4=0.5,解得x=0.125mol,y=0.375mol。M(平均)=20g/0.5mol=40g/mol。正确答案:0.5mol、40g/mol。(2)无论CO还是CO2,每个分子中都只含有1个C 原子,所以混合气体中C原子数等于气体的物质的量为0.5mol,既0.5NA。正确答案:0.5NA。(3)根据图示,混合气体通过Ba(OH)2溶液后,CO2气体被吸收生成BaCO3沉淀,再经过浓硫酸干燥,气球中收集到的是CO气体,其质量为0.125mol×28g/mol=0.35g。从A瓶中得到BaCO3沉淀可以先过滤分离出沉淀,再洗涤、干燥即可。A瓶中的阳离子是Ba2+,检验方法是取上层清液,加入Na2SO4,如果没有白色沉淀产生则说明Ba2+已经完全沉淀,如果有白色沉淀产生则说明Ba2+没有完全沉淀。正确答案:3.5g、过滤,洗涤,干燥、待A瓶中充分沉淀后,取上层清液少许于一支洁净试管中,再滴加的稀硫酸溶液,若有白色沉淀产生,说明Ba2+未沉淀完全;反之,则Ba2+已沉淀完全。


科目:高中化学 来源: 题型:
【题目】人体中的一种脑内分泌物多巴胺,可影响一个人的情绪,主要负责大脑的感觉,将兴奋及开心的信息传递,使人感到愉悦和快乐。它可由香兰素与硝基甲烷缩合,再经锌还原水解而得,合成过程如下:
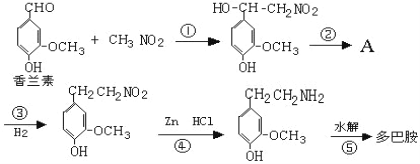
已知多巴胺的结构简式为: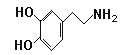 。
。
请回答下列问题:
(1)香兰素除了醛基之外,还含有官能团名称是 、 。
(2)多巴胺的分子式是 。
(3)上述合成过程中属于加成反应类型的是: (填反应序号)。反应②的反应条件是 。
(4)写出符合下列条件的多巴胺的其中一种同分异构体的结构简式: 。
①属于1,3,5-三取代苯; ②苯环上直接连有一个羟基和一个氨基;
③分别能与钠和氢氧化钠反应,消耗钠与氢氧化钠的物质的量之比为2∶1。
(5)请写出有机物A与足量浓溴水反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某晶体的部分结构为正三棱柱(如图所示),这种晶体中A,B,C三种微粒数目之比为( ) 
A.3:9:4
B.1:4:2
C.2:9:4
D.3:8:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾是一种典型的强氧化剂,无论在实验室还是在化工生产中都有重要的应用。下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。

(1)制备氯气选用的药品为:高锰酸钾和浓盐酸,相应的离子方程式为:______________________。
(2)装置B的作用是_______________________。如果B中长颈漏斗液面上升,则说明____________________________________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入________。(选a或b或c)
a | b | c | |
I | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
II | 碱石灰 | 浓硫酸 | 无水氯化钙 |
III | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。当向D中缓缓通入足量氯气时,可以看到无色溶液逐渐变为红棕色,说明氧的非金属性大于溴。打开活塞,将D中的少量溶液加入E中,振荡E,观察到的现象是_______________________________。该现象______(填“能”或“不能”)说明溴的非金属性强于碘,原因是______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,用0.1000mol·L-1稀硫酸滴定20.00mL 0.1000mol·L-1氨水,溶液中水的电离程度随所加稀硫酸体积的变化如图所示。下列说法不正确的是
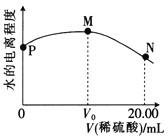
A. 该实验可选择甲基橙作指示剂
B. 从P点到N点,溶液中水的电离程度先增大后减小
C. M点对应的溶液中:c(H+)=c(OH-)+c(NH3·H2O)
D. N点对应的溶液中:c(NH4+)+c(NH3·H2O)=2c(SO42-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com