

分析 Ⅰ.图1中,左边装置是原电池,较活泼的金属锌作负极,较不活泼的金属铜作正极,如果要找电极材料代替铜,所找材料必须是不如锌活泼的金属或导电的非金属,M是阳极,N是阴极,电解池中阴极上阳离子得电子发生还原反应,原电池放电时,阴离子向负极移动;
(1)在保证电极反应不变的情况下,仍然是锌作负极,则正极材料必须是不如锌活泼的金属或导电的非金属;
(2)N电极是电解池的阴极氢离子得到电子生成氢气;
Ⅱ.该电解池中,阳极材料是活泼金属,则电解池工作时,阳极上铁失电子发生氧化反应,同时氢氧根离子失电子生成氧气,阴极上氢离子得电子发生还原反应,根据阴阳极上转移电子数相等计算铁反应的质量,在碱性锌电池中,正极上得电子发生还原反应;
(3)铁是活泼金属,电解池工作时,阳极上铁失电子发生氧化反应,氢氧根离子失电子发生氧化反应;
(4)根据阴阳极上转移电子数相等计算铁反应的质量.
解答 解:I.(1)在保证电极反应不变的情况下,仍然是锌作负极,则正极材料必须是不如锌活泼的金属或导电的非金属,铝是比锌活泼的金属,所以不能代替铜;
故答案为:A;
(2)N电极连接原电池负极,所以是电解池阴极,阴极上氢离子得电子发生还原反应,电极反应式为:2H++2e-═H2↑,
故答案为:2H++2e-═H2↑;
II.(3)铁是活泼金属,电解池工作时,阳极上铁失电子发生氧化反应,氢氧根离子失电子发生氧化反应,所以发生的电极反应式为:Fe-6e-+8OH-═FeO42-+4H2O和4OH--4e-═2H2O+O2↑,
故答案为:4OH--4e-═2H2O+O2↑;
(4)X电极上析出的是氢气,Y电极上析出的是氧气,且Y电极失电子进入溶液,
设铁质量减少为xg,
根据转移电子数相等得$\frac{0.672L}{22.4L/mol}$×2=$\frac{0.168L}{22.4L}$×4×$\frac{xg}{56g/mol}×6$,x=0.28;
故答案为:0.28g.
点评 本题考查了原电池和电解池原理,注意:电解池中如果活泼金属作阳极,则电解池工作时阳极材料失电子发生氧化反应,为易错点,注意电子守恒在计算中的应用,题目难度中等.


科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 氯酸钾和亚硫酸氢钾溶液能发生氧化还原反应:ClO3-+3HSO3-═3SO42-+Cl-+3H+.已知该反应的速率随c(H+)的增大而加快.下列为用ClO3-在单位时间内物质的量浓度变化表示的该反应v-t图.下列说法中不正确的是( )
氯酸钾和亚硫酸氢钾溶液能发生氧化还原反应:ClO3-+3HSO3-═3SO42-+Cl-+3H+.已知该反应的速率随c(H+)的增大而加快.下列为用ClO3-在单位时间内物质的量浓度变化表示的该反应v-t图.下列说法中不正确的是( )| A. | 反应开始时速率增大可能是c(H+)所致 | |
| B. | 纵坐标为v(Cl-)的v-t曲线与图中曲线完全重合 | |
| C. | 图中阴影部分的面积表示t1-t2时间内ClO3-的物质的量的减少量 | |
| D. | 后期反应速率下降的主要原因是反应物浓度减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

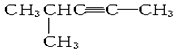 分子式为C5H8,名称是4-甲基-1-戊炔,
分子式为C5H8,名称是4-甲基-1-戊炔,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阴离子的半径按X、Y、Z的顺序增大 | |
| B. | 元素非金属性按X、Y、Z的顺序增强 | |
| C. | 气态氢化物的稳定性按X、Y、Z的顺序增强 | |
| D. | 单质的氧化性按X、Y、Z的顺序增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ④⑥⑦ | C. | ①④⑥⑦ | D. | ①⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向水中加入稀氨水,水的电离平衡逆向移动,c(OH-)降低 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 | |
| C. | 向水中加入少量CH3COOH,水的电离平衡逆向移动,c(H+)降低 | |
| D. | 将水加热,Kw增大,pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18 g H2O中含有2 mol氢 | |
| B. | 阿伏加德罗常数是指0.012 kg碳所含有的碳原子数,其数值约等于6.02×1023 | |
| C. | 铁的摩尔质量及其相对原子质量均为56 g•mol-1 | |
| D. | 常温常压下,44 g CO2气体与46 g N2O4气体具有相同数目的氧原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com