
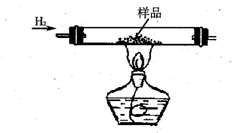
 实验室有CuO和铜粉的混合物.要测定该样品(已称得其质量为m g)中氧化铜的质量分数.
实验室有CuO和铜粉的混合物.要测定该样品(已称得其质量为m g)中氧化铜的质量分数.| 实验方法 | 有关化学方程式 | 实验用仪器(填序号) | 实验需直接测定的物理量(用文字说明) |
| (1) | H2SO4+CuO═CuSO4+H2O | ||
| (2) | 实验前坩埚与样品总质量(或坩埚质量)、实验后坩埚与CuO总质量 |
| ||
| 80 |
| x |
| 16 |
| m-n |
| 5(m-n) |
| m |
| 5(m-n) |
| m |
| 方法(1) | ①②③⑤ | 过滤后剩余固体的质量 | |||||
| 方法(2) | 2Cu+O2
|
①②④⑥⑦⑧ |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
实验方法 | 实验过程中反应的化学方程式 | 实验所选用仪器的编号 | 实验需直接测定的有关物理量(用文字说明) |
1 |
|
|
|
2 |
|
|
|
实验可能用到的主要仪器:①托盘天平 ②启普发生器 ③硬质玻璃管 ④泥三角 ⑤烧杯⑥坩埚 ⑦酒精灯 ⑧玻璃棒 ⑨漏斗 ⑩干燥管
实验可能用到的试剂:a.锌粒 b.稀硫酸 c.氯化钠溶液 d.浓硫酸
查看答案和解析>>
科目:高中化学 来源:2012-2013学年重庆市重庆一中高一10月月考化学试卷(带解析) 题型:实验题
(10分)实验室有CuO和铜粉的混合物。要测定该样品(已称得其质量为m g)中氧化铜的质量分数。用下图所示仪器装置制取H2,再用H2还原CuO,最后根据样品质量的减少和无水CaCl2质量的增加来测定样品中氧化铜的质量分数。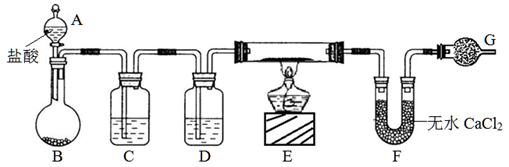
请回答:
(1)仪器中装入的试剂:D 。
(2)操作“①打开A的活塞”和“②点燃E处酒精灯”应该先进行的是 (填序号),在这两步操作之间还应进行的操作是: 。
(3)若实验中有部分CuO被还原为红色的Cu2O,对实验的影响为_____(偏大、偏小、无影响)。
(4)若测得的原质量为a g的硬质玻璃管(E),反应后质量变为b g;U型管实验后质量增加n g,由以上数据可以列出计算氧化铜质量分数的两个不同计算式:
计算式1: ;计算式2: 。
查看答案和解析>>
科目:高中化学 来源:2015届重庆市高一10月月考化学试卷(解析版) 题型:实验题
(10分)实验室有CuO和铜粉的混合物。要测定该样品(已称得其质量为m g)中氧化铜的质量分数。用下图所示仪器装置制取H2,再用H2还原CuO,最后根据样品质量的减少和无水CaCl2质量的增加来测定样品中氧化铜的质量分数。
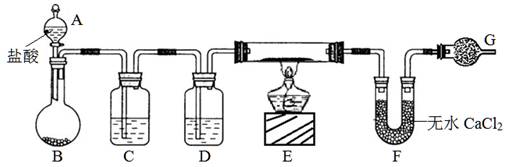
请回答:
(1)仪器中装入的试剂:D 。
(2)操作“①打开A的活塞”和“②点燃E处酒精灯”应该先进行的是 (填序号),在这两步操作之间还应进行的操作是: 。
(3)若实验中有部分CuO被还原为红色的Cu2O,对实验的影响为_____(偏大、偏小、无影响)。
(4)若测得的原质量为a g的硬质玻璃管(E),反应后质量变为b g;U型管实验后质量增加n g,由以上数据可以列出计算氧化铜质量分数的两个不同计算式:
计算式1: ;计算式2: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室可以通过三条途径来制取N2:
①加热条件下用NH3还原CuO制得纯净的N2和铜粉,反应的化学方程式为:
![]()
② 将空气通过灼热的铜粉制得的N2
③ 加热NaNO2(有毒性)与NH4Cl的混合浓溶液制取N2,反应的化学方程式为:
![]()
按上述途径制N2可供选择的实验仪器如下图所示,其他必要的仪器如铁架台、铁夹、铁圈、石棉网、酒精灯等未列出。
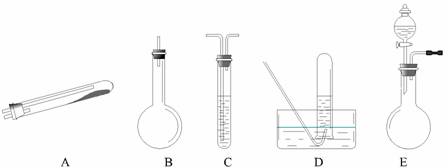
(1)按途径 ① 制取N2时所需的氨气要用浓氨水与生石灰反应得到,化学方程式为:
CaO+NH3?H2O === Ca(OH)2+NH3↑,,最好要用上述装置中的 。 (填字母,下同)作为氨气发生装置。要制取并收集N2,还应使用到上述装置中的
(2)①和②两种途径常常被联合使用。这种方法与途径③相比其优越性在于 。
(3)检查E装置气密性的方法是 。利用E装置还可以制取的气体有 (只需写出三种)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com