
Q、R、X、Y、Z为周期表中原子序数依次递增的前四周期元素。
已知:①Q为元素周期表中原子半径最小的元素;②R的基态原子中电子占据三种能量不同的能级,且每种能级中的电子总数相同;③Y的基态原子的核外成对的电子数是未成对的电子数的3倍;④Z基态原子有六个未成对电子。用对应的元素符号或化学式回答下列问题:
(1)R、X、Y的第一电离能由大到小的顺序为 。
(2)Q元素在元素周期表中属于 区,与Y元素同族的第四周期元素的价电子排布式为 。
(3)RY2的电子式为 ,Z3+的原子结构示意图为____________。
(4)RQ2Y2的结构式为 ,m g该物质完全燃烧后通过足量Na2O2固体吸收,Na2O2固体增重的质量为 g。
(5)由Y、Z两种元素组成的Z2Y72-离子在酸性条件下可与乙醇反应,生成乙酸、Z3+等物质。该反应的离子方程式为__________________________________________。
科目:高中化学 来源: 题型:
A、B、C、D、E五种元素,它们原子的核电荷数依次递增且均小于18。A元素原子核外只有1个电子;C是地壳中含量最多的元素;B、C可形成两种化合物BC和BC2,B的最高正价与最低负价绝对值相等,BC有毒,BC2可用于灭火;D元素的最外层电子数是其电子层数的三分之一;E—具有与Ar原子相同的电子层结构。
(1)写出A、C两种元素的符号:A , C 。
(2)写出D原子和E—离子的结构示意图:D原子 ,E—离子 。
(3)由A、B、C、D四种元素组成的常见化合物的化学式为 ,
其电离方程式为 。
(4)写出A、C、D三种元素组成的常见化合物的稀溶液,常温下和E的单质反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料。
(1)在25 ℃、101 kPa时,8 g CH4完全燃烧生成液态水时放出的热量是445.15 kJ,
则CH4燃烧的热化学方程式是 。
(2)已知:C(s) + O2(g)  CO2(g) ΔH=-437.3 kJ•mol-1
CO2(g) ΔH=-437.3 kJ•mol-1
H2(g) + 1/2 O2(g)  H2O(g) ΔH=-285.8 kJ•mol-1
H2O(g) ΔH=-285.8 kJ•mol-1
CO(g) + 1/2 O2(g)  CO2(g) ΔH=-283.0 kJ•mol-1
CO2(g) ΔH=-283.0 kJ•mol-1
则煤的气化主要反应的热化学方程式是:C(s) + H2O(g)  CO(g) + H2(g)
CO(g) + H2(g)
ΔH= kJ•mol-1。如果该反应ΔS=+133.7 J·K-1·mol-1 该反应在常温(25 ℃)下能否自发进行?(△G=△H-T△S) (填“能”或“不能”,并写出判断依据).
(3)由气态基态原子形成1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ·mol-1 | 436 | 391 | 945 |
已知反应N2+3H2  2NH3 △H=a kJ·mol-1。试根据表中所列键能数据估算a的
2NH3 △H=a kJ·mol-1。试根据表中所列键能数据估算a的
数值为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法错误的是
A.X、Y、Z三种元素最低价氢化物的沸点依次升高
B.物质W3X4中,每个原子最外层均达到8电子稳定结构
C.X、Y和氢形成的化合物中可能既有离子键、又有共价键
D.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4
| X | Y | ||
| W | Z | ||
| T |
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。根据图中数据,下列有关说法错误的是
A.该反应的化学方程式为3X+Y===2Z
B.2 min时,反应达最大限度,但化学反应仍在进行
C.反应开始至2 min,Z的反应速率为0.05 mol·L-1·min-1
D.反应达到平衡时,压强是开始时的0.9倍

查看答案和解析>>
科目:高中化学 来源: 题型:
KNO3是重要的化工产品,下面是一种已获得专利的KNO3制备方法的主要步骤:
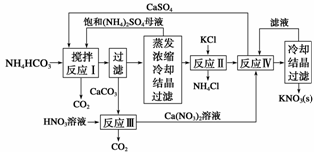
(1)反应Ⅰ中,CaSO4与NH4HCO3的物质的量之比为1∶2,该反应的化学方程式为_____
___________________________________________________________________。
(2)反应Ⅱ需在干态、加热的条件下进行,加热的目的是___________________________
___________________________________ _____________________________________;
_____________________________________;
从反应Ⅳ所得混合物中分离出CaSO4的方法是趁热过滤,趁热过滤的目的是________________________________________________________________________。
(3)检验反应Ⅱ所得K2SO4中是否混有KCl的方法是:取少量K2SO4样品溶解于 水,________________________________________________________________________。
水,________________________________________________________________________。
(4)整个流程中,可循环利用的物质除(NH4)2SO4外,还有________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
胶体区别于其他分散系的本质特征是
A.胶体的分散质能通过滤纸孔隙,而浊液的分散质不能
B.胶体能产生丁达尔现象
C.胶体分散质粒子直径在1nm~100nm之间
D.胶体在一定条件下能稳定存在
查看答案和解析>>
科目:高中化学 来源: 题型:
FeC13、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是
A.溶液中一定不含Cu2+ B.溶液中一定含Fe2+
C.加入KSCN溶液一定不变红色 D.剩余固体中可能含有Fe
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com