
| A. | “沙尘暴”属于一种自然现象,与人类活动无关 | |
| B. | 碳酸铝是一种应用很广的视频添加剂,可大量添加到馒头、面包、油条等食品中 | |
| C. | 利用垃圾发电能达到节能减排的目的 | |
| D. | 持续高温天气的出现与人类活动无关 |
分析 A.“沙尘暴”与人类过度砍伐有关;
B.食品添加剂不能大量使用,需要控制加入量;
C.能减少化石燃料的燃烧;
D.持续高温的天气与二氧化碳的过量排放有关.
解答 解:A.“沙尘暴”与人类过度砍伐有关,是与人类活动有关的,故A错误;
B.碳酸铝是一种食品添加剂,但不能大量使用,故B错误;
C.利用垃圾发电能节约能源,减少二氧化碳的排放,故C正确;
D.持续高温的天气与二氧化碳的过量排放有关,是与人类活动有关的,故D错误.
故选C.
点评 本题考查了化学与环境,主要考查了自然界的灾害是否与人类活动有关,碳酸铝的性质等知识,题目难度不大,要求学生能够用化学知识解释化学现象,试题培养了学生的分析、理解能力及灵活应用基础知识的能力.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(HCN)+c(CN-)=0.02 mol•L-1 | B. | c(Na+)>c(OH-)>c (CN-)>c(H+) | ||
| C. | c(Na+)+c(H+)=c(CN-)+c(OH-) | D. | c(HCN)>c(CN-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 应称取Na2CO3的质量 26.5(g) | 应选用容量瓶的规格 250mL(mL) | 除容量瓶外还需要的其它玻璃仪器是上图中的烧杯、胶头滴管及玻璃棒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
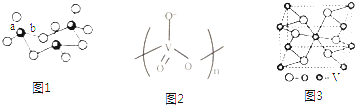
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
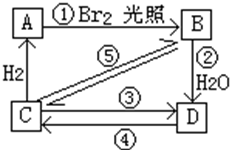 (1)下表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准).
(1)下表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准).| 烯类化合物 | 相对速率 |
| (CH3)2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
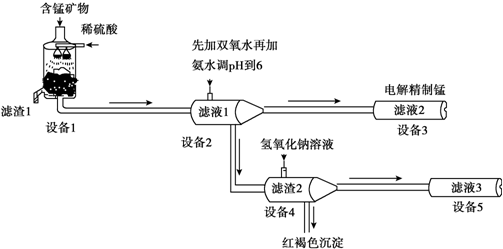
 Al(OH)3
Al(OH)3 AlO2-+H++H2O,加入NaOH溶液,H+被中和,浓度减低,Al(OH)3不断溶解.
AlO2-+H++H2O,加入NaOH溶液,H+被中和,浓度减低,Al(OH)3不断溶解.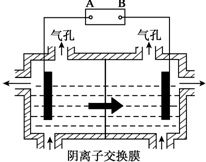
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com