


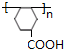 ��
��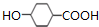 $��_{��}^{Ũ����}$
$��_{��}^{Ũ����}$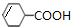 +H2O��
+H2O�� +4NaOH$��_{��}^{ˮ}$CH3CH2COONa+
+4NaOH$��_{��}^{ˮ}$CH3CH2COONa+ +2H2O+2NaCl��
+2H2O+2NaCl�� ��
������ A�ķ���ʽΪC3H8O������������������C����AΪCH3CH2CH2OH��BΪCH3CH2CHO��CΪCH3CH2COOH��
D�ķ���ʽΪC7H6O2����������������ͭ��Ӧ����E����D�к���ȩ����D��E��FeCl3��Һ���ܷ�����ɫ��Ӧ��˵�����б�������ǻ������ǵĺ˴Ź���������ʾΪ����壬�ҷ����֮��Ҳ��Ϊ1��2��2��1������֪DΪ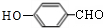 ��EΪ
��EΪ ��E���������������ӳɷ�Ӧ����FΪ
��E���������������ӳɷ�Ӧ����FΪ ��F������ȥ��Ӧ����HΪ
��F������ȥ��Ӧ����HΪ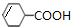 ��F�����Ӿ۷�Ӧ���ɸ߷���IΪ
��F�����Ӿ۷�Ӧ���ɸ߷���IΪ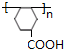 ��F�������۷�Ӧ���ɸ߷���GΪ
��F�������۷�Ӧ���ɸ߷���GΪ ����X�ķ���ʽΪC10H10O2Cl2������������ˮ����ữ�õ�C��D����ϸ������Ϣ��֪XΪ
����X�ķ���ʽΪC10H10O2Cl2������������ˮ����ữ�õ�C��D����ϸ������Ϣ��֪XΪ ��
��
��� �⣺A�ķ���ʽΪC3H8O������������������C����AΪCH3CH2CH2OH��BΪCH3CH2CHO��CΪCH3CH2COOH��
D�ķ���ʽΪC7H6O2����������������ͭ��Ӧ����E����D�к���ȩ����D��E��FeCl3��Һ���ܷ�����ɫ��Ӧ��˵�����б�������ǻ������ǵĺ˴Ź���������ʾΪ����壬�ҷ����֮��Ҳ��Ϊ1��2��2��1������֪DΪ ��EΪ
��EΪ ��E���������������ӳɷ�Ӧ����FΪ
��E���������������ӳɷ�Ӧ����FΪ ��F������ȥ��Ӧ����HΪ
��F������ȥ��Ӧ����HΪ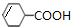 ��F�����Ӿ۷�Ӧ���ɸ߷���IΪ
��F�����Ӿ۷�Ӧ���ɸ߷���IΪ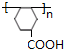 ��F�������۷�Ӧ���ɸ߷���GΪ
��F�������۷�Ӧ���ɸ߷���GΪ ����X�ķ���ʽΪC10H10O2Cl2������������ˮ����ữ�õ�C��D����ϸ������Ϣ��֪XΪ
����X�ķ���ʽΪC10H10O2Cl2������������ˮ����ữ�õ�C��D����ϸ������Ϣ��֪XΪ ��
��
��1��XΪ ��������������������AAΪCH3CH2CH2OH������Ϊ 1-������
��������������������AAΪCH3CH2CH2OH������Ϊ 1-������
�ʴ�Ϊ��������1-������
��2��I�Ľṹ��ʽΪ��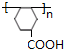 ���ʴ�Ϊ��
���ʴ�Ϊ��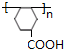 ��
��
��3��EΪ ��
��
a�����з��ǻ����Ȼ������Է���ȡ����Ӧ����a��ȷ��
b�����ܷ�����ȥ��Ӧ����b����
c�����ǻ��ױ�����������ȼ�գ����Է���������Ӧ����c��ȷ��
d�����ǻ�����̼�����Ʒ�Ӧ���Ȼ���̼�����Ʒ�Ӧ��1molE�������1mol NaHCO3��Ӧ����d����
��ѡ��bd��
��4����F��H�ķ�Ӧ����ʽΪ�� $��_{��}^{Ũ����}$
$��_{��}^{Ũ����}$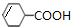 +H2O��
+H2O��
��X�� ��������ϡNaOH��Һ���ȷ�Ӧ����ʽΪ��
��������ϡNaOH��Һ���ȷ�Ӧ����ʽΪ�� +4NaOH$��_{��}^{ˮ}$CH3CH2COONa+
+4NaOH$��_{��}^{ˮ}$CH3CH2COONa+ +2H2O+2NaCl��
+2H2O+2NaCl��
�ʴ�Ϊ�� $��_{��}^{Ũ����}$
$��_{��}^{Ũ����}$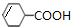 +H2O��
+H2O�� +4NaOH$��_{��}^{ˮ}$CH3CH2COONa+
+4NaOH$��_{��}^{ˮ}$CH3CH2COONa+ +2H2O+2NaCl'
+2H2O+2NaCl'
��5��ͬʱ��������������E�� ����ͬ���칹�壺
����ͬ���칹�壺
���ܷ���������Ӧ��˵������ȩ������������NaOH��Һ��Ӧ������2mol NaOH���ۺ��б���������2�����ǻ���2��-OH������λ��-CHO��2��λ�ã�2��-OH���ڼ�λ��-CHO��3��λ�ã�2��-OH���ڶ�λ��-CHO��1��λ�ã�����6�֣�����һ��Ϊ�� �ȣ�
�ȣ�
�ʴ�Ϊ��6�� ��
��
���� ���⿼���л�����ƶϣ������л������ʽ����Ӧ���������ƶϣ���Ҫѧ���������չ����ŵ�������ת�����Ƕ��л���ѧ�������ۺϿ��飮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
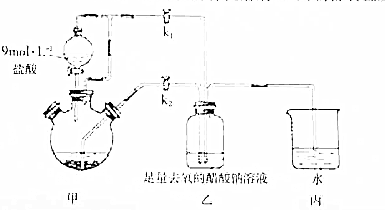 �ټ��װ�������Ժ���������ƿ�����μ������п��������CrCl3��Һ��
�ټ��װ�������Ժ���������ƿ�����μ������п��������CrCl3��Һ�� �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
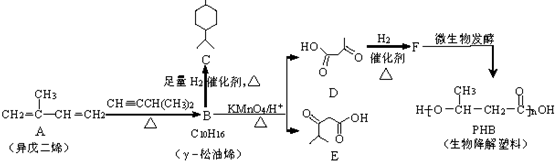
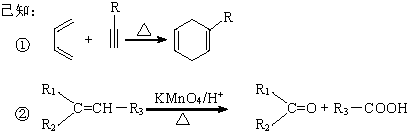
 ��D�ĺ˴Ź���������3��壮
��D�ĺ˴Ź���������3��壮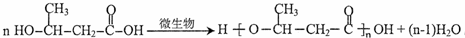 ��
�� �ĺϳ�·��ͼΪ
�ĺϳ�·��ͼΪ ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���ô�������Ӧ��SO2ת��ΪSO3�ǹ�ҵ����������Ĺؼ����裮
���ô�������Ӧ��SO2ת��ΪSO3�ǹ�ҵ����������Ĺؼ����裮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��Ȼ���д��ڴ����Ľ���Ԫ�أ������ơ�þ����������ͭ���ڹ�ũҵ���������Ź㷺��Ӧ�ã�
��Ȼ���д��ڴ����Ľ���Ԫ�أ������ơ�þ����������ͭ���ڹ�ũҵ���������Ź㷺��Ӧ�ã�| �����ܣ�KJ/mol�� | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��PX��+12MnO4-+36H+��5
��PX��+12MnO4-+36H+��5  ��PTA��+12Mn2++28H2O�������й�˵��������ǣ�������
��PTA��+12Mn2++28H2O�������й�˵��������ǣ�������| A�� | PTA �Ǹ÷�Ӧ���������� | |
| B�� | PTA ���Ҷ���ͨ�����۷�Ӧ�������� PET ���� | |
| C�� | PX ���Ӻ��б�����ͬ���칹�廹�� 3 �� | |
| D�� | �÷�Ӧ���� 1molPX����ת�� 10mol���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com