
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
分析 可与碳酸氢钠反应放出二氧化碳气体的有机化合物中一定含有羧基,根据分子式为C6H12O2且含有羧基的有机物的同分异构体的种类来回答.
解答 解:可与碳酸氢钠反应的有机化合物中一定含有羧基,分子式为C6H12O2且含有羧基的有机物可以简写为C5H11COOH,其中-C5H11有8种同分异构体:CH2CH2CH2CH2CH3、-CH(CH3)CH2CH2CH3、-CH(CH2CH3)2、-CHCH(CH3)CH2CH3、-C(CH3)2CH2CH3、-C(CH3)CH(CH3)2、-CH2CH2CH(CH3)2、-CH2C(CH3)3,所以C5H11COOH有8种同分异构体,故选D.
点评 本题主要考查涉及羧酸的化学性质以及同分异构体的书写等方面的知识,属于综合知识的考查,难度不大,掌握小于5的烃基的个数可以轻松解答,甲基与乙基1个、丙基2个、丁基4个、戊基8个.


科目:高中化学 来源: 题型:解答题
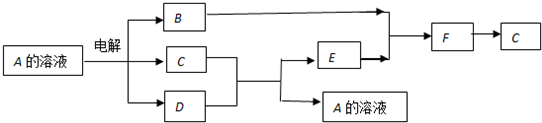
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 甲肾上腺素的分子式为:C8H10NO3 | |
| B. | 1 mol去甲肾上腺素最多能与2 mol Na发生反应 | |
| C. | 1 mol去甲肾上腺素最多能与2 mol Br2发生取代反应 | |
| D. | 去甲肾上腺素能发生加成、取代、消去和氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 名称为:2,5-二甲基-2,4-己二烯
名称为:2,5-二甲基-2,4-己二烯 名称为:2,4-二甲基-3-乙基戊烷.
名称为:2,4-二甲基-3-乙基戊烷.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
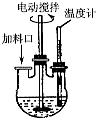 实验室制取高纯NaI晶体(无色)可按下列步骤进行:按化学计量称取各原料,在三颈烧瓶中(如图)先加入适量的高纯水,然后按Na2CO3、I2和水合肼的投料顺序分批加入.
实验室制取高纯NaI晶体(无色)可按下列步骤进行:按化学计量称取各原料,在三颈烧瓶中(如图)先加入适量的高纯水,然后按Na2CO3、I2和水合肼的投料顺序分批加入.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
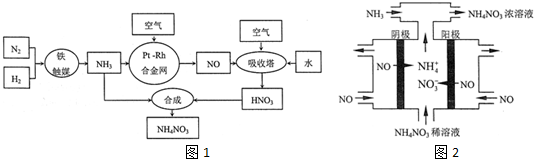
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
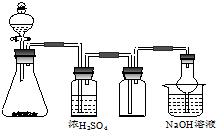 如图是一套实验室制备气体的装置,用于发生、干燥、收集和吸收有毒气体.下列各组物质能利用这套装置进行实验的是( )
如图是一套实验室制备气体的装置,用于发生、干燥、收集和吸收有毒气体.下列各组物质能利用这套装置进行实验的是( )| A. | 电石和水 | B. | 高锰酸钾和浓盐酸 | ||
| C. | Cu片和稀硝酸 | D. | FeS和稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 甲烷分子中的4个氢原子都可以被取代.若甲烷分子中的4个氢原子被苯基取代,则可得到的分子如图所示,对该分子的描述中,不正确的是( )
甲烷分子中的4个氢原子都可以被取代.若甲烷分子中的4个氢原子被苯基取代,则可得到的分子如图所示,对该分子的描述中,不正确的是( )| A. | 化学式为C25H20 | B. | 此物质属芳香烃类物质 | ||
| C. | 所有碳原子都在同一平面上 | D. | 最多有13个碳原子在同一平面上 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com