
【题目】A、B、C、D、E均为中学化学的常见单质或化合物,它们之间的反应关系如图所示:
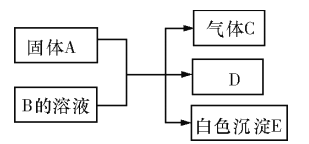
(1)若A是短周期中原子半径最大的元素构成的单质,E 既可溶于盐酸又可溶于NaOH ,E 溶于NaOH 溶液的离子方程式为___________;工业上冶炼A 的化学反应方程式为_________________。
(2)若A为红色金属,B 为某酸的浓溶液,C 为可形成酸雨的无色气体。则A 与B反应的化学方程式为___________________________。
(3)若B为某酸式盐的溶液,C 是既含有极性键又含有非极性键的四原子分子,则实验室制取C的化学方程式为 _________________;0.1molC 完全燃烧生成液态水时放热130kJ·mol-1,则表达C 燃烧热的热化学方程式是_______________。
【答案】 Al(OH)3+OH-==AlO-2+2H2O 2NaCl(熔融)![]() 2Na+Cl2↑ Cu+2H2SO4(浓)
2Na+Cl2↑ Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O CaC2+2H2O→C2H2↑+Ca(OH)2 C2H2(g)+
CuSO4+SO2↑+2H2O CaC2+2H2O→C2H2↑+Ca(OH)2 C2H2(g)+![]() O2(g)→2CO2(g)+H2O(l) △H=-1300kJ·mol-1
O2(g)→2CO2(g)+H2O(l) △H=-1300kJ·mol-1
【解析】(1)A是短周期中原子半径最大的元素构成的单质,应为Na,E既可溶于盐酸又可溶于NaOH溶液,应为Al(OH)3,Al(OH)3与NaOH溶液反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,工业冶炼Na用电解熔融的NaCl的方法,反应的化学方程式为2NaCl(熔融)![]() 2Na+Cl2↑,故答案为:Al(OH)3+OH-=AlO2-+2H2O;2NaCl(熔融)
2Na+Cl2↑,故答案为:Al(OH)3+OH-=AlO2-+2H2O;2NaCl(熔融)![]() 2Na+Cl2↑;
2Na+Cl2↑;
(2)若A为红色金属,B 为某酸的浓溶液,C 为可形成酸雨的无色气体。则A为铜,C为二氧化硫,铜与浓硫酸反应的化学方程式为Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,故答案为:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
(3)既含有极性键又含有非极性键的四原子分子有C2H2或H2O2,其中能燃烧的是C2H2,则A为CaC2,与水反应生成C2H2和Ca(OH)2,与B的溶液反应生成C2H2、水和碳酸钙,则B为Ca(HCO3)2,1molC2H2完全燃烧生成液态水时放热1300kJ,则2molC2H2完全燃烧放出2600kJ的热量,所以完全燃烧的热化学方程式为2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-2600kJmol-1,因此燃烧热的热化学方程式为C2H2(g)+ ![]() O2(g)→2CO2(g)+H2O(l) △H=-1300kJ·mol-1,故答案为:C2H2(g)+
O2(g)→2CO2(g)+H2O(l) △H=-1300kJ·mol-1,故答案为:C2H2(g)+ ![]() O2(g)→2CO2(g)+H2O(l) △H=-1300kJ·mol-1。
O2(g)→2CO2(g)+H2O(l) △H=-1300kJ·mol-1。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 根据反应Cu+H2SO4![]() CuSO4+H2↑可推知Cu的还原性比H2的强
CuSO4+H2↑可推知Cu的还原性比H2的强
B. 在反应CaH2+2H2O===Ca(OH)2+2H2↑中,水作氧化剂
C. 反应3NO2+H2O===2HNO3+NO中氧化剂和还原剂的物质的量之比是3∶1
D. Cl2的氧化性强于I2的氧化性,故置换反应I2+2NaClO3===2NaIO3+Cl2不能发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某容器中发生一个化学反应,反应过程中存在H2O、ClO-、CN-、HCO![]() 、N2、Cl-六种粒子反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示。下列有关判断中正确的是
、N2、Cl-六种粒子反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示。下列有关判断中正确的是

A. 还原剂是CN-,氧化产物只有N2
B. 氧化剂是ClO-,还原产物是HCO![]()
C. 配平后氧化剂与还原剂的计量数之比为5∶2
D. 标准状况下若生成2.24 L N2,则转移电子0.5 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。

(1)制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为:
___________________________________________________________。
(2)装置B中饱和食盐水的作用是_______________;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象___________________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入_______。
a | b | c | d | |
I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
II | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
III | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。当向D中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为______色,说明氯的非金属性大于溴。
(5)打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是_____________。
(6)有人提出,装置F中可改用足量的NaHSO3溶液吸收余氯,试写出相应的离子反应方程式:__________________,判断改用NaHSO3溶液是否可行______(填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)18.6gNa2X含有0.6molNa+,则X的相对原子质量为___________,该物质的化学式__________。
(2)2molCO(NH2)2中含_____mol碳原子,_____mol氧原子,_____mol氮原子,____mol氢原子,所含氧原子数跟_____molH2O中所含氧原子数相等。
(3)已知 1.204×1023 个 X 气体分子的质量为 8g,则 X 气体的摩尔质量是__________。
(4)同温同压下,同体积的N2和SO2分子数之比为__________________,物质的量之比为____________,原子总数之比为____________,摩尔质量之比为__________,质量之比为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物X的结构简式如图所示,下列有关说法不正确的是

A. X分子中含有三种官能团
B. 可用酸性高锰酸钾溶液区别苯和X
C. X在一定条件下能发生加成、加聚、取代、氧化等反应
D. 在催化剂的作用下,1 mol X最多能与5 mol H2加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 在配制一定物质的量浓度溶液的实验中量筒是必需仪器
B. 实验室中,盛装NaOH 溶液的试剂瓶用橡皮塞
C. 某未知液中加稀NaOH溶液,没有产生使湿润的红色石蕊试纸变蓝的气体,则该未知液中不含NH4+
D. 用pH试纸测定某溶液的pH时,需预先用蒸馏水湿润pH 试纸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于浓硫酸和浓硝酸的说法正确的是( )
A. 浓硫酸和浓硝酸都能用来直接跟锌粒反应制氢气
B. 浓硫酸和浓硝酸加水稀释后都能与金属铜反应
C. 浓硫酸和浓硝酸都能与单质碳反应
D. 浓硫酸和浓硝酸在高温下都能用金属铝制容器盛放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A. 把金属铁放入稀硫酸中:2Fe + 6H+===2Fe3++ 3H2↑
B. 石灰石跟醋酸反应:CaCO3 + 2H+===Ca2+ + H2O + CO2↑
C. 氢氧化钡跟硫酸溶液反应:Ba2++ SO![]() + H+ + OH-===BaSO4↓+H2O
+ H+ + OH-===BaSO4↓+H2O
D. Cu(OH)2与硝酸反应:Cu(OH)2 + 2H+ = Cu2+ + 2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com