
”¾ĢāÄæ”æ2015Äź10ŌĀ£¬ĶĄÓ“Ó“»ńµĆŵ±“¶ūÉśĄķѧ»ņŅ½Ń§½±£¬ĄķÓÉŹĒĖż·¢ĻÖĮĖĒąŻļĖŲ£¬ÕāÖÖŅ©Ę·æÉŅŌÓŠŠ§½µµĶű¼²»¼ÕßµÄĖĄĶöĀŹ£¬Ėż³ÉĪŖŹ×»ńæĘѧĄąÅµ±“¶ū½±µÄÖŠ¹śČĖ”£ĒąŻļĖŲĮ½²½æÉŗĻ³ÉµĆµ½ÖĪĮĘű¼²µÄŅ©ĪļĒąŻļēśõ„”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ( )
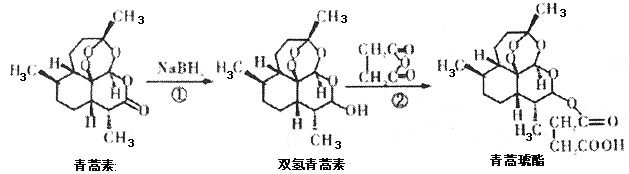
A£®ĒąŻļĖŲ·Ö×ÓŹ½ĪŖC15H24O5
B£®·“Ó¦¢ŚŌ×ÓĄūÓĆĀŹĪŖ100%
C£®øĆ¹ż³ĢÖŠĒąŻļĖŲÉś³ÉĖ«ĒāĒąŻļĖŲŹōÓŚŃõ»Æ·“Ó¦
D£®1 molĒąŻļēśõ„ÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦£¬×ī¶ąĻūŗÄ1 molĒāŃõ»ÆÄĘ
”¾“š°ø”æB
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗA£®øł¾Ż½į¹¹¼ņŹ½ÖŖ£¬Ęä·Ö×ÓŹ½ĪŖC15H22O5£¬¹ŹA“ķĪó£»B£®·“Ó¦¢ŚĪŖ¼Ó³É·“Ó¦£¬Ō×ÓĄūÓĆĀŹĪŖ100%£¬¹ŹBÕżČ·£»C£®øł¾Ż½į¹¹æÉÖŖ£¬ĒąŻļĖŲÉś³ÉĖ«ĒāĒąŻļĖŲ¹ż³ĢÖŠĢ¼ŃõĖ«¼ü¼ÓĒā±»»¹Ō£¬ŹōÓŚ»¹Ō·“Ó¦£¬¹ŹC“ķĪó£»D£®ĒąŻļēśõ„ÖŠŗ¬ÓŠōČ»łŗĶõ„»ł£¬¶¼ÄÜÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦£¬×ī¶ąĻūŗÄ2 molĒāŃõ»ÆÄĘ£¬¹ŹD“ķĪó£»¹ŹŃ”B”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŅĻĀ±ķĪŖŌŖĖŲÖÜĘŚ±ķµÄŅ»²æ·Ö”£X”¢Y”¢Z”¢WĪŖ¶ĢÖÜĘŚŌŖĖŲ£¬ĘäÖŠXŌŖĖŲµÄŌ×Ó×īĶā²ćµē×ÓŹżŹĒĘäÄŚ²ćµē×ÓŹżµÄ2±¶”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ()

A. øł¾ŻŌŖĖŲÖÜĘŚĀÉ£¬æÉŅŌĶĘ²ā“ęŌŚT3Y4”¢TZ2ŗĶTW4
B. XĒā»ÆĪļµÄ·ŠµćŅ»¶Ø±ČYĒā»ÆĪļµÄ·Šµćøß
C. XZ2”¢XW4ÓėYW3¶¼ŹĒ·Ē¼«ŠŌ·Ö×Ó
D. WµÄŃõ»ÆĪļµÄĖ®»ÆĪļĖįŠŌŅ»¶Ø±ČZµÄĒæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧæĪĶāŠ”×éÓĆÓŅĶ¼×°ÖĆÖĘČ”äå±½”£ĻČĻņ·ÖŅŗĀ©¶·ÖŠ¼ÓČė±½ŗĶŅŗä壬ŌŁ½«»ģŗĻŅŗĀżĀżµĪČė·“Ó¦Ę÷A(AĻĀ¶Ė»īČū¹Ų±Õ)ÖŠ”£
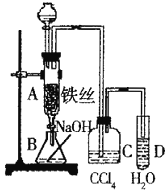
£Ø1£©Š“³öAÖŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½______________________________£»
£Ø2£©¹Ū²ģµ½DÖŠµÄĻÖĻóŹĒ______________________________£»
£Ø3£©ŹµŃé½įŹųŹ±£¬“ņæŖAĻĀ¶ĖµÄ»īČū£¬ČĆ·“Ó¦ŅŗĮ÷ČėBÖŠ£¬³ä·ÖÕńµ“£¬ÄæµÄŹĒ_______________£»
£Ø4£©CÖŠŹ¢·ÅCCl4µÄ×÷ÓĆŹĒ______________________________”£
£Ø5£©ÄÜÖ¤Ć÷±½ŗĶŅŗäå·¢ÉśµÄŹĒČ”“ś·“Ó¦£¬¶ų²»ŹĒ¼Ó³É·“Ó¦£¬æÉĻņŹŌ¹ÜDÖŠĻČ¼ÓČė_________£¬ŌŁ¼ÓČėAgNO3ČÜŅŗ£¬Čō²śÉśµ»ĘÉ«³Įµķ£¬ŌņÄÜÖ¤Ć÷”£ĮķŅ»ÖÖŃéÖ¤µÄ·½·ØŹĒĻņŹŌ¹ÜDÖŠ¼ÓČė__________£¬ĻÖĻóŹĒ_____________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ2SO2(g)+O2(g) ![]() 2SO3(g)ŹĒÖʱøĮņĖįµÄÖŲŅŖ·“Ó¦”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
2SO3(g)ŹĒÖʱøĮņĖįµÄÖŲŅŖ·“Ó¦”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A£®“߻ƼĮV2O5²»øıäøĆ·“Ó¦µÄÄę·“Ó¦ĖŁĀŹ
B£®ŗćŃ¹£¬ĶØČėĻ”ÓŠĘųĢ壬·“Ó¦ĖŁĀŹ²»±ä
C£®øĆ·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬½µµĶĪĀ¶Č½«Ėõ¶Ģ·“Ó¦“ļµ½Ę½ŗāµÄŹ±¼ä
D£®ŌŚt1”¢t2Ź±æĢ£¬SO3£Øg£©µÄÅØ¶Č·Ö±šŹĒC1mol/L£¬C2 mol/L£¬ŌņŹ±¼ä¼äøōt1£Øs£©”«t2(s)ÄŚ£¬SO3£Øg£©ĻūŗĵÄĘ½¾łĖŁĀŹĪŖ V=(C2-C1)/(t2-t1) mol/(L”¤s)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”放»Æѧ”ŖŃ”ŠŽ2£ŗ»ÆѧÓė¼¼Źõ”æ·ŪĆŗ»ŅŹĒČ¼Ćŗµē³§ÅųöµÄÖ÷ŅŖ¹ĢĢå·ĻĪļ”£ĪŅ¹ś»šµē³§·ŪĆŗ»ŅµÄÖ÷ŅŖŃõ»ÆĪļ×é³ÉĪŖ£ŗSiO2”¢Al2O3”¢CaOµČ”£Ņ»ÖÖĄūÓĆ·ŪĆŗ»ŅÖĘČ”Ńõ»ÆĀĮµÄ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ
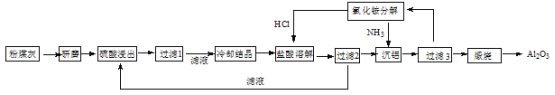
£Ø1£©·ŪĆŗ»ŅŃŠÄ„µÄÄæµÄŹĒ ”£
£Ø2£©µŚ1“Ī¹żĀĖĀĖŌüµÄÖ÷ŅŖ³É·ÖÓŠ ŗĶ £ØĢī»ÆѧŹ½, ĻĀĶ¬£©,µŚ3“Ī¹żĀĖŹ±£¬ĀĖŌüµÄ³É·ÖµÄŹĒ ”£
£Ø3£©ŌŚ104”ęÓĆĮņĖį½žČ”Ź±£¬ĀĮµÄ½žČ”ĀŹÓėŹ±¼äµÄ¹ŲĻµČēĻĀĶ¼1£¬ŹŹŅĖµÄ½žČ”Ź±¼äĪŖ h£»ĀĮµÄ½žČ”ĀŹÓė”°ÖśČܼĮ/·ŪĆŗ»Ņ”±µÄ¹ŲĻµČēĶ¼2ĖłŹ¾£¬“Ó½žČ”ĀŹ½Ē¶Čæ¼ĀĒ£¬ČżÖÖÖśČܼĮNH4F”¢KF¼°ĘäNH4FÓėKFµÄ»ģŗĻĪļ£¬ŌŚÖśČܼĮ/·ŪĆŗ»ŅĻąĶ¬Ź±£¬½žČ”ĀŹ×īøߵďĒ £ØĢī»ÆѧŹ½£©£»ÓĆŗ¬·śµÄ»ÆŗĻĪļ×÷ÕāÖÖÖśČܼĮȱµćŹĒ £Ø¾ŁŅ»Ąż£©”£
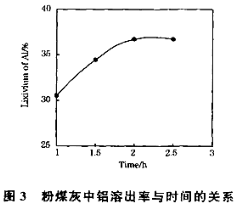
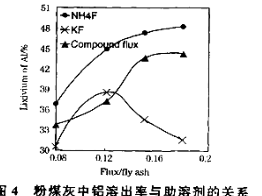
£Ø4£©Į÷³ĢÖŠŃ»·Ź¹ÓƵÄĪļÖŹÓŠ ŗĶ £ØĢī»ÆѧŹ½£©”£
£Ø5£©ÓĆŃĪĖįČܽāĮņĖįĀĮ¾§Ģ壬Äܹ»·¢ÉśµÄŌŅņŹĒ ”£
£Ø6£©ÓĆ·ŪĆŗ»ŅÖĘČ”ŗ¬ĀĮ»ÆŗĻĪļµÄÖ÷ŅŖŅāŅåŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ±ź×¼×“æöĻĀ£¬½«224L HClĘųĢåČÜÓŚ635mLĖ®ÖŠ£¬ĖłµĆŃĪĖįµÄĆܶČĪŖ1.18gcm-3£®ŹŌ¼ĘĖć£ŗ
£Ø1£©ĖłµĆŃĪĖįµÄĪļÖŹµÄĮæÅØ¶ČŹĒ_________£»
£Ø2£©Č”³öÕāÖÖŃĪĖį10mL£¬Ļ”ŹĶÖĮ118mL£¬ĖłµĆĻ”ŃĪĖįµÄĪļÖŹµÄĮæÅØ¶ČŹĒ_________”£ČōÓĆĮæĶ²Č”10mLŃĪĖįŹ±ŃöŹÓ£¬ĘäĖū²Ł×÷¾łÕżČ·£¬ŌņĻ”ŃĪĖįÅضČ_________(Ģī”°Ę«“ó”±”¢ ”°²»±ä”±»ņ”°Ę«Š””±)”£
£Ø3£©ŌŚ40.0mL 0.065molL-1 Na2CO3ČÜŅŗÖŠ£¬Öš½„¼ÓČė£Ø2£©ĖłĻ”ŹĶµÄĻ”ŃĪĖį£¬±ß¼Ó±ßÕńµ“”£ČōŹ¹·“Ó¦²»²śÉśCO2ĘųĢ壬¼ÓČėĻ”ŃĪĖįµÄĢå»ż×ī¶ą²»³¬¹ż_________ mL£æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æA£¬B£¬C£¬D£¬E“ś±ķ5ÖÖŌŖĖŲ”£Ēė°“ŅŖĒóĢīæÕ£ŗ
£Ø1£©AŌŖĖŲ»łĢ¬Ō×ÓµÄ×īĶā²ćÓŠ3øöĪ“³É¶Ōµē×Ó£¬“ĪĶā²ćÓŠ2øöµē×Ó£¬ĘäŌŖĖŲ·ūŗÅĪŖ__________£»Ęä¼Ū²ćµē×ÓÅŲ¼Ķ¼ĪŖ________”£
£Ø2£©BŌŖĖŲµÄøŗŅ»¼ŪĄė×ÓŗĶCŌŖĖŲµÄÕżŅ»¼ŪĄė×ӵĵē×Ó²ć½į¹¹¶¼Óėė²ĻąĶ¬£¬BµÄŌŖĖŲŌ×ÓµÄĆū³ĘĪŖ________£¬CĄė×ӵĽį¹¹Ź¾ŅāĶ¼ĪŖ____________________________”£
£Ø3£©DŌŖĖŲµÄÕżČż¼ŪĄė×ÓµÄ3dÄܼ¶ĪŖ°ė³äĀś£¬DµÄŌŖĖŲ·ūŗÅĪŖ________£¬Ę仳Ģ¬Ō×ӵĵē×ÓÅŲ¼Ź½ĪŖ____________________£¬ĘäŌ×ӵĽį¹¹Ź¾ŅāĶ¼ĪŖ______________”£
£Ø4£©EŌŖĖŲ»łĢ¬Ō×ÓµÄM²ćČ«³äĀś£¬N²ćƻӊ³É¶Ōµē×Ó£¬Ö»ÓŠŅ»øöĪ“³É¶Ōµē×Ó£¬EµÄŌŖĖŲ·ūŗÅĪŖ________£¬Ę仳Ģ¬Ō×Ó¼Ū²ćµē×ÓÅŲ¼Ź½ĪŖ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀ±ķŹĒŌŖĖŲÖÜĘŚ±ķµÄŅ»²æ·Ö£¬Ēė²ĪÕÕŌŖĖŲ
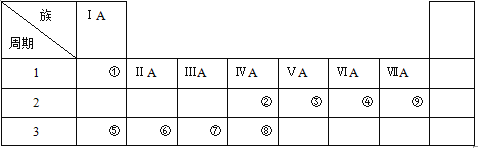
£Ø1£©¢Ł”«¢įÖŠ½šŹōŠŌ×īĒæµÄŌŖĖŲŹĒ£ØĢīŌŖĖŲ·ūŗÅ£© £¬·Ē½šŹōŠŌ×īĒæµÄŌŖĖŲŹĒ£ØĢīŌŖĖŲ·ūŗÅ£© ”£
£Ø2£©¢Ü”¢¢Ż”¢¢ßµÄŌ×Ó°ė¾¶Óɓ󵽊”µÄĖ³ŠņĪŖ£ØĢīŌŖĖŲ·ūŗÅ£© ”£
£Ø3£©¢Ś”¢¢ŪµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄĖįŠŌĒæČõĖ³ŠņĪŖ£ØĢī»ÆѧŹ½£© ”£
£Ø4£©ÓÉ¢Ł”¢¢ÜŌŖĖŲ°“Ō×ÓøöŹż±Č2£ŗ1×é³ÉµÄ»ÆŗĻĪļµÄµē×ÓŹ½ĪŖ ”£
£Ø5£©ÓÉ¢ŚŗĶ¢Ü×é³ÉµÄ»ÆŗĻĪļÓė¢Žµ„ÖŹ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ ”£
£Ø6£©¢ßµ„ÖŹÓė¢ŻµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¢ń£®øł¾Ż·“Ó¦Fe+H2SO4=FeSO4+ H2”ü »Ų“šĻĀĮŠĪŹĢā”£
£Ø1£©ŌŚ“Ė·“Ó¦ÖŠ£¬×Ō·“Ó¦æŖŹ¼ÖĮ2·ÖÖÓÄ©£¬H2SO4ÅضČÓÉ1mol/L±äĪŖ0.4mol/L£¬ŌņH2SO4µÄ·“Ó¦ĖŁĀŹĪŖ ”£ČōŅŖŹ¹øĆ·“Ó¦µÄ·“Ó¦ĖŁĀŹ¼Óæģ£¬ĻĀĮŠ“ėŹ©²»æÉŠŠµÄŹĒ £ØĢī×ÖÄø£©
a”¢øÄĢśĘ¬ĪŖĢś·Ū b”¢øÄĻ”H2SO4ĪŖ98%µÄÅØH2SO4
c”¢ÉżøßĪĀ¶Č d”¢µĪ¼ÓÉŁĮæCuSO4ČÜŅŗ
£Ø2£©ŌŚ“šĢāæصÄ×ų±źĶ¼ÖŠ£¬»³ö“Ė·“Ó¦¹ż³ĢÖŠĢåĻµµÄÄÜĮæ±ä»ÆĶ¼£Ø½ųŠŠ±ŲŅŖµÄ±ź×¢£©
£Ø3£©øł¾Ż“Ė·“Ó¦Éč¼ĘŅ»øöŌµē³Ų£¬ŅŖĒó»³ö×°ÖĆĶ¼²¢½ųŠŠ±ŲŅŖµÄ±ź×¢
¢ņ£®Ä³Š£»ÆѧŠĖȤŠ”×éÉč¼ĘĮĖĶ¼Ź¾ŹµŃé×°ÖĆ£ØĶ¼ÖŠŹ”ĀŌĮĖ¼Š³ÖŅĒĘ÷£©Ą“²ā¶ØijĢśĢ¼ŗĻ½šÖŠĢśµÄÖŹĮæ·ÖŹż”£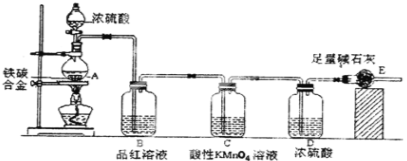
£Ø1£©½«a gĢśĢ¼ŗĻ½šŃłĘ··ÅČė×°ÖĆAÖŠ£¬ŌŁ¼ÓČė×ćĮæµÄÅØĮņĖį£¬¼ÓČČ£¬“żAÖŠ²»ŌŁŅŻ³öĘųĢåŹ±£¬Ķ£Ö¹¼ÓČČ£¬²šĻĀE²¢³ĘÖŲ£¬EŌöÖŲb g”£ĢśĢ¼ŗĻ½šÖŠĢśµÄÖŹĮæ·ÖŹżĪŖ____________(Š“±ķ“ļŹ½)”£
£Ø2£©·“Ó¦Ņ»¶ĪŹ±¼äŗ󣬓ÓAÖŠŅŻ³öĘųĢåµÄĖŁĀŹČŌČ»½Ļæģ£¬³żŅņĪĀ¶Č½Ļøߣ¬·“Ó¦·ÅČČĶā£¬»¹æÉÄܵÄŌŅņŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com