
| A. | 标准状况下,22.4L水中所含的分子数约为6.02×1023个 | |
| B. | 1 mol Cl2参加反应转移电子数一定为2 NA个 | |
| C. | 48gO3与O2的混合气体中含有的氧原子数为3NA 个 | |
| D. | 从1L0.5 mol/LNaCl溶液中取出100mL,剩余溶液中NaCl物质的量浓度为0.45mol/L |
分析 A、标况下,水为液态;
B、根据反应后氯元素的化合价可能为-1、+1、+3、+5、+7来分析;
C、氧气和臭氧中均由氧原子构成;
D、溶液是均一、稳定的.
解答 解:A、标况下,水为液态,不能根据气体摩尔体积来计算其物质的量,故A错误;
B、反应后氯元素的化合价可能为-1、+1、+3、+5、+7,还可能发生歧化反应,故1mol氯气转移的电子数不一定为2NA个,故B错误;
C、氧气和臭氧中均由氧原子构成,故48g混合物中含有的氧原子的物质的量n=$\frac{48g}{16g/mol}$=3mol,即3NA个,故C正确;
D、溶液是均一、稳定的,与所取的溶液的体积无关,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
 普伐他汀是一种调节血脂的药物,其结构如图所示(未表示出其空间构型).下列关系普伐他汀的性质描述正确的是( )
普伐他汀是一种调节血脂的药物,其结构如图所示(未表示出其空间构型).下列关系普伐他汀的性质描述正确的是( )| A. | 能与FeCl3溶液发生显色反应 | |
| B. | 1mol该物质与1molBr2发生加成反应,产物有2种 | |
| C. | 能发生加成、取代、消去反应 | |
| D. | 1mol该物质最多可与1molNaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v1=v2 | B. | v1=2v3 | C. | v3=3v2 | D. | v1=v4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 活化分子间发生的碰撞就是有效碰撞 | |
| B. | 增大反应物浓度会加快反应速率,原因是增大了活化分子百分数,从而使有效碰撞次数增加 | |
| C. | 吸热反应,升高温度,v正增大,v逆减小 | |
| D. | 有气体参与的反应达到平衡后,增大压强,平衡可能不移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
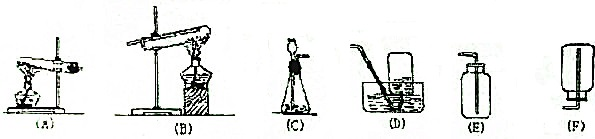
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
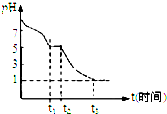
| 实验步骤(不要求写出具体操作过程) | 预期的实验现象和结论 |
| 取少量完全分解的固体产物于试管中,加入稀盐酸 | 若有淡黄色沉淀,则有Na2S2O3存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若仅加入催化剂,改变反应途径→降低反应所需要的活化能→活化分子数增多→有效碰撞次数增多→化学反应速率增大 | |
| B. | 若仅增大反应物浓度,单位体积活化分子数增多→单位体积有效碰撞次数增多→化学反应速率增大 | |
| C. | 若仅升高温度,活化分子百分数增加且分子间的碰撞频率提高→有效碰撞次数增多→化学反应速率增大 | |
| D. | 若仅加大体系压强,体积变小→活化分子百分数增加→单位体积的活化分子数目增加→有效碰撞次数增多→化学反应速率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a<b | B. | a=b | ||
| C. | 水的离子积为1.0×10-(7+a) | D. | 水的离子积为1.0×10-(b+a) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com