
纯碱(Na2CO3)在生产生活中具有广泛的用途。以下是实验室模拟制碱原理制取Na2CO3的流程图
已知:向饱和食盐水中通入NH3,CO2后发生和反应为NaCl+NH3+CO2+H2O NaHCO3↓+NH4Cl,请回答以下问题:
NaHCO3↓+NH4Cl,请回答以下问题:
(1)粗盐中含有的杂质离子有Ca2+,Mg2+,SO42-等。
精制除杂的步骤顺序a→_______→________→________→b(填字母编号)。
a.粗盐溶解,滤去沉渣.b.加入盐酸调pH;c.加入Ba(OH)2溶液;d.加入Na2CO3溶液;e.过滤
向饱和食盐水中先通入NH3,后通人CO2,理由是_____________________。
(2)灼烧固体A制Na2CO3在_____填字母序号)中进行。
a.坩埚 b.蒸发皿 c.烧杯 d.锥形瓶
证明滤液A中含有NH4+的方法是__________________________________________________________。
对滤液A进行重结晶能够获得NH4HCO3,向pH=13含Na+,K+的溶液中加入少量NH4HCO3。使pH降低,反应的离子方程式____________________________________。
(3)下图装置中常用于实验室制备CO2的是_____(填字母编号);用b示意的装置制备NH3,分液漏斗中盛放的试剂______(填试剂名称),烧瓶内可加入的固体试剂__________(填试剂名称)。
(4)一种天然碱晶体成分是aNa2CO3·bNa2CO3·cH2O,某同学利用下列提供的试剂,设计了如下简单合理测定Na2CO3的质量分数的实骏方案。(仪器自选)请把实验方案填全:供选择的试剂:1.0mol/LH2SO4溶液、1.0mol/L BaCl2溶液、稀氨水、碱石灰、Ca(OH)2溶液、蒸馏水
①称取m1g一定量天然碱晶体样品,溶于适量蒸馏水中。
②_________________________________________________________________。
③_________________________________________________________________。
④计算天然碱晶体中含Na2CO3的质量分数。
(共16分)(1)c d e(2分);NH3易溶于水,有利于吸收溶解度不大的CO2(2分)
(2) a (1分);取少量滤液A于试管中,加入足量NaOH溶液并加热,产生能使湿润的红色石蕊试纸变蓝色的气体,证明A中含有NH4+(2分);NH4++HCO3-+2OH-=NH3·H2O+CO32-+H2O (2分)
(3)b c (2分)浓氨水( 1分)、生石灰(或NaOH固体或碱石灰)( 1分)
(4) ②加入足量稀硫酸并微热,产生的气体通过足量的澄清石灰水,(1分)
③过滤、洗涤、干燥、称量沉淀;(2分)
解析试题分析:(1)Ca2+用碳酸钠除去,Mg2+用OH-除去,SO42-用Ba2+除去,最后加入盐酸酸化。但由于过量的Ba2+要用碳酸钠来除,所以碳酸钠必需放在最后加入,所以正确的操作顺序是acdeb;由于NH3易溶于水,CO2在水中的溶解度不大,所以先通入氨气有利于吸收溶解度不大的CO2。
(2)固体灼烧在坩埚中进行,因此答案选a;由于铵盐能和强碱反应生成氨气,所以可以通过检验氨气来检验NH4+,即正确的操作是取少量滤液A于试管中,加入足量NaOH溶液并加热,产生能使湿润的红色石蕊试纸变蓝色的气体,证明A中含有NH4+;由于NH4+、HCO3-和OH-均反应,从而使溶液的pH降低,反应的离子方程式是NH4++HCO3-+2OH-=NH3·H2O+CO32-+H2O。
(3)实验室制取CO2利用的是石灰石和盐酸反应,且反应不需要加热,所以装置中适合制取CO2的是选项bc;在氨水中存在平衡NH3+H2O NH3·H2O
NH3·H2O NH4++OH-,所以可以向浓氨水中加入生石灰(或NaOH固体或碱石灰)来制备氨气,即分液漏斗中盛放的是浓氨水,烧瓶内可加入的固体试剂生石灰(或NaOH固体或碱石灰)。
NH4++OH-,所以可以向浓氨水中加入生石灰(或NaOH固体或碱石灰)来制备氨气,即分液漏斗中盛放的是浓氨水,烧瓶内可加入的固体试剂生石灰(或NaOH固体或碱石灰)。
(4)由于碳酸钠能和稀硫酸反应生成CO2气体,而CO2能和澄清的石灰水反应生成碳酸钙沉淀,因此可以通过称量碳酸钙的质量来计算碳酸钠的质量,即正确的操作是②加入足量稀硫酸并微热,产生的气体通过足量的澄清石灰水;③过滤、洗涤、干燥、称量沉淀;
考点:考查粗盐的提纯;碳酸钠的制备;仪器选择;CO2和氨气的制备;NH4+检验以及物质含量测定的实验方案设计等


科目:高中化学 来源: 题型:实验题
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。为测定补血剂中铁元素的含量,某化学兴趣小组设计了两套实验方案:
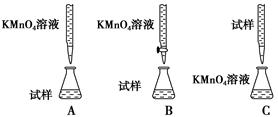
方案一 滴定法 用酸性KMnO4溶液滴定测定铁元素的含量。
反应原理:5Fe2++MnO4—+8H+===5Fe3++Mn2++4H2O
(1)实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需________(填仪器名称)。
(2)上述实验中KMnO4溶液需要酸化,用于酸化的酸是________。
| A.稀硫酸 | B.浓硝酸 | C.稀硝酸 | D.稀盐酸 |

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
硫代硫酸钠(Na2S2O3)可由下面一系列反应制得:
①Na2CO3+SO2 =Na2SO3+CO2
②Na2S+SO2+H2O=Na2SO3+H2S
③2H2S+SO2=3S↓+2H2O
④Na2SO3 + S  Na2S2O3,
Na2S2O3,
常温下溶液中析出晶体为Na2S2O3?5H2O。Na2S2O3·5H2O于40~45℃熔化,48℃分解;
Na2S2O3易溶于水,不溶于乙醇。在水中有关物质的溶解度曲线如图所示。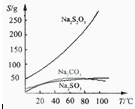
Ⅰ.现按如下方法制备Na2S2O3·5H2O:
将硫化钠和碳酸钠按反应要求比例一并放入三颈烧瓶中,注入150mL蒸馏水使其溶解,在分液漏斗中,注入浓盐酸,在装置2中加入亚硫酸钠固体,并按下图安装好装置。
请问:仪器2的名称为 ,
装置6中可放入 。
| A.BaCl2溶液 | B.浓H2SO4 |
| C.酸性KMnO4溶液 | D.NaOH溶液 |

 6I-+Cr2O72-+14H+=3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应: I2+2S2O32-=2I-+S4O62-,滴定终点的现象为 ,
6I-+Cr2O72-+14H+=3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应: I2+2S2O32-=2I-+S4O62-,滴定终点的现象为 ,查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某同学进行试验探究时,欲配制1.0molL-1Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2·8H2O试剂(化学式量:315)。在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在大量未溶物。
为探究原因,该同学查得Ba(OH)2·8H2O 部分溶解度数据,见下表:
| 温度 | 283K | 293K | 303K |
| 溶解度(g/100g H2O) | 2.5 | 3.9 | 5.6 |
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀。 | ###### |
| 步骤2:取适量滤液于试管中,滴加稀硫酸。 | _______________________ |
| 步骤3:取适量步骤1中的沉淀于试管中, ,连接带塞导气管将产生的气体导入澄清石灰水中。 | _______________________ ______________________ |
| 步骤4:取步骤1中的滤液于烧杯中,______________________________ | _______________________,说明该试剂中含有Ba(OH)2。 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
过碳酸钠和盐酸反应的化学方程式为:2Na2CO4+4HCl=4NaCl+2CO2↑+O2↑+2H2O,商品过碳酸钠中一般都含有Na2CO3,为了测定它的纯度,取一定量的样品和盐酸反应,通过测量产生的氧气的体积,可以计算出过碳酸钠的含量。
(1)根据下图提供的仪器装置,组装一套测定商品过碳酸钠的实验装置,这些装置的连接顺序是(填接口字母): 。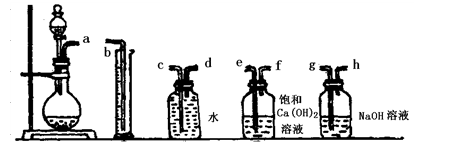
① ② ③ ④ ⑤
(2)装置④的作用是 。
(3)如果实验时,称取w g样品和过量盐酸反应后,测得氧气的体积(标准状况)为V mL,则此样品的纯度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
重铬酸钠(Na2Cr2O7?2H2O)俗称红矾钠,在工业方面有广泛用途.我国目前主要是以铬铁矿(主要成份为FeO?Cr2O3,还含有Al2O3、MgO、SiO2等杂质)为主要原料进行生产,其主要工艺流程如下: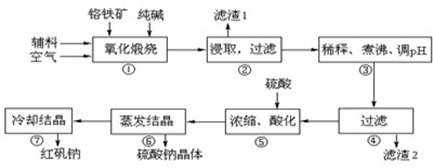
中涉及的主要反应有:
主反应:4FeO?Cr2O3+8Na2CO3+7O2  8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
副反应: SiO2+Na2CO3 Na2SiO3+CO2↑ Al2O3+Na2CO3
Na2SiO3+CO2↑ Al2O3+Na2CO3 2NaAlO2+CO2↑
2NaAlO2+CO2↑
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 |
| 完全沉淀时溶液pH | 4.7 | 3.7 | 11.2 | 5.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确的是( )
| | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 乙酸乙酯(乙酸) | CCl4 | 萃取、分液 |
| B | 乙烷(乙烯) | 酸性KMnO4溶液 | 洗气 |
| C | 溴苯(溴) | 氢氧化钠溶液 | 分液 |
| D | 苯(苯酚) | 浓溴水 | 过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
为了除去粗盐中Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作①过滤; ②加过量NaOH溶液; ③加过量盐酸; ④加过量Na2CO3溶液; ⑤加过量BaCl2溶液。其中正确的操作顺序
| A.①④②⑤③ | B.④①②⑤③ | C.②④⑤①③ | D.⑤②④①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列依据相关实验得出的结论正确的是
| A.向溶液X中滴加盐酸无明显现象,再滴加BaCl2溶液有白色沉淀,则X中含有SO42- |
| B.向NaAlO2溶液中滴入NaHCO3溶液有白色沉淀,则AlO2-结合H+能力比CO32-强 |
| C.向1 mL 1% NaOH溶液加入2 mL 2%的CuSO4溶液,振荡后滴加0.5 mL5%葡萄糖溶液,加热,未出现红色沉淀。证明葡萄糖中不含醛基 |
| D.检验某补铁药片(主要成分为亚铁化合物)是否氧化变质,使用氯水和硫氰化钾溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com