
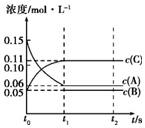
 向某体积固定的密闭容器中加入0.3mol A、0.1mol C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示.已知在反应过程中混合气体的平均相对分子质量没有变化.请回答:
向某体积固定的密闭容器中加入0.3mol A、0.1mol C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示.已知在反应过程中混合气体的平均相对分子质量没有变化.请回答:分析 (1)根据图象中A的起始浓度及物质的量求算体积;
(2)根据图象中C的浓度变化求算其反应速率;
(3)A的浓度减小为反应物,C的浓度增大为生成物,且反应前后计量数相同,根据反应物质的变化量之比等于计量数比求算;
(4)转化率=$\frac{消耗量}{起始量}$×100%;其数值之比等此时正反应速率与逆反应速率相等,于其化学计量数之比;
(5)B为生成物,根据反应的量和平衡时的量求出初始量;
(6)根据阿伏加德罗定律可知,在同温同体积条件下,气体的压强之比等于其物质的量之比,也等于其分子数之比.
解答 解:(1)由图象可知A的起始浓度为0.15mol/L,A的物质的量为0.3mol,则体积为V=$\frac{n}{c}$=$\frac{0.3mol}{0.15mol/L}$=2L;
故答案为:2;
②由图象C的浓度变化为c(C)=0.11mol/L-0.05mol/L=0.06mol/L,则其反应速率为v(C)=$\frac{△c}{△t}$=$\frac{0.06mol/L}{15s}$=0.004 mol•L-1•s-1;
故答案为:0.004mol•L-1•s-1;
③A的浓度较小为反应物,A的浓度变化为:0.15mol/L-0.06mol/L=0.09mol/L,C的浓度增大为生成物,C的浓度变化为0.11mol/L-0.05mol/L=0.06mol/L,则A、C的计量数之比为3:2,在反应过程中混合气体的平均分子量没有变化,则反应前后计量数相同,所以B为生成物,且计量数为1,所以反应方程式为:3A?B+2C;
故答案为:3A?B+2C;
(4)t1s时,A的转化率为=$\frac{0.15mol/L-0.06mol/L}{0.15mol/L}$×100%=25%,其数值之比等此时正反应速率与逆反应速率相等,于其化学计量数之比,所以v(A)正=3v(B)逆,v(A)正>v(B)逆,
故答案为:25%;>;
(5)B为生成物,B的变化量为$\frac{1}{2}$×△c(C)=$\frac{1}{2}$×0.06mol/L=0.03mol/L,B的平衡浓度为0.05mol/L,则B的起始浓度为0.05mol/L-0.03mol/=0.02mol/,则物质的量为0.02mol/L×2L=0.04mol;
故答案为:0.04mol;
(6)根据阿伏加德罗定律可知,在同温同体积条件下,气体的压强之比等于其物质的量之比,也等于其分子数之比.由于反应前后气体的分子数保持不变,所以平衡时体系内的压强保持不变,为初始状态的1倍,故答案为:1.
点评 本题考查了化学平衡状态的判断、反应速率的计算、反应方程式的确定等,题目涉及的内容较多,侧重于考查学生对所学知识的综合应用能力,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 2,2-二甲基-1-丙醇和2-甲基-1-丁醇 | |
| B. | 邻氯甲苯和对氯甲苯 | |
| C. | 2-甲基丁烷和戊烷 | |
| D. | 乙醇和乙醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
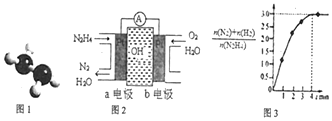
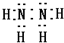 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 目的 | 分离方法 | 原理 |
| A | 分离溶于水中的碘 | 乙醇萃取 | 碘在乙醇中的溶解度较大 |
| B | 除去NH4Cl溶液中的FeCl3 | 加NaOH溶液后过滤 | Fe3+转化为Fe(OH)3沉淀 |
| C | 除去KNO3固体中混杂的NaCl | 重结晶 | NaCl在水中的溶解度很大 |
| D | 除去丁醇中的乙醚 | 蒸馏 | 丁醇与乙醚的沸点相差较大 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 700 | 900 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、蛋白质和油脂都属于高分子化合物,一定条件下都能水解 | |
| B. | 医疗上可用硫酸钡作X射线透视肠胃的内服药,是因为硫酸钡不溶于水 | |
| C. | 用过滤的方法从碘的四氯化碳溶液中获得碘 | |
| D. | 甲烷、苯、乙醇、乙酸和乙酸乙酯在一定条件下都能发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H6O | B. | C2H4O2 | C. | CH4O | D. | C4H10O? |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 难溶电解质的溶度积Ksp越小,则它的溶解度越小 | |
| B. | 任何难溶物在水中都可以存在沉淀溶解平衡,给定温度的溶解度大小都可以用Ksp计算出来 | |
| C. | 溶度积常数Ksp与温度有关,温度越高,溶度积越大 | |
| D. | 升高温度,某沉淀溶解平衡逆向移动,说明它的溶解度是减小的,Ksp也变小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com