
【题目】NH4Al(SO4)2是一种食品添加剂,用于焙烤食品;NH4HSO4在分析化学、制药工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其理由是___________________________________________________ (用必要的化学用语和相关文字说明)。
(2)相同温度下,浓度均为0.1 mol/L 的下列溶液中的c(![]() )由大到小_____(填序号)。
)由大到小_____(填序号)。
①NH4Al(SO4)2 ②CH3COONH4 ③ NH4HSO4 ④NH3·H2O ⑤NH4Cl
(3)如图1是0.1 mol/L电解质溶液的pH随温度变化的图像。其中符合0.1 mol/L NH4Al(SO4)2溶液的pH随温度变化的曲线是_____(填写字母)。
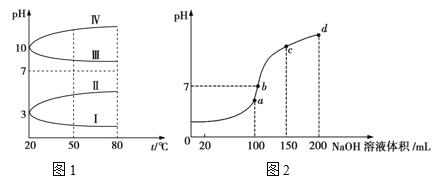
(4)室温时,向100 mL 0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L NaOH溶液,所得溶液的pH与所加NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是_____;在b点,溶液中各离子浓度由大到小的排列顺序是______;在cd段发生反应的离子方程式________________。
【答案】 Al3+水解生成的Al(OH)3胶体具有吸附性,即Al3++3H2O![]() Al(OH)3(胶体)+3H+,Al(OH)3胶体吸附悬浮颗粒使其沉降从而净化水 ③①⑤②④ Ⅰ a (Na+)>c(SO42-)>c(NH4+>c(OH-)=c(H+) NH4++OH-=NH3H2O
Al(OH)3(胶体)+3H+,Al(OH)3胶体吸附悬浮颗粒使其沉降从而净化水 ③①⑤②④ Ⅰ a (Na+)>c(SO42-)>c(NH4+>c(OH-)=c(H+) NH4++OH-=NH3H2O
【解析】(1)由于 NH4Al(SO4)2溶于水电离出的Al3+水解生成的Al(OH)3胶体具有吸附性,即Al3++3H2O![]() Al(OH)3(胶体)+3H+,Al(OH)3胶体吸附悬浮颗粒使其沉降从而净化水;(2)①NH4Al(SO4)2 、②CH3COONH4、 ③ NH4HSO4 、⑤NH4Cl等溶液中存在:NH4++H2O
Al(OH)3(胶体)+3H+,Al(OH)3胶体吸附悬浮颗粒使其沉降从而净化水;(2)①NH4Al(SO4)2 、②CH3COONH4、 ③ NH4HSO4 、⑤NH4Cl等溶液中存在:NH4++H2O![]() NH3H2O+H+,其中硫酸氢铵存在大量的H+,抑制NH4+的水解,NH4+浓度最大;NH4Al(SO4)2 中铝离子水解抑制铵根离子的水解,但抑制程度较小,NH4+浓度次之;醋酸铵为弱酸弱碱盐,发生相互促进的水解,四种物质中NH4+浓度最小;④氨水为弱电解质,难以电离,在这五种溶液中NH4+浓度最小,所以有:③①⑤②④;(3)①由于 NH4Al(SO4)2溶于水电离出的NH4+、Al3+水解溶液显酸性,且水解是吸热的,加入促进水解,溶液的酸性增强,pH减小,因此符合条件的曲线是I;(4)向100 mL0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L NaOH溶液,反应的离子方程式为H++OH-=H2O、OH-+NH4+=NH3·H2O。d点恰好中和氢离子,溶液中的NH4+水解促进水的电离。d点之后NH4+浓度减小,所以溶液中水的电离程度最大是a点;在b点,pH=7,溶液显中性,溶液中的溶质是硫酸钠和硫酸铵和氨气,则溶液中各离子浓度由大到小的排列顺序是(Na+)>c(SO42-)>c(NH4+>c(OH-)=c(H+);在cd段发生反应的离子方程式是NH4++OH-=NH3H2O。
NH3H2O+H+,其中硫酸氢铵存在大量的H+,抑制NH4+的水解,NH4+浓度最大;NH4Al(SO4)2 中铝离子水解抑制铵根离子的水解,但抑制程度较小,NH4+浓度次之;醋酸铵为弱酸弱碱盐,发生相互促进的水解,四种物质中NH4+浓度最小;④氨水为弱电解质,难以电离,在这五种溶液中NH4+浓度最小,所以有:③①⑤②④;(3)①由于 NH4Al(SO4)2溶于水电离出的NH4+、Al3+水解溶液显酸性,且水解是吸热的,加入促进水解,溶液的酸性增强,pH减小,因此符合条件的曲线是I;(4)向100 mL0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L NaOH溶液,反应的离子方程式为H++OH-=H2O、OH-+NH4+=NH3·H2O。d点恰好中和氢离子,溶液中的NH4+水解促进水的电离。d点之后NH4+浓度减小,所以溶液中水的电离程度最大是a点;在b点,pH=7,溶液显中性,溶液中的溶质是硫酸钠和硫酸铵和氨气,则溶液中各离子浓度由大到小的排列顺序是(Na+)>c(SO42-)>c(NH4+>c(OH-)=c(H+);在cd段发生反应的离子方程式是NH4++OH-=NH3H2O。


科目:高中化学 来源: 题型:
【题目】人工光合作用能够借助太阳能,用CO2和H2O制备化学原料。如图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是
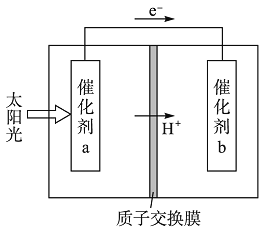
A. 该过程是将太阳能转化为化学能的过程
B. 催化剂a表面发生氧化反应,有O2产生
C. 催化剂a附近酸性减弱,催化剂b附近酸性增强
D. 催化剂b表面的反应是CO2+2H++2e-=HCOOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种常用的化工原料,如合成氨和尿素[CO(NH2)2]等。
(1)以H2合成CO(NH2)2的有关热化学方程式有:
①N2(g)+3H2(g)===2NH3(g)ΔH1=-92.4 kJ·mol-1
②NH3(g)+![]() CO2(g)===
CO2(g)===![]() NH2CO2NH4(s)ΔH2=-79.7 kJ·mol-1
NH2CO2NH4(s)ΔH2=-79.7 kJ·mol-1
③NH2CO2NH4(s)===CO(NH2)2(s)+H2O(l)ΔH3=+72.5 kJ·mol-1
则N2(g)、H2(g)与CO2(g)反应生成CO(NH2)2(s)和H2O(l)的热化学方程式为_______________________________________________________。
(2)电解制H2的原理为C(s)+2H2O(l)![]() CO2(g)+2H2(g)。某学习小组拟以二甲醚(CH3OCH3)-空气碱性燃料电池为电源,电解煤浆液(由煤粉与稀硫酸组成)探究上述原理,装置如图所示。
CO2(g)+2H2(g)。某学习小组拟以二甲醚(CH3OCH3)-空气碱性燃料电池为电源,电解煤浆液(由煤粉与稀硫酸组成)探究上述原理,装置如图所示。
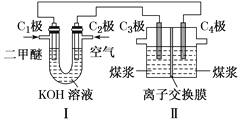
①分别写出电极C1和C3的电极反应式__________________;___________________。
②离子交换膜可能是________(填字母)。
a.阳离子交换膜 b.阴离子交换膜 c.质子交换膜
③已知4.6 g二甲醚参与反应,假设装置Ⅰ的能量转化率为100%,C4极收集到11.2L(标准状况)气体,装置Ⅱ的电流效率η=________。![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇可作为燃料电池的原料。通过下列反应可以制备甲醇:CO ( g ) + 2H2( g )CH3OH ( g ) △H=-90.8 kJ·mol-1在一容积可变的密闭容器中充入10 mol CO 和20 molH2,CO 的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A时,容器的体积为20 L。
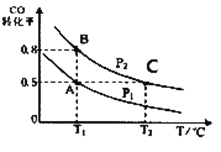
(1)该反应的化学平衡常数表达式为_____________。
(2)图中正反应速率:ν(A)___ν(B);平衡常数: K(A)_____K(C);平均摩尔质量:M(B)_____M(C)(填“>”、“<”或“=”)。
(3)关于反应CO(g)+2H2(g) CH3OH(g)在化学平衡状态时的描述正确的是_______(填字母)。
A.CO的含量保持不变
B.2V正(CH3OH)=V正(H2)
C.容器中CH3OH浓度与CO浓度相等
D.容器中混合气体的密度保持不变
(4)如反应开始时仍充入10mol CO 和20mol H2,则在平衡状态B时容器的体积V(B)为__________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向25℃时,体积均为20mL、浓度均为0. 1mol·L-1的两种酸HX、HY溶液中分別滴加0. 1mol·L-1的NaOH溶液,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是
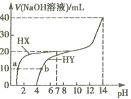
A. HX与NaOH溶液反应的离子方程式为:HX +OH-=X-+H2O
B. Ka(HY)的数量级约为10-10
C. b点时: c(Na+)=c(Y-)+c(HY)
D. V(NaOH)= 20mL时,两种反应后的溶液中c(X-)>c(Y-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按照下列元素基态原子的电子排布特征判断元素,并回答问题。
A元素的原子中只有一个能层且只含1个电子;B元素的原子3p轨道上得到1个电子后不能再容纳外来电子;C元素的原子的2p轨道上有1个电子的自旋方向与其他电子的自旋方向相反;D元素的原子第三能层上有8个电子,第四能层上只有1个电子;E元素原子的外围电子排布为3s23p6。
(1)写出由A、B、C、D中的三种元素组成的化合物的化学式: (至少写出5个)。
(2)写出用上述元素组成的物质制得A的单质的化学方程式: 、
(3)检验某溶液中是否含有D+,可通过 反应来实现;检验某溶液中是否含有B-,通常所用的试剂是 和 。
(4)写出E的元素符号: ,要证明太阳上是否含有E元素,可采用的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分类的正确组合是( )
碱 | 酸 | 盐 | 酸性氧化物 | |
A | 纯碱 | 盐酸 | 烧碱 | 二氧化硫 |
B | 烧碱 | 硫酸 | 食盐 | 一氧化碳 |
C | 苛性钠 | 醋酸 | 石灰石 | 水 |
D | 苛性钾 | 碳酸 | 苏打 | 三氧化硫 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】治疗癌症的有机小分子酯类药物X被批准使用。以芳香族化合物A为主要原料合成X的路线如下:
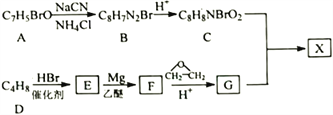
已知:
①核磁共振氢谱显示A有3种化学环境的氢,E只有1种化学环境的氢;
②![]()
③![]()
回答下列问题:
(1)A的名称是______________________;G中官能团名称是____________________。
(2)C在一定条件下反应生成高分子化合物,该反应的化学方程式为:__________________________。
(3)D生成E的反应类型为_____________________。
(4)X的结构简式为_____________________。
(5)已知:同一个碳原子若连有两个—OH时,易转化成![]() 。H是C的同分异构体,写出两种满足下列要求的H的结构简式______________________。
。H是C的同分异构体,写出两种满足下列要求的H的结构简式______________________。
①苯环上有两个取代基;
②能发生银镜反应,且在碱性条件下水解的两种产物也能发生银镜反应。
(6)参照上述合成路线和信息,用乙烯、乙醚、环氧乙烷为原料(其他无机试剂任选)合成1,6-己二酸_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com