
【题目】利用芳香烃X和烯烃Y可以合成紫外线吸收剂BAD.
已知:G不能发生银镜反应,B遇FeCl3溶液显紫色,C到D的过程为引入羧基(﹣COOH)的反应.其中BAD结构简式为: 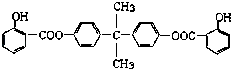
BAD的合成路线如下: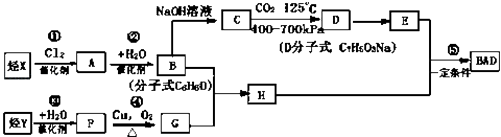
试回答下列问题:
(1)写出结构简式YD .
(2)属于加成反应的有(填数字序号) .
(3)1molBAD最多可与含molNaOH的溶液完全反应.
(4)写出方程式反应④ . F+E .
(5)E有多种同分异构体,判断符合下列要求的同分异构体数目为种.
①能发生银镜反应②遇FeCl3溶液显紫色③核磁共振氢谱图中有四个吸收峰.
【答案】
(1)CH3CH=CH2,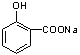
(2)③
(3)6
(4)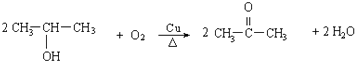 ,
,
(5)3
【解析】解:C到D的过程为引入羧基(﹣COOH)的反应,由转化关系可知E含有羧基,结合BAD结构简式可知E为 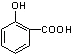 ,H为
,H为 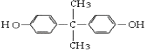 ,根据D的分子式结合E的结构可知D为
,根据D的分子式结合E的结构可知D为 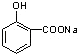 ,再根据B的分子式可知B为
,再根据B的分子式可知B为 ![]() ,则A为
,则A为 ![]() ,烃X为
,烃X为 ![]() ,F在Cu为催化剂条件下发生催化氧化生成G,G不能发生银镜反应,结合B和H的结构可知G为
,F在Cu为催化剂条件下发生催化氧化生成G,G不能发生银镜反应,结合B和H的结构可知G为 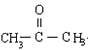 ,则F为CH3CH(OH)CH3,烃Y为CH3CH=CH2.
,则F为CH3CH(OH)CH3,烃Y为CH3CH=CH2.
(1)由上述分析可知,Y的结构简式为CH3CH=CH2,D的结构简式为:  ,
,
所以答案是:CH3CH=CH2;  ;
;
(2)由转化关系可知,①为取代反应,②为取代反应,③为加成反应,④为氧化反应,⑤为取代反应,
所以答案是:③;
(3)根据BAD结构简式可知,BAD水解生成4个酚羟基和2个羧基,则1molBAD最多可与含6molNaOH的溶液反应,
所以答案是:6;
(4)反应④的反应方程式为:  ,
,
F+E反应方程式为:  ,
,
所以答案是: 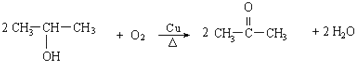 ;
;  ;
;
(5)E( 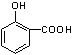 )的同分异构体有下列性质:①与FeCl3反应,溶液呈紫色,说明含有酚羟基;②能发生银镜反应,说明含有醛基,③核磁共振氢谱图中有四个吸收峰,说明分子组成中有4种H原子,符合条件的同分异构体的结构简式有:
)的同分异构体有下列性质:①与FeCl3反应,溶液呈紫色,说明含有酚羟基;②能发生银镜反应,说明含有醛基,③核磁共振氢谱图中有四个吸收峰,说明分子组成中有4种H原子,符合条件的同分异构体的结构简式有: ![]() 、
、  、
、 ![]() ,
,
所以答案是:3.


科目:高中化学 来源: 题型:
【题目】常温下,用20mL 移液管移取氨水至锥形瓶中,用0.05moL/LHCl溶液滴定。用pH计采集数据,电脑绘制的滴定曲线如下图所示。下列说法正确的是

A. 当pH=11.0时,NH3H2O的电离平衡常数Kb=1.78×10-5
B. 当pH=9.0 时,c(Cl-)>c(NH4+ )>c(OH-) >c(H+)
C. 当pH= 5.5时,溶液中有5 种微粒
D. 当pH= 7.0 时,氨水和HCl 溶液恰好完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香叶醇是合成玫瑰香油的主要原料,其结构简式如图所示:下列有关香叶醇的叙述正确的是( )
A.香叶醇的分子式为C10H18O
B.不能使溴的四氯化碳溶液褪色
C.不能使酸性高锰酸钾溶液褪色
D.能发生加成反应不能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尿黑酸是由酪氨酸在人体内非正常代谢而产生的一种物质.其转化过程如下:
下列说法错误的是( )
A.酪氨酸既能与盐酸反应,又能与氢氧化钠反应
B.1 mol尿黑酸与足量浓溴水反应,最多消耗3 mol Br2
C.对羟基苯丙酮酸分子中在同一平面上的碳原子至少有7个
D.1 mol尿黑酸与足量NaHCO3反应,最多消耗3 mol NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,向10mL.0.1mol/LCaCl2溶液中滴加0.1mol/L的Na2CO3溶液。滴加过程中溶液中-1gc(Ca2+)与Na2CO3溶液体积(V)的关系如图所示,下列有关说法正确的是( )
(已知1g5=0.7)

A. x、y两点c(Ca2+)之比为2000:3 B. Ksp(CaCO3)=5×10-9
C. w点对应的分散系很稳定 D. x、y、z三点中,水的电离程度最大的为x点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列原子或离子的基态电子排布式正确的是( )
A. Ni2+:[Ar]3d8 B. Cu:[Ar]3d94s2
C. S2-:[Ne]2s23p6 D. Si:[Ar]3s23p2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废弃物回收利用可变废为宝。某工业固体废物的组成为Al2O3、FeO、Fe2O3等。下图是以该固体废物为原料制取氧化铝、磁性Fe3O4胶体粒子的一种工艺流程:

(1)检验制备Fe3O4胶体粒子成功的实验操作名称是____________________________。
(2)写出由溶液B制备磁性Fe3O4胶体粒子的离子方程式__________________________________。
(3)由溶液B制得Fe3O4胶体粒子的过程中,须持续通入N2。其原因是____________________________。
(4)向溶液C中加入NaHCO3溶液,溶液的pH_________(填“增大”,“不变”或“减小”)。
(5)固体D是Al(OH)3,空温时Al(OH)3溶于NaOH溶液反应的平衡常数等于20,则此时Al(OH)3![]() A1O2-+H++H2O的电离常数K=_______________。
A1O2-+H++H2O的电离常数K=_______________。
(6)用重路酸钾(K2Cr2O7)可测定产物磁性Fe3O4胶体粒子中铁元素的含量,过程如下图。已知,反应中K2Cr2O7被还原为Cr3+。

①写出甲→乙的化学方程式___________________________________。
②写出乙→丙的离子方程式_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应mA(s)+nB(g)pC(g)△H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是( )
①m+n>p ②y点表示的正反应速率小于逆反应速率
③n>p ④x点比y点时的反应速率慢
⑤若降低温度,该反应的平衡常数增大.
A.①②⑤
B.②④⑤
C.只有①③
D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色济液中,只可能含有以下离子中的若干种:NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,,现取三份100mL溶液进行如下实验:
①第一份加足量AgNO3溶液后,有白色沉淀产生。
②第二份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99g
③第三份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图。根据上述实验,试回答下列问题:

(1)该溶液中一定不存在的阴离子有_______。
(2)实验③中NaOH溶液滴至35mL后发生的离子方程式为_______________________________。
(3)原得液确定含Mg2+、Al3+、NH4+,且n(Mg2+)∶n(Al3+)∶n(NH4+)=___________。
(4)实验所加的NaOH溶液的浓度为________。
(5)溶液中存在一种不能确定的阳离子,请设计实验方案加以检验_________________________。
(6)原溶液中NO3-的浓度为c(NO3-)则c(NO3-)的最小浓度为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com