
CO�dz����Ļ�ѧ���ʣ��й������ʺ�Ӧ�õ��о����¡�
��1����ͬѧ��ΪCO���Ա����Ը��������Һ����ΪCO2���������ʵ����֤��ͬѧ�IJ����Ƿ���ȷ��������������ͼ��������������ҩƷ�����ƻ�ѧʽ���Ӷ����������ƣ��������Բ���Ҳ���Բ�������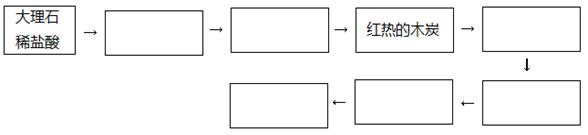
��2��CO��������һ�������¿��Ժϳ����ʻ�����[Fe(CO)5]�������ʿ�������Ǧ���͵ķ���������һ��dz��ɫҺ�壬�۵㡪20.5�棬�е�103�棬�����ڱ����л��ܼ���������ˮ���ܶ�1.46��1.52g/cm3���ж�������ʱ����Fe2(CO)9��60�淢����ȼ�����ʻ��������Ʊ�ԭ�����£�
Fe(s)+5CO(g) Fe(CO)5(g)
Fe(CO)5(g)
������˵����ȷ���� ��
| A������������Ӧԭ�����Ʊ��ߴ��� |
| B���Ʊ�Fe(CO)5Ӧ�ڸ��������������½��� |
C����ӦFe(s)+5CO(g) Fe(CO)5(g)��ƽ�ⳣ������ʽΪ Fe(CO)5(g)��ƽ�ⳣ������ʽΪ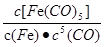 |
| D��Fe(CO)5Ӧ�ܷ⡢�������ܹⲢ����������ˮҺ������ |
��1��
��2����ABD ��Fe(CO)5+4NaOH=Na2Fe(CO)4+Na2CO3+2H2O ��Fe2O3�� 2��1
�����������������ʯ�����ᷢ����Ӧ����������̼���塣���������лӷ��ԣ������Ķ�����̼�����к���HCl�����ˮ������Ҫ���ñ��͵�̼��������Һ����ȥHCl���ʣ�Ȼ������Ũ������������õ������Ķ�����̼���塣ͨ�����ȵ�ľ̿�����߷�Ӧ������ԭ��Ӧ����CO��������������Һ���ʯ�ҳ�ȥδ��Ӧ�Ĺ�����CO2���壬��COͨ�뵽���Ը��������Һ�У���CO���Ա����Ը��������Һ����ΪCO2���ῴ�����Ը��������Һ����ɫ��ɫ���ó����ʯ��ˮ�����鲢��ȥ����CO2������ȼδ��ȫ��Ӧ��CO���壬��ֹ��Ⱦ��������2����A.�÷�Ӧ�ǿ��淴Ӧ�����ø÷�Ӧ����ʹ��̬������CO��Ӧ����Һ̬�����ʻ�����[Fe(CO)5]��ʹ��̬�����е����ʹ��˳�ȥ����ȷ��B.����[Fe(CO)5]���۵㡪20.5�棬�е�103�棬����ʱ����Fe2(CO)9��60�淢����ȼ�����Է�ӦҪ���ڸ��������������½��У��Է�ֹ[Fe(CO)5]��CO��Fe��������ȼ�ա���ȷ��C.�ڸ�ʵ��״̬��Fe�ǹ�̬�����Է�Ӧ�ﵽ��ѧƽ��ʱ��ƽ�ⳣ����K="C" [Fe(CO)5]/C5(CO). ����D.����[Fe(CO)5]���۵㡪20.5�棬�е�103�棬�����ڱ����л��ܼ���������ˮ���ܶȱ�ˮ��Ϊ1.46��1.52g/cm3���ж�������ʱ����Fe2(CO)9��60�淢����ȼ�����Fe(CO)5Ӧ�ܷ⡢�������ܹⲢ����������ˮҺ�����档��ȷ��ѡ��Ϊ��ABD�������ʻ�������������������Һ��Ӧ�Ļ�ѧ����ʽΪ��Fe(CO)5+4NaOH=Na2Fe(CO)4+Na2CO3+2H2O���۸��������غ㶨�ɿ�֪�ú���ɫ��ĩ��Fe2O3��2[Fe(CO)5]= Fe2(CO)9+CO��n(Fe2O3)=1.6g��160g/mol="0.01mol," n(Fe)="0.02mol." n(C)= 30.58g��44g/mol=0.695mol.n(H2O)= 5.4g��18g/mol=0.3mol,n(H)=0.6mol.��Ϊ�ڱ�C6H6��̼ԭ�Ӻ���ԭ�Ӹ�����Ϊ1:1�����Ժ����������к��е�̼Ԫ�ص����ʵ���Ϊ0.695mol-0.6mol=0.095mol������[Fe(CO)5]��Fe2(CO)9�����ʵ����ֱ�Ϊ��X��Y����أ����٣�0.02; 5X +9Y=0.095��������⡣���X=0.01��Y=0.005.����X��Y=2:1.
���㣺���鳣���Ļ�ѧ����CO�����ʺ�Ӧ�õ�֪ʶ��


 Ʒѧ˫�ž�ϵ�д�
Ʒѧ˫�ž�ϵ�д� Сѧ��ĩ���100��ϵ�д�
Сѧ��ĩ���100��ϵ�д� ��ĩ��ϰ���ϵ�д�
��ĩ��ϰ���ϵ�д� ����ѧ�䵥Ԫ������ĩר����100��ϵ�д�
����ѧ�䵥Ԫ������ĩר����100��ϵ�д� �Ƹ�360�ȶ����ܾ�ϵ�д�
�Ƹ�360�ȶ����ܾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�����������£���ijһ�ݻ��̶�����������ڳ��붡�飨������������ʹ�����ڻ��������ѹǿ�ﵽp1�����ȼ�գ�������Ӧ��ȫ����ȴ�����º��������������ѹǿΪp2��
��1��������ȼ�յ�������ֻ��H2O��Һ����CO2����p2/p1�� ��
��2����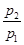 ��0.64����Ӧǰ������ж�������ʵ��������� ��
��0.64����Ӧǰ������ж�������ʵ��������� ��
�����谢���ӵ�����ΪNA���ڳ��³�ѹ�������Ħ�����ΪVm L��mol��1��O2��N2�Ļ������a g����b�����ӣ���c g�û�������ڳ��³�ѹ����ռ�����Ӧ�� L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�Ӻ�þ�����κ�ˮ���������õ������к���±ʯ(xKCl��yMgCl2��zH2O)����������طʺ���ȡ����þ����Ҫԭ�ϣ�����ɿ�ͨ������ʵ��ⶨ��
��ȷ��ȡ5.550g��Ʒ����ˮ�����100.0mL��Һ��
�ڽ���Һ�ֳɶ��ȷݣ���һ���м���������NaOH��Һ��������ȫ�����ˡ�ϴ�ӡ���
�������أ��õ���ɫ����0.580g��
������һ����Һ�м��������������ữ��AgNO3��Һ��������ȫ�����ˡ�ϴ�ӡ�����
�����أ��õ���ɫ����4.305g��
��1��������м����ɫ������ϴ���ķ����ǣ� ��
��2����֪ij�¶���Mg(OH)2��Ksp��6.4��l0?12������Һ��c(Mg2+)��1.0��10?5mol��L?1����Ϊ������ȫ������¶���Ӧ������Һ��c(OH��)�� mol��L?1��
��3��ͨ������ȷ����Ʒ����ɣ�д��������̣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ijѧ��������6��0 mol·L��1��H2SO4 1 000 mL��ʵ���������ֲ�ͬŨ�ȵ������480 mL 0��5 mol·L��1�������150 mL 25%������(�ѣ�1��18 g·mL��1)����������18 mol·L��1�����ᡣ�����ֹ�������ƿ��250 mL��500 mL��1 000 mL����ʦҪ��Ѣ٢���������ȫ�����꣬����IJ����ɢ������䡣
��ش��������⣺
��1��ʵ������25%����������ʵ���Ũ��Ϊ________mol·L��1(����1λС��)��
��2�����Ƹ�������ҺӦѡ������ƿ�Ĺ��Ϊ________mL��
��3������ʱ����ͬѧ�IJ���˳�����£��뽫��������B��D����������
A�����٢�����Һȫ�����ձ��л�Ͼ��ȣ�
B������Ͳȷ��ȡ����� 18 mol·L��1��Ũ���� mL���ز����������������Һ�С�
���ò��������裬ʹ���Ͼ��ȣ�
C������Ͼ��ȵ������ز�����ע����ѡ������ƿ�У�
D��______________________________________��
E��������������ƿ�м�ˮ��ֱ��Һ��ӽ��̶���1��2 cm����
F�����ý�ͷ�ιܼ�ˮ��ʹ��Һ�İ�Һ��ǡ����̶������У�
G��������ƿ�ǽ�����ҡ�ȡ�
��4�����ʡ�Բ���D����������ҺŨ���к�Ӱ�죿________(�ƫ����ƫС������Ӱ�족)��
��5�����в���Cǰ����ע��________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ͬ��ͬѹ�£���0.3molO2��0.2molO3�����ǵ�����֮��Ϊ ������������ԭ����֮��Ϊ �����ǵ����֮��Ϊ �����ǵ��ܶ�֮��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
һ������������������ȼ�գ����û������100ml 3.00mol/L��NaOH��Һǡ����ȫ���գ������Һ�к���NaClO�����ʵ���Ϊ0.05 mol��
��1��������Һ��Cl-�����ʵ���Ϊ mol��
��2���μӷ�Ӧ�������ڱ�״���µ������ L��(д��������̣���ͬ)
��3�����������Ͳμӷ�Ӧ�����������ʵ���֮��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��300 mL2mol/LH2SO4��Һ�У����ʵ������� ������Һ�к�H+�����ʵ����� ��H+�����ʵ���Ũ���� �����к��� ��SO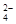 ��SO
��SO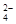 �����ʵ���Ũ���� ��
�����ʵ���Ũ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ij�о�С����CaCl2��H2Ϊԭ�ϣ���ͼ�Ʊ� +1��Ca�Ļ����������ֲ�����ֻ�����ֻ�������ң���Ԫ����ɷ���������������иơ���Ԫ�ص����������ֱ�Ϊ52.36%��46.33%���������ҵ�ˮ��Һ�����ԡ���ش��������⣺
��1�����о�С���Ƿ�ɹ��Ƶ� +1��Ca�Ļ���� ����ǡ������Ļ�ѧʽ�� ��
��2������ˮ��Ӧ�ɵ�H2���仯ѧ����ʽ�� ����Ӧ������Һ���ᾧ�ɵõ�һ�־��壬�仯ѧʽΪCaCl2�� xCa(OH)2�� 12H2O��Ϊȷ��x��ֵ�������ʵ�鷽�� ��
��3���ڼ��������£��ҵ�ˮ��Һ��Ũ����MnO2��Ӧ�����ӷ���ʽ�� ���ҵ�ˮ��Һ��Fe��Ӧ���õ���Һ���ȶ����������Һ�Ĵ�ʩ�� ��
��4����д��һ������Ϊ���ܵõ�CaCl�Ļ�ѧ����ʽ����CaCl2Ϊԭ�ϣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ʴ���
��֪��������[NaxFey(SO4)m(OH)n]���г��������������ʿ졢�����˵��ص㡣ij�о�С���Ƚ�ij��ˮ��Fe2������ΪFe3�����ټ���Na2SO4ʹ�����ɻ�����������ȥ����С��Ϊ�ⶨ������������ɣ�����������ʵ�飺
�ٳ�ȡ4.850 g��Ʒ����������ȫ�ܽ�����100.00 mL��ҺA��
����ȡ25.00 mL��ҺA������������KI����0.2500 mol��L��1Na2S2O3��Һ���еζ�����ӦΪI2��2Na2S2O3��2NaI��Na2S4O6��������30.00 mLNa2S2O3��Һ���յ㡣
����ȡ25.00 mL��ҺA��������BaCl2��Һ��ַ�Ӧ���ˡ�ϴ�ӡ������ó���1.165 g��
��1����С�鲻��������Fe(OH)3�����ķ�����ȥ��Ԫ�أ�����Ϊ���ɵ�Fe(OH)3 ��
��2����Na2S2O3��Һ���еζ�ʱ��ʹ�õ�ָʾ��Ϊ ���ζ����յ����ɫ�仯Ϊ ��
��3��ͨ������ȷ�����������Ļ�ѧʽ��д��������̣���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com