
[有机化学基础]
颠茄酸酯(J)是一种用于胃肠道平滑肌痉挛及溃疡病的辅助治疗药物,其合成路线如下:
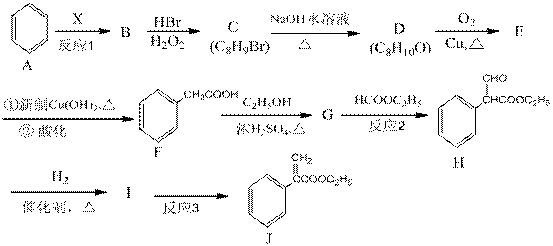
回答下列问题:
(1)烃B中含氢的质量分数为7.69%,其相对分子质量小于118,且反应1为加成反应,则B的分子式为___________,X的化学名称为 。
(2)C→D的反应类型为_____________,G→H 的反应类型为_____________。
(3)D的结构简式为___________________,G的结构简式为_______________________。
(4)反应3的化学方程式为_______________________________________________________。
(5)J的核磁共振氢谱有__________个峰。
(6)化合物I有多种同分异构体,同时满足下列条件的结构有 种。
①能发生水解反应和银镜反应
②能与FeCl3溶液发生显色反应
③苯环上有四个取代基,且苯环上一卤代物只有一种
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:高中化学 来源: 题型:
下列有关实验的选项正确的是:
| A.配制0.10mol/L NaOH溶 | B.除去CO中的CO2 | C.苯萃取碘水中的I2分出水层后的操作 | D.记录滴定终点读数为12.20mL |
|
|
|
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生产生活密切相关,下列说法不正确的是
A.小苏打可用作糕点的膨化剂
B.二氧化硫可用作食品的漂白剂
C.PX(对二甲苯)是生成塑料、聚酯纤维和薄膜的主要原料
D.PM2.5指数是雾霾天气监测中的重要指标
1.B
查看答案和解析>>
科目:高中化学 来源: 题型:
在常温下,对于pH=3的醋酸溶液。下列说法正确的是( )。
A.在醋酸溶液中,NH4+、Na、SiO32、C2O42能大量共存
B.与Na2S2O3溶液反应的离子方程式:S2O32+2H=S↓+SO2↑+H2O
C.常温下,加水稀释醋酸,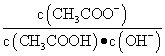 增大
增大
D.该醋酸溶液中c(CH3COO)<0.001 mol•L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定量经硫酸酸化的KMnO4溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+ 的物质的量随加入的KI的物质的量的变化关系如图所示,下列有关说法不正确的是
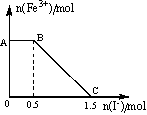
A.图中AB段发生的是过量的酸性KMnO4溶液与KI的反应
B.从题中可以得出还原性:I->Fe2+>Mn2+
C.取B点以后的少量溶液滴入几滴KSCN溶液,溶液变红色
D.根据OC段的数据可知,开始加入的KMnO4的物质的量为0.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
磺酰氯(SO2Cl2)和亚硫酰氯(SOCl2)均是实验室常见试剂。
已知: SO2Cl2(g) SO2(g) + Cl2(g) K1 △H=a kJ/mol (Ⅰ)
SO2(g) + Cl2(g) K1 △H=a kJ/mol (Ⅰ)
SO₂(g) +Cl₂(g)+ SCl₂(g) 2SOCl₂(g) K2 △H=b kJ/mol (Ⅱ)
2SOCl₂(g) K2 △H=b kJ/mol (Ⅱ)
(1)反应:SO2Cl2(g)+ SCl₂(g)  2SOCl2(g)的平衡常数K = (用K1、K2表示),该反应
2SOCl2(g)的平衡常数K = (用K1、K2表示),该反应
△H= kJ/mol(用a、b表示)。
(2)为研究不同条件对反应(Ⅰ)的影响,以13.5 g SO2Cl2充入2.0L的烧瓶中,在101kPa 375K时,10min达到平衡,平衡时SO2Cl2转化率为0.80,则0~10minCl2的平衡反应速率为 ,平衡时容器内压强为 kPa,该温度的平衡常数为 ;若要减小SO2Cl2转化率,除改变温度外,还可采取的措施是 (列举一种)。
(3)磺酰氯对眼和上呼吸道粘膜有强烈的刺激性,发生泄漏时,实验室可用足量NaOH固体吸收,发生反应的化学方程式为 ;亚硫酰氯溶于水的离子方程式为 。
(4)一定量的Cl2用稀NaOH溶液吸收,若恰好反应,则溶液中各离子浓度由大到小的顺序为 ;
已知常温时次氯酸的Ka=2.5×10-8则该温度下NaClO水解反应的平衡常数
Kb= mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
2013年11月江苏在大部分地市推广使用含硫量大幅减少的苏V汽油。下列有关汽油的说法正确的是( )
A.汽油属于可再生能源
B.将原油通过萃取、分液可获得汽油
C.使用苏V汽油可降低酸雨发生率
D.苏V汽油只含C、H、O三种元素
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验现象与对应结论不正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 常温下将Cu片放入浓H2SO4中 | 生成刺激性气味气体 | Cu与浓H2SO4反应生成SO2 |
| B | Al2(SO4)3溶液中滴加过量氨水 | 生成白色胶状物质 | Al(OH)3不溶于氨水 |
| C | 向某溶液中加入KSCN溶液,再向溶液中加入新制氯水 | 溶液先不显红色,加入氯水后变红色 | 该溶液中含有Fe2+ |
| D | 向某溶液中加入CCl4,振荡后静置 | 液体分层,下层呈紫红色 | 该溶液中存在I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
针对下面10种元素,完成以下各小题。
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(1)地壳中含量最多的元素是___________(填名称)。
(2)化学性质最不活泼的元素是___________(填元素符号)。
(3)Al的原子结构示意图为___________________。
(4)C与N相比,原子半径较小的是___________。
(5)最高价氧化物对应的水化物碱性最强的是___________(填化学式)。
(6)MgO和Al2O3中,属于两性氧化物的是___________。
(7)S和Cl相比,元素非金属性较强的是___________。
(8)可用来制造光导纤维的物质是___________,晶体硅的主要用途是___________(写出一种)。
(9)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式:____________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com