
| A. | 同种元素的原子均有相同的质子数和中子数 | |
| B. | 同主族元素的简单阴离子还原性越强,水解程度越大 | |
| C. | 同周期金属元素的化合价越高,其原子失电子能力越强 | |
| D. | 短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构 |
分析 A、同种元素的不同核素质子数相同,中子数不同;
B、同主族元素的简单阴离子还原性越强,越难水解;
C、同周期金属元素的化合价越高,越难失去电子;
D、短周期第ⅣA与ⅦA族元素的原子间构成的分子,化合物为XY4型,共价键数+原子最外层电子数=8满足8电子.
解答 解;A、同种元素的不同核素质子数相同,中子数不同,故A错误;
B、同主族元素的简单阴离子还原性越强,越难水解,如卤族元素中,碘离子还原性最强,不水解,故B错误;
C、同周期金属元素的化合价越高,越难失去电子,如第三周期中,Na比Al容易失去电子,故C错误;
D、ⅣA(用X表示)与ⅦA(用Y表示)形成的化合物为XY4,X形成四个键,加上原来的4个电子,最外层共8个电子,每个Y形成一个键,加上原来的7个电子,共8个电子,故D正确.
故选:D.
点评 本题考查元素周期表和元素周期律的应用,注意同周期、同主族元素的性质变化规律是解答本题的关键,注意利用实例分析问题,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ②③⑤ | C. | ③④ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ②③⑤ | C. | ①④⑤ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{m-x-2}{W-m}$ mol | B. | $\frac{W(m-x)}{m}$ mol | C. | $\frac{W(m-x-2)}{m}$mol | D. | $\frac{W(m-x+2)}{m}$ mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 奥运会中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中正确的是( )
奥运会中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中正确的是( )| A. | 该物质与苯酚属于同系物 | |
| B. | 该物质不能使酸性KMnO4溶液褪色 | |
| C. | 1 mol该物质与浓溴水反应时最多消耗Br2为4 mol | |
| D. | 该分子中的所有原子共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
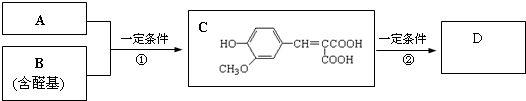
 .
.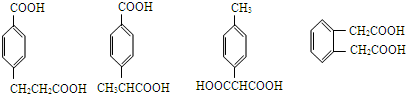 任意一种.
任意一种.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素原子核内质子数为8+b | |
| B. | b≥4时形成的单质均为绝缘体 | |
| C. | 随着b数字的增大(b<8),元素的原子半径逐渐减小 | |
| D. | 随着b数字的增大,元素单质的还原性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K2CO3和CaSO4都属于盐 | B. | H2SO4和HNO3都属于酸 | ||
| C. | KOH和Fe(OH)3都属于碱 | D. | Na2O和Na2SiO3都属于氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com