
| A. | 将58.5gNaCl溶于1L水中可得1mol/L的NaCl溶液 | |
| B. | 将标准状况下22.4LHCl溶于1L水中可得1mol/L盐酸 | |
| C. | 将 25.0g胆矾溶于水后配成100mL溶液所得溶液浓度为1mol/L | |
| D. | 将 78gNa2O2溶于水,配成1L溶液可得到浓度为1mol/L溶液 |
分析 A.物质的量浓度中,体积为溶液的体积不是溶剂的体积;
B.标准状况下22.4L HCl溶于1L水,所得溶液的体积不等于1L;
C.25.0g胆矾中含硫酸铜的物质的量为0.1mol,溶液的体积为100ml,依据C=$\frac{n}{V}$分析;
D.依据Na2O2~2NaOH,计算78g Na2O2溶于水生成的氢氧化钠的物质的量,依据C=$\frac{n}{V}$分析解答.
解答 解:A.将58.5g NaCl的物质的量为1mol,溶于1L水中,配成的溶液的体积大于1L,浓度小于1mol•L-1,故A错误;
B.标准状况下22.4L HCl的物质的量为1mol,但是将标准状况下22.4L HCl溶于1L水得到溶液的体积大于1L,所以浓度不等于1mol/L,故B错误;
C.25.0g胆矾中含硫酸铜的物质的量为0.1mol,溶液的体积为100ml,c=$\frac{n}{V}$=$\frac{0.1mol}{0.1L}$=1mol/L,故C正确;
D.78g Na2O2溶于水反应生成2mol氢氧化钠,溶液的体积为1L,溶液的浓度为2mol/L,故D错误;
故选:C.
点评 本题考查一定物质的量浓度溶液的配制,难度不大,明确物质的量浓度定义是解题关键,注意体积为溶液的体积.


科目:高中化学 来源: 题型:选择题
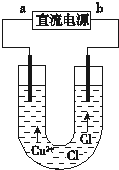
| A. | a极为电源正极 | B. | 每生成6.4gCu,转移电子0.2 mol | ||
| C. | 阳极反应式:Cu2++2e→Cu | D. | 在直流电源中电流从b流向a |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
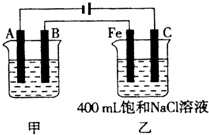 如图为相互串联的甲、乙两电解池.试回答:
如图为相互串联的甲、乙两电解池.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Fe+3Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3 | B. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | ||
| C. | CaO+CO2═CaCO3 | D. | 2H2O+2Na═2NaOH+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中加入AgNO3溶液,生成白色沉淀,可确定有Cl-存在 | |
| B. | 向某溶液中加入氢氧化钠溶液,产生蓝色沉淀,可确定有Cu2+存在 | |
| C. | 向某溶液中加入BaCl2溶液,生成白色沉淀,加稀盐酸沉淀不溶解,可确定有SO${\;}_{4}^{2-}$存在 | |
| D. | 向某溶液中加入稀盐酸,生成的气体能使澄清石灰水变浑浊,可确定有CO${\;}_{3}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol | B. | 0.2 mol | C. | 0.3mol | D. | 0.4 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com