
科目:高中化学 来源: 题型:
能够说明一个可逆反应H2(g)+I2(g)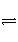
 2HI(g)已达到平衡状态的是( )
2HI(g)已达到平衡状态的是( )
A.1 mol H—H键断裂的同时有1 mol H—I键形成
B.1 mol H—H键断裂的同时有2 mol H—I键形成
C.1 mol I—I键断裂的同时有2 mol HI键形成
D.1 mol H—H键断裂的同时有1 mol I—I键形成
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某溶液X可能由K+、Mg2+、Cu2+、Ag+、Ba2+、Al3+、Fe2+、AlO 、CO
、CO 、SO
、SO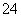 、I-、SiO
、I-、SiO 、MnO
、MnO 中的若干种离子组成。某化学兴趣小组通过下列实验确定了其组成。
中的若干种离子组成。某化学兴趣小组通过下列实验确定了其组成。
(1)根据下列实验步骤和现象,推断实验结论:
| 实验步骤与实验现象 | 实验结论 |
| Ⅰ.观察溶液:无色透明 | ①原溶液中一定不含的离子是____________ |
| Ⅱ.取适量该溶液,加入过量的硝酸,有气体生成,并得到无色溶液 | ②原溶液中一定不含的离子是__________________________,一定含有的离子是________ |
| Ⅲ.在Ⅱ所得溶液中再加入过量的碳酸氢铵溶液,有气体生成,同时析出白色沉淀A | ③原溶液中还一定含有的离子是________,生成沉淀A的离子方程式为___________________ |
| Ⅳ.在Ⅲ所得溶液中再逐滴加入氢氧化钡溶液至过量,加热也有气体生成,同时析出白色沉淀B | ④白色沉淀B中一定含有_____ __,可能含有________________ |
(2)上述实验步骤Ⅳ中开始阶段发生反应的离子方程式一定有____________。

(3)该化学兴趣小组的同学为了进一步确定B的成分,取一定量经洗涤后的B与Y溶液反应,白色固体的物质的量与Y溶液体积之间的关系如图所示。
Y可能为______________________。B的组成为_______________________。
(4)已知氢氧化铝电离出H+比碳酸氢钠电离出H+更难。根据上述推断,取少量原溶液于试管中,向试管中滴加少量硫酸氢钠稀溶液至过量,按先后顺序可以观察到的现象有_____________________________________________。
写出最后发生反应的离子方程式:____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D是中学常见的混合物分离或提纯的基本装置。
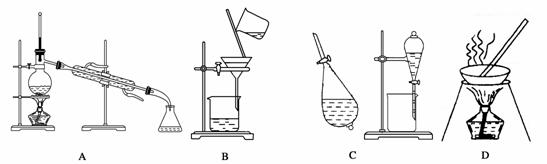
请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
(1)除去Ca(OH)2溶液中悬浮的CaCO3__________________________________________;
(2)从碘水中提取碘__________________________________________;
(3)用自来水制取蒸馏水___________________________________;
(4)分离植物油和水_______________________________________;
(5)除去粗盐中的泥沙__________________________________________;
(6)与海水晒盐原理相符的是__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机物的叙述,错误的是
A.乙烯能使溴水和酸性KMnO4溶液褪色
B.体积分数为75%的酒精溶液会使细菌蛋白质变性
C.1 mol甲烷和1 mol氯气在光照条件下充分反应,生成1 mol CH3Cl
D.CH3CH2CH2CH3和CH3CH (CH3)2互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
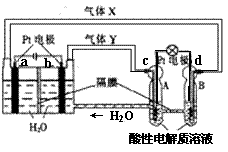
“天宫一号” RFC供电系统是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池。右图为RFC工作原理示意图,有关说法正确的是
A.当转移0.1 mol电子,a极产生2.24 L H2
B.b电极反应是:4H2O +4e-=2H2↑+4OH—
C.d电极反应是:O2 +4H+ +4e-=2H2O
D.c极上发生还原反应,B中H+经隔膜进入A
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃时有关弱酸的电离平衡常数如下。下列有关说法正确的是
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×l0-10 | K1=4.3×10-7 K2=5.6×10-11 |
A.NaHCO3溶液中,一定有c(Na+)=c(HCO3—)+c(CO32—)
B.将amol•L—1HCN溶液与amol•L—1NaOH溶液等体积混合后,测得所得溶液显碱性(pH>7),则c(OH—)>c(H+),c(CN—)>c(Na+)
C.等物质的量浓度的各溶液pH关系为:
pH(Na2CO3)>pH(NaCN)>pH(CH3COONa)
D.1mol/L醋酸溶液加水稀释,溶液中所有离子浓度均减小
查看答案和解析>>
科目:高中化学 来源: 题型:
防止钢铁的腐蚀是世界级难题,每年全世界钢产量的四分之一因腐蚀而损失,根据下图回答:
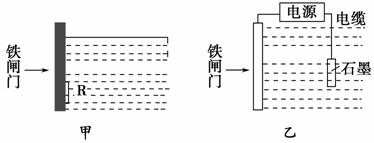
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为________________________________________________________________。
(2)为降低某水库的铁闸门的被腐蚀速率,可以采用图甲方案,其中焊接在铁闸门上的固体材料R可以采用__________。
A.铜 B.钠 C.锌 D.石墨
(3)图乙所示方案也可降低铁闸门的被腐蚀速率,其中铁闸门应该连接在直流电源的________极。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.汽油、柴油和植物油都是碳氢化合物
B.乙醇可以被氧化为乙酸,二者都能发生酯化反应
C.甲烷、乙烯和苯在工业上都可通过石油分馏得到
D.含5个碳原子的有机物,每个分子中最多可形成4个C—C单键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com