“嫦娥一号”的登月成功,实现了中国人“奔月”的梦想.
(1)2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ?mol-1
C(s)+O2(g)═CO2(g);△H=-393.5kJ?mol-1
C8H18(l)+12.5O2(g)═8CO2(g)+9H2O(l);△H=-5518kJ?mol-1
CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H=-890kJ?mol-1
相同质量的H2、C、C8H18、CH4完全燃烧时,放出热量最多的是______.
(2)氢气、氧气不仅燃烧能放出热量,二者形成的原电池还能提供电能.“嫦娥一号”绕月飞行部分使用的是氢氧燃料电池,电解质溶液为KOH溶液,其电极反应式为:负极______;正极______;
(3)若用氢氧燃料电池电解100mL由NaCl和CuSO4组成的混合溶液,其中[Na+]=3[Cu2+]=0.3mol?L-1,用石墨作电极,通电一段时间后,在阴极收集到0.112LH2(标况).试计算:
①阴极析出Cu______mol.阳极析出气体为______(填化学式).
②若所得溶液仍然为100mL,则此时溶液的pH值为______.



 天天向上口算本系列答案
天天向上口算本系列答案 2PbSO4 +2H2O。请依据上述情况判断:⑴铅蓄电池的负极材料是 。
2PbSO4 +2H2O。请依据上述情况判断:⑴铅蓄电池的负极材料是 。
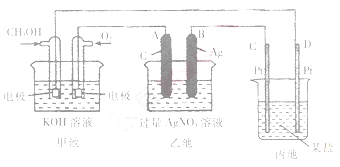
 、
、 可以大量共存
可以大量共存 ==
==