
【题目】一种芳纶纤维的拉伸强度比钢丝还高,广泛用作防护材料。其结构片段如下图

下列关于该高分子的说法正确的是
A. 完全水解产物的单个分子中,苯环上的氢原子具有不同的化学环境
B. 完全水解产物的单个分子中,含有官能团―COOH或―NH2
C. 氢键对该高分子的性能没有影响
D. 结构简式为:![]()
科目:高中化学 来源: 题型:
【题目】下表是某些原子晶体的熔点和硬度,分析表中的数据,判断下列叙述正确的是( )
原子晶体 | 金刚石 | 氮化硼 | 碳化硅 | 石英 | 硅 | 锗 |
熔点/℃ | 3 900 | 3 000 | 2 700 | 1 710 | 1 410 | 1 211 |
硬度 | 10 | 9.5 | 9.5 | 7 | 6.5 | 6.0 |
①构成原子晶体的原子种类越多,晶体的熔点越高
②构成原子晶体的原子间的共价键的键能越大,晶体的熔点越高
③构成原子晶体的原子半径越大,晶体的硬度越大
④构成原子晶体的原子半径越小,晶体的硬度越大
A.①② B.③④ C.①③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na![]() 2Na2CO3+C。下列说法错误的是
2Na2CO3+C。下列说法错误的是

A. 放电时,ClO4-向负极移动
B. 充电时释放CO2,放电时吸收CO2
C. 放电时,正极反应为:3CO2+4e =2CO32-+C
D. 充电时,正极反应为:Na++e=Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是 ( )
A. 标准状况下,22.4L水中所含的分子数约为6.02×1023
B. 标准状况下,aL的氧气和氮气的混合物含有的分子数约为![]() ×6.02×1023
×6.02×1023
C. 22 g二氧化碳与标准状况下11.2 L 氯化氢气体含有的分子数不同
D. 2.24L CO2中含有的原子数为0.3×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学按下列步骤配制500mL 0.200mol·L-1 Na2CO3溶液,请回答有关问题。
实验步骤 | 有关问题 |
(1)计算所需Na2CO3的质量 | 需要Na2CO3的质量为_________g。 |
(2)称量Na2CO3固体 | 称量过程中主要用到的仪器是_____ |
(3)将Na2CO3加入100mL烧杯中 | 为加快溶解速率,可采取的措施是___ |
(4)将烧杯中的溶液转移至500mL容量瓶中 | 为防止溶液溅出,应采取的措施是____________________________________________________________________________ |
(5)向容量瓶中加蒸馏水至刻度线 | 在进行此操作时应注意的问题是______ |
(6)你认为按上述步骤配制的Na2CO3溶液的浓度是否为0.200mol·L-1,请说明理由。________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】叠氮化钠(NaN3)是一种无色晶体,常见的两种制备方法为2NaNH2+N2O==NaN3+NaOH+NH3,3NaNH2+NaNO3==NaN3+3NaOH+NH3↑。
回答下列问题:
(1)氮元素所在的周期中,电负性最大的元素是________,第一电离能最小的元素是_______。
(2)基态氮原子的L层电子排布图为_________________。
(3)与N3-互为等电子体的分子为_________(写出一种)。依据价层电子对互斥理论,NO3-的空间构型是______________,其中心原子杂化类型是__________。
(4)叠氮化钠中不含有的化学键类型有_____________。
A.离子键 B.极性共价键 C.σ键 D.π键
(5)N2O沸点(-88.49℃)比NH3沸点(-33.34℃)低,其主要原因是____________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“低碳经济”已成为全世界科学家研究的重要课题。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
(1)已知:①CO(g)+H2O(g)![]() H2(g)+CO2(g) ΔH=-41 kJ·mol-1
H2(g)+CO2(g) ΔH=-41 kJ·mol-1
②C(s)+2H2(g)![]() CH4(g) ΔH=-73 kJ·mol-1
CH4(g) ΔH=-73 kJ·mol-1
③2CO(g)![]() C(s)+CO2(g) ΔH=-171 kJ·mol-1
C(s)+CO2(g) ΔH=-171 kJ·mol-1
写出CO2与H2反应生成CH4和H2O(g)的热化学方程式:_____________________________________。
(2)目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,在容积为2 L的密闭容器中,充入1 mol CO2和3.25 mol H2在一定条件下发生反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化如图所示:
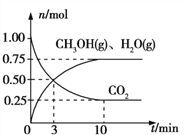
①反应的化学方程式为:____________________________________________________。
②从反应开始到平衡,氢气的平均反应速率v(H2)=_____________mol/(Lmin)。
(3)煤化工通常研究不同条件下CO转化率以解决实际问题。已知在催化剂存在条件下反应:CO(g)+H2O(g)![]() H2(g)+CO2(g)中CO的平衡转化率随p(H2O)/p(CO)及温度变化关系如图所示: [p(H2O)、p(CO)表示H2O、CO的平衡分压,分压=总压×物质的量分数]:
H2(g)+CO2(g)中CO的平衡转化率随p(H2O)/p(CO)及温度变化关系如图所示: [p(H2O)、p(CO)表示H2O、CO的平衡分压,分压=总压×物质的量分数]:
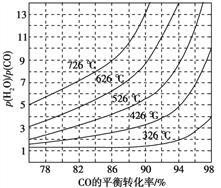
①上述反应的逆反应方向是_____________反应(填“吸热”或“放热”);
②对于气相反应,用某组分(B)的平衡分压(pB)代替平衡浓度(cB)也可以表示平衡常数(记作Kp),,则该反应的Kp=______________,提高![]()
![]() ,则Kp_____________(填“变大”“变小”或“不变”)。使用铁镁催化剂的实际工业流程中,一般采用400 ℃左右、
,则Kp_____________(填“变大”“变小”或“不变”)。使用铁镁催化剂的实际工业流程中,一般采用400 ℃左右、![]()
![]() =3~5,采用此条件的原因可能是______________________________________________________________________。
=3~5,采用此条件的原因可能是______________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关溶液的说法正确的是
A. 向AgCl、AgBr的混合饱和溶液中加入少量AgNO3固体,溶液中![]() 不变
不变
B. 将CH3COONa溶液从20C升温至30C,溶液中![]() 增大
增大
C. 向盐酸中加入氨水至中性,溶液中![]()
D. 同0.1mol/LCH3COOH溶液中加入少量水.溶液中![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于数千万计的化学物质和为数更多的化学反应,分类法的作用几乎是无可替代的。下图为一“链状连环”图案,图案上由左到右分别写了Cl2、NO2、Na2O2、Na2CO3、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分由左到右用A、B、C、D代替。
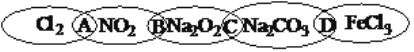
请回答下列问题:
(1)请将上述字母代号填入相应的括号内。
①两种物质都不属于电解质(________) ②两种物质都属于钠的化合物(________)
③两种物质都属于氧化物(_______) ④两种物质都属于盐类(________)
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入1molL-1的上图中一种化合物的饱和溶液,可制得一种红褐色的胶体。
①该反应的离子方程式为___________________________________。
②如何用较简单的方法判断胶体是否制备成功?____________________________。
③向该胶体中逐滴加入稀硫酸,先出现红褐色沉淀,随后红褐色沉淀溶解,其原因是_______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com