
����Ŀ���ζ�ʵ���ǻ�ѧѧ������Ҫ�Ķ���ʵ�顣��ش��������⣺
I������к͵ζ������ñ�����ζ�δ֪Ũ�ȵ�NaOH��Һ��
(1)��ѧ����ʵ��������£�
a���ü�ʽ�ζ���ȡϡNaOH 25.00 mL��ע����ƿ�У����������ָʾ����
b���ô��ⶨ����Һ��ϴ��ʽ�ζ��ܡ�
c��������ˮϴ�ɾ��ζ��ܡ�
d��ȡ����ʽ�ζ����ñ���HCl��Һ��ϴ����Һע��ζ��̶ܿ���0������2��3 cm�����ٰѵζ��̶ܹ��ã�����Һ�����̶���0������0���̶����¡�
e�����ζ����Ƿ�©ˮ��
f����ȡ��ƿ�����ظ�����һ�Ρ�
g������ƿ���ڵζ������棬ƿ�µ�һ�Ű�ֽ���ߵα�ҡ����ƿֱ���ζ��յ㣬���µζ���Һ�����ڿ̶ȡ�
�ٵζ���������ȷ˳����(�������д)___________________��
��ij�εζ�ǰ�����ʢ������ζ�����Һ���λ�á���ش�
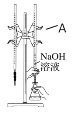
����A��������_____________�����������������ζ�ǰ����Ϊ____mL���ζ������Ϊ____mL��
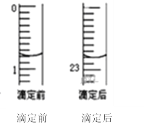
����g���������ȷ���յ�________________��
(2)���в�����ɲⶨ���ƫ�ߵ���______(��ѡ����ĸ)��
A���ζ��յ�ʱ�����ӵζ�����ҺҺ��
B��ʢװδ֪Һ����ƿ������ˮϴ����δ��δ֪Һ��ϴ
C����ʽ�ζ���������ˮϴ����δ�ñ�������ϴ
D���ζ�ǰ���ζ��ܼ��������ݣ��ζ���������ʧ
II��������ԭ�ζ�����ȡ������Һ������ƿ�У���������ϡ���ᣬ��Ũ��Ϊ0.1 mol/L�ĸ��������Һ�ζ��������ķ�ӦΪ��2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2��+2MnSO4+8H2O�������м�¼��ʵ�����ݣ�
�ζ����� | ����Һ���(mL) | ��KMnO4��Һ���(mL) | |
�ζ�ǰ���� | �ζ������ | ||
��һ�� | 25.00 | 0.50 | 20.40 |
�ڶ��� | 25.00 | 3.00 | 23.00 |
������ | 25.00 | 4.00 | 24.10 |
(1)�ζ�ʱ��KMnO4��ҺӦװ��___(��������������)ʽ�ζ����У��ζ��յ�ʱ��ƿ�ڵ���ɫ�仯��___��
(2)�ò�����Һ�����ʵ���Ũ��Ϊ__________��
���𰸡�e��c��b��a��d��g��f ��ʽ�ζ��� 0.80 22.80 ���������һ����Һ����ƿ���ɻ�ɫ��Ϊ��ɫ�Ұ�����ڲ���ɫ CD �� ��ɫ��Ϊdz��ɫ���Ұ�����ڲ���ɫ 0.2 mol/L
��������
I.(1)�ٵζ�ʵ�鲽���м�©��ϴ�ӡ���ϴ��װҺ��ȡ����Һ��ָʾ�����ζ��Ȳ�����
�ڸ��������ṹ�ж��������ƣ����ݵζ���С�̶����ϣ���̶����£���ϵζ�ǰ��Һ�尼Һ��λ�ö�����
�۸����ü�����ָʾ��ʱ����Һ�ɻ�ɫ���ɫ���Ұ�����ڲ���ɫ����ζ��յ㣻
(2)���ݲ��������ı���Һ�����С�������Һ�����ʵ���Ũ�ȶ���ʽ����ʵ����
II.(1)���ݸ��������Һ����ǿ������ѡ��ζ������ͣ����ݵζ�����ǰ��ҺΪ��ɫ���ζ�����ʱ��Һ����Ϻ�ɫΪ�ζ��յ㣻
(2)���жϵζ����ݵ���Ч�ԣ�Ȼ���������ı�Һ��ƽ��������ٸ���c(����)=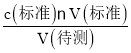 �������������Һ��Ũ�ȡ�
�������������Һ��Ũ�ȡ�
I.(1)���к͵ζ����������м�©��ϴ�ӡ���ϴ��װҺ��ȡ����Һ����ָʾ�����ζ��Ȳ��������Եζ���������ȷ˳����e��c��b��a��d��g��f��
������AΪ�²��в������������Ϊ��ʽ�ζ��ܣ���ϵζ��ܽṹ��֪���ڵζ�ǰ����Ϊ0.80 mL���ζ������Ϊ22.80 mL��
���ü�����ָʾ��ʱ����Һ�ɻ�ɫ���ɫ���Ұ�����ڲ���ɫ����ζ��յ㣻
(2) A.�ζ��յ����ʱ�����ӵζ��ܵĿ̶ȣ����V(��)ƫС������c(����)=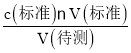 ������֪��c(����)ƫС��A���������⣻
������֪��c(����)ƫС��A���������⣻
B.ʢװδ֪Һ����ƿ������ˮϴ����δ��δ֪Һ��ϴ����V(��)��Ӱ�죬����c(����)=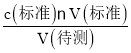 ������֪��c(����)���䣬B���������⣻
������֪��c(����)���䣬B���������⣻
C.��ʽ�ζ���������ˮϴ����δ�ñ�������ϴ��������Ũ��ƫС�����V(��)ƫ����c(����)ƫ��C�������⣻
D.�ζ�ǰ���ζ��ܼ��������ݣ��ζ���������ʧ�����V(��)ƫ�����յ�c(����)ƫ��D�������⣻
�ʺ���ѡ����CD��
II.(1)���Ը��������Һ����ǿ�����ԣ��ܹ�������ʽ�ζ��ܵ��ܣ�����Ӧ��ʹ����ʽ�ζ���ʢװ���Ը��������Һ���ζ�����ǰ���ҺΪ��ɫ���ζ�����ʱ���Һ�����dz��ɫ�����Եζ��յ�����Ϊ����ƿ����Һ����ɫ��Ϊdz��ɫ���Ұ�����ڲ���ɫ��
(2)���εζ����ı�Һ��������ֱ�Ϊ��(20.400.50)mL=19.90 mL��(23.003.00)mL=20.00m L��(24.104.00)mL=20.10 mL���������εζ������ݶ���Ч�������ı�Һ��ƽ�����ΪV=![]() =20.00 mL��������ص����ʵ���Ϊn(KMnO4)=cV=0.10 mol/L��0.020 L=0.0020 mol�����ݷ�Ӧ2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2��+2MnSO4+8H2O��֪��n(H2C2O4)=
=20.00 mL��������ص����ʵ���Ϊn(KMnO4)=cV=0.10 mol/L��0.020 L=0.0020 mol�����ݷ�Ӧ2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2��+2MnSO4+8H2O��֪��n(H2C2O4)=![]() n(KMnO4)= 0.005 mol���ʴ���Һ��������ʵ���Ũ��c(H2C2O4)=
n(KMnO4)= 0.005 mol���ʴ���Һ��������ʵ���Ũ��c(H2C2O4)=![]() =0.2 mol/L��
=0.2 mol/L��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������Ҫ��Fe2O3��SiO2���Ʊ�����Fe3O4�Ĺ����������£�
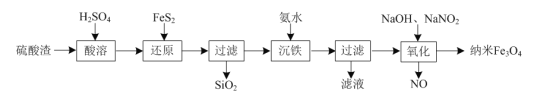
��1������ԭ��ʱFeS2������ΪSO![]() ���÷�Ӧ�����ӷ���ʽΪ��_____��
���÷�Ӧ�����ӷ���ʽΪ��_____��
��2���������������е����ӷ�Ӧ����ʽΪ��______��
��3���������������е����ӷ���ʽΪ��________��
��4��һ����������FeƬ��������ʯī���������NaCl��ҺҲ���Ƶ�����Fe3O4��д���÷�Ӧ�Ļ�ѧ����ʽ��_________��
��5�����������£�NO�ɱ�NH3����ԭΪN2��H2O����n(NO)��n(O2)��4��1ʱ���÷�Ӧ�Ļ�ѧ����ʽ��_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��д���������з���ʽ������һ���˴Ź����źŵĻ�����Ľṹ��ʽ��
(1)C5H12_________________________��
(2)C3H6__________________________��
(3)C2H6O________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���20.00mL 0.1000mol��L1�����еμ�0.1000mol��L1 NaOH��Һ����Һ��pH��NaOH��Һ����ı仯��ͼ����֪lg3=0.5���ڱ�������Ϊ���ᡣ����˵������ȷ����( )
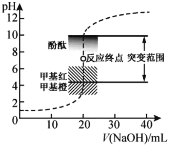
A.ѡ���ɫ��Χ��pHͻ�䷶Χ�ڵ�ָʾ�����ɼ�Сʵ�����
B.����ʽ�ζ�����ȡ20.00mL 0.1000mol��L1����ʱ����ʽ�ζ���ˮϴ�����ô�ȡҺ��ϴ
C.NaOH����ҺŨ�ȵ�ȷ��ֱ��Ӱ���������Ŀɿ��ԣ���������ڱ����������Ʊ궨NaOH��Һ��Ũ�ȣ��궨ʱ���ü���Ϊָʾ��
D.V(NaOH)=10.00mL ʱ��pHԼΪ1.5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���᳧������SO2�Ļ������÷�����ͼ��ʾ������˵������ȷ����
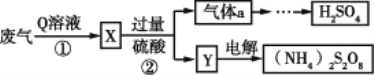
A.Q��Һ�ǰ�ˮ
B.��ҵ����������a��ͨ��������Ӧת��ΪH2SO4
C.�������б�������Ԫ������
D.��Ʋ���١�����Ϊ�˸���SO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʵ��������Ҫ�������Ȼ�����Һ,��ʵ����ֻ�л��������ơ�̼����淋��Ȼ���.ijѧ����������·��������ᴿ:
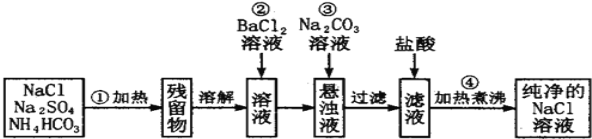
(1)�������ܷ��Ϊ�����ᱵ��Һ��______(��ܡ���) ������_____________________________��
(2)���в����ں�,����ж�SO42- �ѳ���,������___________________��
(3)�����ܵ�Ŀ����_______________________________��
�����������(NH4)2SO4��FeSO4��6H2OΪdz��ɫ���壬ʵ�����г��Է���мΪԭ�����Ʊ����䲽�����£�
����1 ������м����̼������Һ����г����ۣ������Һ�壬��ˮϴ����м��
����2 ����������м�м��������3mol/L H2SO4��Һ����60������ʹ�䷴Ӧ�����ٲ������壬���ȹ��ˣ���FeSO4��Һ��
����3 ������FeSO4��Һ�м��뱥��(NH4)2SO4��Һ��������һϵ�в�������õ���������茶��塣
��ش��������⣺
(1)�ڲ���1�У�������������õ��IJ���������___________________________������������ţ�
��©�� �ڷ�Һ©�� ���ձ� �ܹ��ƿ ������̨ ������ �߾ƾ���
(2)�ڲ���3�У���һϵ�в���������Ϊ_____________________��_______________________���ˡ�
(3)ʵ��������18mol/L H2SO4������240mL 3mol/L H2SO4��Һ����Ҫ��ȡ________mLŨ���ᣬʵ��ʱ�����в��������������ҺŨ��ƫ�͵���__________________��(����ĸ)
a.����ƿ�ڱڸ���ˮ���δ���ﴦ�� b.δ��ȴ������ֱ��ת��������ƿ��
c.��ˮʱ�����̶��ߺ��ֵ��� d.����ʱ���ӿ̶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ����д�����˵����ȷ����(����)
A. CH4(g)��2O2(g)===CO2(g)��2H2O(l)����H����890 kJ
B. C(s)��![]() O2(g)===CO(g)����H����101.5 kJ��mol��1���÷���ʽ�Ħ�H�ɱ�ʾ̼��ȼ����
O2(g)===CO(g)����H����101.5 kJ��mol��1���÷���ʽ�Ħ�H�ɱ�ʾ̼��ȼ����
C. 2 mol����ȼ�յ�ˮ��������484 kJ����H2O(g)===H2(g)��![]() O2(g) ��H����242 kJ��mol��1
O2(g) ��H����242 kJ��mol��1
D. Ba(OH)2(aq)��H2SO4(aq)===BaSO4(s)��2H2O(l)����H����2a kJ��mol��1�����κ�ǿ���ǿ����кͷ�Ӧ����1 mol H2O(l)�ķ�Ӧ�Ⱦ�Ϊ��a kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A. 1.00mol NaCl���6.02��1023��NaCl����
B. 1.00mol NaCl��,����Na+��������������Ϊ8��6.02��1023
C. ������1.00L ,1.00mol.L-1��NaCl��Һ���ɽ�58.5g NaCl����1.00Lˮ��
D. ���58.5g���ڵ�NaCl���ܲ���22.4L��������״������23.0g������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�Ϊ��������Ԫ�������ڱ��е�λ�ã�
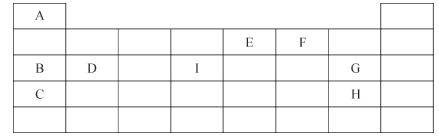
��ش��������⣺
(1)IԪ�ص�λ���ǵ� ________���ڣ���______�塣
(2)C��B��D ����Ԫ�صĽ�������ǿ������˳��Ϊ___________________(��Ԫ�ط���)��
(3)E��F����Ԫ�ض�Ӧ������⻯����ȶ��ԣ�________________ (�ѧʽ)��
(4)C�ĵ�����ϡ���ᷴӦ�����ӷ���ʽΪ_________________________ ��
(5)G �ĵ�������ͨ��H��C�γɻ������ˮ��Һ�У�д���÷�Ӧ�Ļ�ѧ����ʽ��______
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com