
关于浓度均为0.1 mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是 ( )
A.水电离出的c(H+):②>①
B.c(NH4+):③>①
C.①和②等体积混合后的溶液:c(H+) = c(OH- ) + c(NH3·H2O)
D.①和③等体积混合后显碱性,c(NH4+)>c(Cl-)>c(NH3·H2O )
科目:高中化学 来源:2016-2017学年浙江省杭州市五县七校高二上期中化学试卷(解析版) 题型:选择题
短周期元素W、X、Y、Z 的原子序数依次增大,W的单质是空气中体积分数最大的气体,W与Y最外层电子数之和为X最外层电子数的2倍,X、Y、Z简单离子的电子层结构相同,Z最外层电子数等于最内层电子数。下列说法正确的是
A. 元素非金属性由强到弱的顺序:W、Y、X
B. 离子半径由大到小的顺序:X、Y、Z
C. W的简单气态氢化物比Y的简单气态氢化物稳定
D. WX与ZX中的化学键类型相同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省天门市三校高一上学期期中化学试卷(解析版) 题型:选择题
在强碱的无色溶液中,下列各组离子能大量共存的是( )
A. K+、Na+、NO3-、Br- B.Na+、NH4+、NO3-、Cl-
C.K+、Na+、HCO3- 、NO3- D.K+、Cu2+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省天门市三校高二上学期期中化学试卷(解析版) 题型:填空题
(1)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈 (填“酸性”、“中性”或“碱性”,下同),溶液中c(Na+) c(CH3COO--)(填“>”、“=”或“<”,下同)。
(2)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中c(Na+) = c(CH3COO--),则混合后溶液呈 ,醋酸体积 氢氧化钠溶液体积。
(3)常温下,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 ,溶液中c(Na+) c(CH3COO--)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省天门市三校高二上学期期中化学试卷(解析版) 题型:选择题
下列叙述正确的是( )
A.纯锌与稀硫酸反应时,加少量CuSO4溶液,可使反应速率加快
B.甲烷和氧气以及KOH溶液构成的新型燃料电池中,负极上发生的反应为CH4+8OH-+8e- =CO2+6H2O
C.把铜片和铁片紧靠在一起浸入稀H2SO4中,铁片表面出现气泡
D.把铜片插入FeCl3溶液中,在铜片表面出现一层铁
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省天门市三校高二上学期期中化学试卷(解析版) 题型:选择题
下列关于电解质溶液的叙述中正确的是( )
A.Na2CO3、NaHCO3两种盐溶液中,离子种类不相同
B.使用pH试纸前要先将其润湿
C.物质的量浓度相同的NH4Cl和NH4HSO4两种溶液中,c(NH4+)前者小于后者
D.某次酸碱中和滴定实验读出标准液的体积为16.8 mL
查看答案和解析>>
科目:高中化学 来源:2017届湖北省老河口市高三10月月考化学卷(解析版) 题型:选择题
将 4 mol A 气体和 2 mol B 气体在 2 L 的容器中混合并在一定条件下发生如下反应:2A(气) + B(气)  2C(气)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:① 用物质 A 表示的反应的平均速率为 0.3 mol·L-1·s-1 ② 用物质 B 表示的反应的平均速率为 0.6 mol·L-1·s-1 ③2 s 时物质 B 的浓度为 0.7 mol·L-1 ④2 s 时物质 A 的转化率为70% 其中正确的是( )
2C(气)若经 2 s(秒)后测得 C 的浓度为 0.6 mol·L-1 ,现有下列几种说法:① 用物质 A 表示的反应的平均速率为 0.3 mol·L-1·s-1 ② 用物质 B 表示的反应的平均速率为 0.6 mol·L-1·s-1 ③2 s 时物质 B 的浓度为 0.7 mol·L-1 ④2 s 时物质 A 的转化率为70% 其中正确的是( )
A.①③ B.①④ C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源:2017届湖北省老河口市高三10月月考化学卷(解析版) 题型:选择题
常温下,某无色溶液能与铝反应放出氢气,该溶液中一定能大量存在的离子组是:( )
A. Na+、Cl-、K+、SO42-  B.Mg2+、NH4+、SO42-、Cl-
B.Mg2+、NH4+、SO42-、Cl-
C. Na+、K+、MnO4-、SO42- D.Na+、K+、CO32-、NO3-
查看答案和解析>>
科目:高中化学 来源:2017届安徽省六校教育研究会高三上第一次联考化学卷(解析版) 题型:填空题
某工厂用回收钒渣(含VOSO4、K2SO4、SiO2))制取V2O5时工艺流程如下:
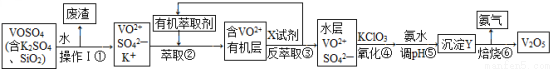
请回答下列问题:
(1)操作I的名称 ,①中产生废渣的主要成分是 。
(2)己知:VOSO4(水层)+2HA(有机层) VOA2(有机层)+H2SO4(水层)。步骤②中必须加入适量碱,其原因是 ;步骤③中反萃取所用的试剂X为 。
VOA2(有机层)+H2SO4(水层)。步骤②中必须加入适量碱,其原因是 ;步骤③中反萃取所用的试剂X为 。
(3)步骤④中的反应的离子方程式:□ClO3—+□VO2++□H+=□VO3++□ +□
(4)沉淀Y的摩尔质量为598g·mol—1,且仅含有四种元素。取59.8g沉淀Y的样品充分焙烧,得到产品54.6g,将产生的气体通过足量碱石灰,碱石灰增重1.8g,剩余的气体再通入稀硫酸被完全吸收。通过计算确定沉淀Y的化学式为 。
(5)钒沉淀率和溶液pH之间关系如下
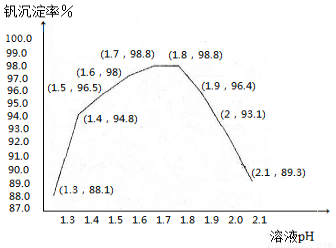
⑤中加入氨水,调节溶液的最佳pH为 ;若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)< 。(己知:25℃时,Ksp[Fe(OH)3]=2.6×l0—39)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com