
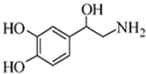
| A. | 该有机物的分子式是C8H10NO3 | |
| B. | 1mol该有机物最多能与2molBr2发生反应 | |
| C. | 该有机物不能与Na2CO3溶液反应 | |
| D. | 该有机物既能与盐酸反应,又能与氢氧化钠溶液反应 |
分析 A.根据结构简式确定分子式;
B.苯环上酚羟基邻对位氢原子能和溴发生取代反应;
C.该有机物中含有酚羟基,能和碳酸钠反应;
D.该物质中含有酚羟基和氨基,具有酸性和碱性.
解答 解:A.由结构简式可知分子式为C8H11NO3,故A错误;
B.苯环上酚羟基邻对位H原子能被溴原子取代,1mol去甲肾上腺素最多能与3mol Br2发生取代反应,故B错误;
C.该有机物中含有酚羟基,能和碳酸钠反应生成酚钠和碳酸氢钠,故C错误;
D.该物质中含有酚羟基和氨基,具有酸性和碱性,能和氢氧化钠、稀盐酸反应,故D正确;
故选D.
点评 本题考查有机物结构和性质,为高频考点,侧重考查酚、氨基性质,明确官能团及其性质关系是解本题关键,注意酚羟基能和碳酸钠反应但不能和碳酸氢钠反应,为易错题.


科目:高中化学 来源: 题型:解答题
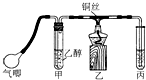 利用如图装置进行乙醇的催化氧化实验并制取乙醛(试管丙中用水吸收产物).
利用如图装置进行乙醇的催化氧化实验并制取乙醛(试管丙中用水吸收产物).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
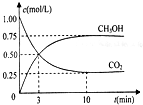 CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标.
CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2FeO4消毒、杀菌时得到的Fe3+可以净水,Fe3+能产生净水物质的原因是:Fe3++3H2O?Fe(OH)3(胶体)+3H+ | |
| B. | 工业上可用FeCl3、NaOH、NaClO三种物质反应制得Na2FeO4,化学方程式为:2FeCl3+10NaOH+3NaClO═2 Na2FeO4+9NaCl+5H2O | |
| C. | Na2FeO4在酸性溶液中不稳定,与水反应生成Fe3+和O2,离子方程式为:4FeO42-+10H2O═4Fe3++20OH-+3O2↑ | |
| D. | 工业上可用铁做阳极,电解浓NaOH溶液的方法制Na2FeO4,阳极的电极反应为:Fe-6e-+8OH-═FeO42-+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 绿色化学的核心是从源头上消除工业生产对环境的污染 | |
| B. | “硫黄姜”又黄又亮,可能是在用硫黄熏制的过程中产生的SO2所致 | |
| C. | 铁在潮湿的空气中放置,易发生化学腐蚀而生锈 | |
| D. | 华裔科学家高琨在光纤传输信息领域中取得突破性成就,光纤的主要成分是高纯度的二氧化硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
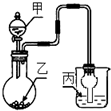 用如图装置进行实验,甲逐滴加入到固体乙中,如表说法正确的是( )
用如图装置进行实验,甲逐滴加入到固体乙中,如表说法正确的是( )| 选项 | 液体甲 | 固体乙 | 溶液丙 | 丙中现象 |
| A | CH3COOH | NaHCO3 | 苯酚钠 | 无明显现象 |
| B | 浓HCl | KMnO4 | 紫色石蕊 | 最终呈红色 |
| C | 浓H2SO4 | Na2SO3 | 品红 | 红色变无色 |
| D | 浓H2SO4 | Cu | 氢硫酸 | 溶液变浑浊 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
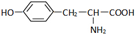 ,其与过量的NaOH溶液反应的化学方程式是
,其与过量的NaOH溶液反应的化学方程式是 +2NaOH→
+2NaOH→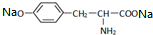 +2H2O.
+2H2O.
 +HBr→
+HBr→ .
. +Br2$\stackrel{红磷}{→}$
+Br2$\stackrel{红磷}{→}$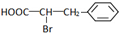 +HBr.
+HBr.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com