
解析:要确认是否含有上述粒子,实质上是检验Fe2+、![]() 、
、![]() 和H2O,H2O可从晶体受热有液体生成说明,其他离子可根据各自检验方法检出。
和H2O,H2O可从晶体受热有液体生成说明,其他离子可根据各自检验方法检出。
答案:(1)检查水的存在:取少量(NH4)2Fe(SO4)2·6H2O放入试管,用酒精灯加热。在试管口有液体生成,说明(NH4)2Fe(SO4)2·6H2O中含有结晶水。
(2)在检验其他离子前,要先将试样配成溶液,取少量(NH4)2Fe(SO4)2·6H2O配成溶液,溶液呈淡绿色,配制过程中,没有沉淀或气体产生,通过观察溶液的颜色,可以推断在(NH4)2Fe(SO4)2·6H2O中含有Fe2+。然后在三支试管中分别加入少量试样溶液。
①在第一支试管中滴入2滴KSCN溶液,溶液不显红色,再向这支试管中加入几滴新配制的氯水,溶液的颜色变为红色,这说明有Fe3+存在,从而说明在原溶液中有Fe2+存在,这是因为Fe2+被氯水氧化为Fe3+,Fe3+和SCN-反应生成血红色[Fe(SCN)]2+。
②在第二支试管中加入浓NaOH溶液并加热,且在试管口用湿润的红色石蕊试纸检验。红色的石蕊试纸变蓝,说明有NH3生成,确定在(NH4)2Fe(SO4)2·6H2O中含有![]() 。
。
③向第三支试管中滴入几滴HCl,无明显变化,然后加入BaCl2溶液,有白色沉淀生成,说明在溶液中有![]() 存在。
存在。
通过上述实验,可确定(NH4)2Fe(SO4)2·6H2O的成分中有Fe2+、![]() 、
、![]() 和H2O。
和H2O。


科目:高中化学 来源: 题型:阅读理解
| 实验序号 | 双氧水体积 | 催化剂 | 待测数据 |
| a | 15mL | 无 | |
| b | 15mL | 0.5g CuO | |
| c | 15mL | 0.5g MnO2 |
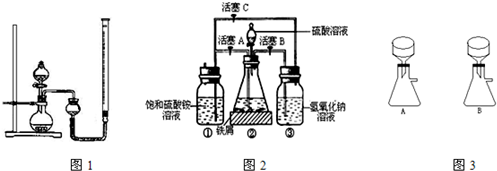
- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 试样 | 所加试剂 | 实验现象 |
| 第一份试液 | 滴加适量的淀粉KI溶液 | 呈蓝色 |
| 第二份试液 | 滴加用盐酸酸化的BaCl2溶液 | 有白色沉淀 |
| 第三份试液 | 滴加NaOH溶液,加热,加入的NaOH溶液体积(V)与生成的沉淀、产生的气体(n)的关系如图 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
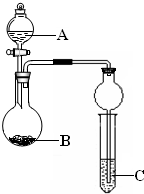 某同学设计了图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请回答:
某同学设计了图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com