
【题目】常温下,下列各组离子在相应的条件下能大量共存的是( )
A.由水电离产生的c(H+)=1×10-10molL-1的溶液中:NO3-、Fe2+、Na+、SO42-
B.![]() =10-10molL-1的溶液中:NH4+、I-、Cl-、K+
=10-10molL-1的溶液中:NH4+、I-、Cl-、K+
C.![]() =1×106的溶液中:K+、Na+、Cl-、HCO3-
=1×106的溶液中:K+、Na+、Cl-、HCO3-
D.惰性电极电解AgNO3后的溶液中:SO32-、K+、Na+、S2-
【答案】B
【解析】
A.由水电离产生的c(H+)=1×10-10molL-1的溶液可能是碱性溶液,也可能是酸性溶液。在酸性溶液中,H+、NO3-和Fe2+发生氧化还原不能大量共存,在碱性溶液中,Fe2+和OH-反应生成Fe(OH)2,不能大量共存,A不符合题意;
B.![]() =10-10molL-1<10-7 molL-1,其溶液为酸性溶液,NH4+、I-、Cl-、K+不生成气体,不产生沉淀,也不生成水,可以大量共存,B符合题意;
=10-10molL-1<10-7 molL-1,其溶液为酸性溶液,NH4+、I-、Cl-、K+不生成气体,不产生沉淀,也不生成水,可以大量共存,B符合题意;
C.![]() =1×106的溶液为碱性溶液,HCO3-与OH-反应生成CO32-和H2O,不能大量共存,C不符合题意;
=1×106的溶液为碱性溶液,HCO3-与OH-反应生成CO32-和H2O,不能大量共存,C不符合题意;
D.用惰性电极电解AgNO3溶液,阴极Ag+放电,阳极溶液中的OH-放电,总反应方程式为4AgNO3+2H2O![]() 4Ag+O2↑+4HNO3,溶液中含有HNO3,则SO32-和S2-会与HNO3发生氧化还原,不能大量共存,D不符合题意。
4Ag+O2↑+4HNO3,溶液中含有HNO3,则SO32-和S2-会与HNO3发生氧化还原,不能大量共存,D不符合题意。
答案选B。


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:
【题目】室温时,向 20 mL 0.1 mol·L 1 的两种酸 HA、HB 中分别滴加 0.1 mol·L 1NaOH 溶液, 其 pH 变化分别对应下图中的Ⅰ、Ⅱ。下列说法不正确的是

A.向 NaA 溶液中滴加 HB 可产生 HA
B.a点,溶液中微粒浓度:c(A-) > c(Na+) > c(HA)
C.滴加 NaOH 溶液至 pH=7 时,两种溶液中 c(A-)= c(B-)
D.滴加 20 mL NaOH 溶液时,Ⅰ中 H2O 的电离程度大于Ⅱ中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2分解速率受多种因素影响。实验测得 70 ℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是
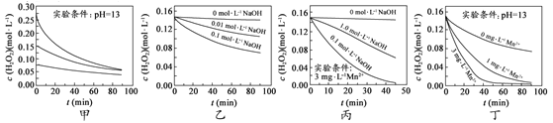
A.图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B.图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
C.图丙表明,少量Mn 2+存在时,溶液碱性越强,H2O2分解速率越快
D.图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2H4(阱)可作制药的原料,也可作火箭的燃料。已知热化学方程式:
反应I:N2H4(g)![]() N2(g)+2H2(g) △H1>0;
N2(g)+2H2(g) △H1>0;
反应II:N2(g)+3H2(g)![]() 2NH3(g) △H2<0;
2NH3(g) △H2<0;
反应III:N2H4(g)+H2(g)![]() 2NH3(g) △H。
2NH3(g) △H。
下列推断不正确的是( )
A.N2H4断裂共价键需要吸收能量
B.反应I中1molN2H4(g)的能量小于1molN2(g)和2molH2(g)的总能量
C.反应II中正反应的活化能大于逆反应的活化能
D.△H=△H1+△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在T℃下,向装有5mL0.005mol.L-1FeCl3溶液的试管中加入5mL0.01mol·L-1KSCN溶液,发生如下反应:FeCl3+3KSCN![]() Fe(SCN)3+3KCl,溶液呈血红色。下列叙述正确的是( )
Fe(SCN)3+3KCl,溶液呈血红色。下列叙述正确的是( )
A.升高温度,逆反应速率减小
B.加入Fe2(SO4)3固体,溶液血红色加深
C.加入KCl固体,溶液血红色加深
D.增大压强,溶液血红色加深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是铜锌原电池示意图。图2中,x轴表示实验时流入正极的电子的物质的量,y轴表示( )
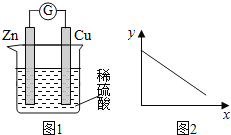
A. 铜棒的质量 B. c(Zn2+) C. c(H+) D. c(SO42-) -
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式硫酸铁[Fe(OH)SO4]是重要的化工原料,工业上利用废铁屑(含少量氧化铝、 氧化铁等)生产碱式硫酸铁的工艺流程如下:
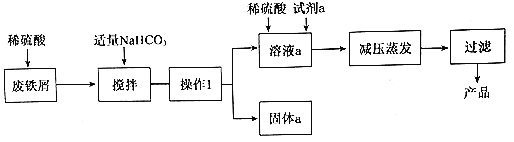
已知:Ksp[Fe(OH)3]=2.6×10-39 Ksp[Fe(OH)2]=4.9×10-17 Ksp[Al(OH)3]=8×10-32(单位略)
(1)工业生产中,常将废铁块处理为废铁屑,其目的是_______;用稀硫酸处理废铁屑的过程中______个氧化还原反应发生。
(2)加入碳酸氢钠后,发生反应的主要离子方程式为_______。
(3)若要使沉淀完全(一般认为离子浓度小于10-5 molL-1即为沉淀完全),溶液的pH为________;此溶液中亚铁离子的物质的量浓度不高于_____molL-1才不会生成沉淀。
(4)从环保、产品纯度角度分析.试剂a最好选择下列物质中的_____(填字母代号)。
A NaClO B KNO3 C H2O2 D KMnO4
(5)若搅拌过程中NaHCO3过量,会产生FeCO3沉淀和大量气泡,若将NaHCO3改为 Na2CO3过量时产生的沉淀为FeCO3和Fe(OH)2的混合物,试解释混合物中有Fe(OH)2的原因___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中,溶质的物质的量浓度不是1 mol/L的是( )
A. 10 g NaOH固体溶解在水中配成250 mL溶液
B. 将80 g SO3溶于水并配成1 L的溶液
C. 将0.5 mol/L的NaNO3溶液100 mL加热蒸发掉50 g水的溶液
D. 标况下,将22.4 L氯化氢气体溶于水配成1 L溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的反应路线及所给信息填空:

(1)A的名称是___________。
(2)填写以下反应的反应类型:①____________;④____________。
(3)物质C中含有的官能团的名称是______________。
(4)反应④的反应试剂及反应条件_______________。
(5)反应②的化学方程式为__________________,反应③的化学方程式为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com