
(16分)下图是某化工厂对海水资源的综合利用的示意图。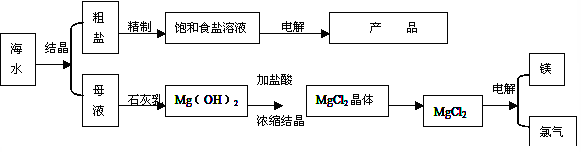
(1)目前国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是: (填物理变化、化学变化)
(2)工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”。电解饱和食盐水的离子方程式为: 。阳极产生气体的如何检验 。利用电解所得气体制36.5%的浓盐酸100t,最少需要消耗食盐: t。
(3)分离出粗盐的母液中含有Mg2+,从图中可看出对母液进行一系列的加工可制得金属镁。
①在母液中加入石灰乳所起的作用是: 。
②从充分利用当地海洋化学资源,就地取材,经济效益的角度考虑,生产生石灰的原料可是: 。
③电解熔融氯化镁的化学方程式是: 。
④氮气和氩是两种化学性质相对稳定的气体,都可用做白炽灯的填充气体。但工业上冷却电解无水氯化镁所得的镁蒸气时,却选择稀有气体氩。试用化学反应方程式解释不选用氮气的原因: 。
(1)物理变化 (2)2Cl- +2H2O 2OH-+H2 ↑+Cl2 ↑ 湿润的淀粉碘化钾试纸 58.5
2OH-+H2 ↑+Cl2 ↑ 湿润的淀粉碘化钾试纸 58.5
(3)①将镁离子转化为沉淀而分离 ②贝壳 ③MgCl2 Mg +Cl2 ↑
Mg +Cl2 ↑
④3Mg +N2 Mg3N2
Mg3N2
解析试题分析:(1)蒸馏法是利用物质的沸点不同进行分离两种互溶的液体的方法,所以蒸馏法是物理变化。
(2)电解饱和食盐水的离子方程式:2Cl- +2H2O 2OH-+H2 ↑+Cl2 ↑。阳极产生的是Cl2,检验Cl2的方法是用湿润的淀粉碘化钾试纸,当试纸变蓝说明有Cl2生成。利用电解所得气体制的36.5%的浓盐酸100t,则需要HCl 36.5t,因此需要NaCl 58.5t。
2OH-+H2 ↑+Cl2 ↑。阳极产生的是Cl2,检验Cl2的方法是用湿润的淀粉碘化钾试纸,当试纸变蓝说明有Cl2生成。利用电解所得气体制的36.5%的浓盐酸100t,则需要HCl 36.5t,因此需要NaCl 58.5t。
(3)①Mg2+可以和OH-反应生成Mg(OH)2,所以在母液中加入石灰乳是将镁离子转化为沉淀而分离。②海边的贝壳主要是CaCO3,CaCO3受热分解得到CaO。③电解熔融氯化镁的化学方程式是:MgCl2 Mg +Cl2 ↑。④氮气可以和镁反应:3Mg +N2
Mg +Cl2 ↑。④氮气可以和镁反应:3Mg +N2 Mg3N2。
Mg3N2。
考点:海水综合利用
点评:本题综合性较强,考查的知识点比较基础简单。


科目:高中化学 来源: 题型:

| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
(16分)我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是某化工厂对海水资源综合利用的示意图:
请根据以上信息回答下列问题:
I.(1)写出N的化学式和B的名称:N 、B 。
(2)写出反应②的化学方程式,并标出其电子转移的方向和数目:
(3)写出反应③的离子方程式: ,
Ⅱ.粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:①盐酸 ②氯化钡溶液
③氢氧化钠溶液 ④碳酸钠溶液,以上试剂添加的顺序可以为 。
A. ②③④① B.③④②① C.④③②① D.③②④①
Ⅲ.提取粗盐后剩余的海水(母液)中,可用来提取Mg和Br2。
(1)若用来提取Mg,根据上述提取Mg的流程,没有涉及到的反应类型是 。
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
(2)若用来提取Br2,反应⑥所用的气态氧化剂的寻找货源的设想,其中合理的是 。
A.从外地购买 B.在当地新建生产厂
C.从本厂生产烧碱处循环 D.从本厂生产镁单质处循环
流程⑦将溴单质从混合物中分离出来是基于溴单质具有 性。
(3)母液用来提取Mg和Br2先后顺序,甲乙两位工程师有不同观点:
甲:母液先提取Mg,后提取Br2
乙:母液先提取Br2,后提取Mg
请你判断哪个更合适? (填“甲”或“乙”),理由是 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省台州市高一上学期期末考试化学试卷 题型:实验题
(16分)我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是某化工厂对海水资源综合利用的示意图: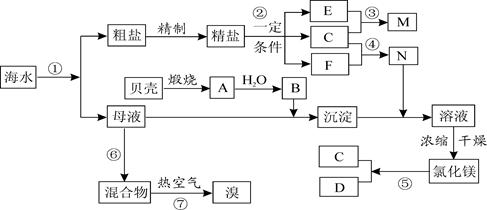
请根据以上信息回答下列问题:
I.(1)写出N的化学式和B的名称:N 、B 。
(2)写出反应②的化学方程式,并标出其电子转移的方向和数目:
(3)写出反应③的离子方程式: ,
Ⅱ.粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:①盐酸 ②氯化钡溶液
③氢氧化钠溶液 ④碳酸钠溶液,以上试剂添加的顺序可以为 。
A. ②③④① B. ③④②① C. ④③②① D. ③②④①
Ⅲ.提取粗盐后剩余的海水(母液)中,可用来提取Mg和Br2。
(1)若用来提取Mg,根据上述提取Mg的流程,没有涉及到的反应类型是 。
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
(2)若用来提取Br2,反应⑥所用的气态氧化剂的寻找货源的设想,其中合理的是 。
A.从外地购买 B.在当地新建生产厂
C.从本厂生产烧碱处循环 D.从本厂生产镁 单质处循环
单质处循环
流程⑦将溴单质从混合物中分离出来是基于溴单质具有 性。
(3)母液用来提取Mg和Br2先后顺序,甲乙两位工程师有不同观点:
甲:母液先提取Mg,后提取Br2
乙:母液先提取Br2,后提取Mg
请你判断哪个更合适? (填“甲”或“乙”),理由是 。
(填“甲”或“乙”),理由是 。
查看答案和解析>>
科目:高中化学 来源:2015届福建省高一上学期期末考试化学试卷(解析版) 题型:填空题
(12分)海水是取之不尽用之不竭的化学资源,从海水中可提取多种化工原料,下图是某化工厂对海水资源综合利用的示意图。
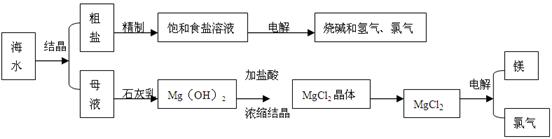
(1)请写出电解食盐水的化学方程式
(2)母液中含有K+、Na+ 、Mg2+等阳离子,从图中可看出对母液进行一系列的加工可制得金属镁。
①石灰乳是生石灰与水作用形成的化合物,从充分利用当地海洋化学资源,提高生产与经济效益的角度考虑,生产生石灰的主要原料是
②电解熔融氯化镁的化学方程式是
③电解无水氯化镁所得的镁蒸气在特定的环境里冷却后可得固态的金属镁,下列物质中可以用作镁蒸气的冷却剂的是(填写代号)
A. H2 B. CO2 C.空气 D. Ar
(3)在该化工厂中,海水提取氯化钠后的母液经过提取氯化镁后又形成了新的母液,向新母液中加入氯气,又制取了重要的化工原料溴单质
①生成溴单质的化学反应的离子方程式是 ,其中氧化剂是
工业生产中将溴单质从混合物中分离出来应采用 (填实验方法)
②以下是对生产溴单质所用的氯气寻找货源的设想,其中合理的是 (填写代号)
A.从外地购买 B.在当地新建生产厂
C.从本厂生产烧碱处循环 D.从本厂生产镁单质处循环
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com