
 的名称是2,2,4,5-四甲基-3,3-二乙基己烷
的名称是2,2,4,5-四甲基-3,3-二乙基己烷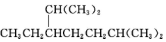 的名称为2,6-二甲基-3-乙基庚烷
的名称为2,6-二甲基-3-乙基庚烷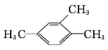 的名称是1,2,4-三甲苯
的名称是1,2,4-三甲苯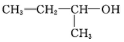 的名称是2-丁醇
的名称是2-丁醇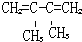 .
. 分析 (1)烷烃命名时,选最长的碳链为主链,从离主链近的一端给主链上的碳原子进行编号,据此分析;
(2)烷烃命名时,选最长的碳链为主链,从离主链近的一端给主链上的碳原子进行编号,据此分析;
(3)苯的同系物命名时,应从简单的侧链开始、按顺时针或逆时针给苯环上的碳原子进行标号,使侧链的位次和最小,据此分析;
(4)醇命名时,应选择含官能团的最长的碳链为主链,从离官能团近的一端给主链上的碳原子进行编号,并标出官能团的位置;
(5)根据二烯烃命名时,选择的是含官能团的最长的碳链为主链,从离官能团近的一端给主链上的碳原子进行编号,并标出官能团的位置,根据名称书写结构简式;
解答 (1)烷烃命名时,选最长的碳链为主链,当有多条等长的碳链可选时,应选择支链多的为主链,故主链上有6个碳原子,故为己烷;从离支链近的一端给主链上的碳原子进行编号,当两端离支链一样近时,要从支链多的一端给主链编号,故在2号碳原子上有2个甲基,在4号和5号碳原子上各有一个甲基,在3号碳原子上有2个乙基,故名称为
2,2,4,5-四甲基-3,3-二乙基己烷,故答案为:2,2,4,5-四甲基-3,3-二乙基己烷;
(2)烷烃命名时,选最长的碳链为主链,当有多条等长的碳链可选时,应选择支链多的为主链,故主链上有7个碳原子,故为庚烷;从离支链近的一端给主链上的碳原子进行编号,当两端离支链一样近时,要从支链多的一端给主链编号,故在2号和6号碳原子上各有一个甲基,在3号碳原子上有一个乙基,故名称为2,6-二甲基-3-乙基庚烷,故答案为:2,6-二甲基-3-乙基庚烷;
(3)苯的同系物命名时,应从简单的侧链开始、按顺时针或逆时针给苯环上的碳原子进行标号,使侧链的位次和最小,故三个甲基分别在苯环的1号、2号和4号位上,故名称为1,2,4-三甲苯,故答案为:1,2,4-三甲苯;
(4)醇命名时,应选择含官能团的最长的碳链为主链,故主链上有4个碳原子,故为丁醇;从离官能团近的一端给主链上的碳原子进行编号,故-OH在2号碳原子上,并标出官能团的位置,故名称为2-丁醇,故答案为:2-丁醇;
(5)二烯烃命名时,选择的是含官能团的最长的碳链为主链,故可知主链上有4个碳原子,且是从离官能团近的一端给主链上的碳原子进行编号,并标出官能团的位置,故在1号和2号碳原子间、3号和4号碳原子间各有一条碳碳双键,在2号和3号碳原子上各有一个甲基,故结构简式为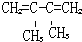 ,故答案为:
,故答案为: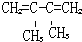 .
.
点评 本题考查了有机物的命名和根据名称来书写结构简式,题目难度不大,注意掌握有机物的命名规则,含官能团的有机物在命名时官能团是首要的考虑对象.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 离子方程式 | 评价 |
| A | 将少量的Fe3O4溶解在过量的稀HNO3中Fe3O4+8H+=Fe2++2Fe3++4H2O | 正确,Fe2+与Fe3+物质的量之比为1:2 |
| B | Ba(HCO3)2溶液与足量的NaOH溶液反应Ba2++HCO3 -+OH-═BaCO3↓+H2O | 正确;酸式盐与碱反应生成正盐和水 |
| C | 过量SO2通入到NaClO溶液中:SO2+H2O+ClO-═HClO+HSO3- | 正确;说明酸性:H2SO3强于HClO |
| D | 1mol/L的NaAlO2溶液和2.5mol/L的HCl溶液等体积互相均匀混合:2AlO2-+5H+═Al3++Al(OH)3↓+H2O | 正确;AlO2-与Al(OH)3消耗的H+的物质的量之比为2:3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
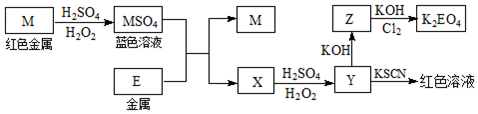
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去KC1中的K2CO3,可先加入过量的BaCl2溶液,待沉淀完全后再过滤、洗涤,取滤液蒸发即可 | |
| B. | 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 | |
| C. | 用冷却结晶的方法提纯含有少量KC1的KNO3 | |
| D. | 通过点燃可除去CO2中混有的CO气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
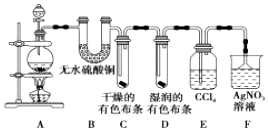
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
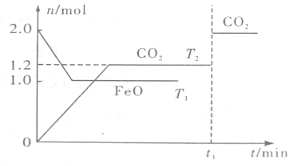
| A. | 平衡前,随着反应的进行,容器内气体的相对分子质量始终不变 | |
| B. | 平衡时,其他条件不变,取出适当铁可提高CO的转化率 | |
| C. | 该反应的△H<0,T1>T2 | |
| D. | 当反应进行到t1时刻仅改变一个条件,可能是通入了氮气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑨ | ⑦ | ⑧ |
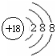 .
.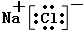
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com