

分析 生石灰容易吸收水生成氢氧化钙;
蒸馏是分离沸点不同,相互溶解的液体,过滤分离固体与液体的操作;
蒸馏时,冷凝水与蒸汽流向逆向冷凝效果最佳;过滤时分液漏斗液面低于滤纸边缘;
白色的无水硫酸铜与水反应生成蓝色晶体;
解答 解:(1)生石灰容易吸收水生成氢氧化钙,CaO与水反应后,增大与乙醇的沸点差异,沸点不同的相互溶解的液体,应选择蒸馏操作分离;
故答案为:生石灰;蒸馏;
(2)①蒸馏时,冷凝水与蒸汽流向逆向冷凝效果最佳,应该下口进上口出,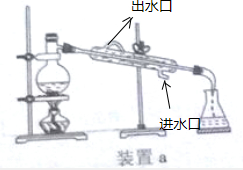 ;
;
过滤时分液漏斗液面低于滤纸边缘, ;
;
故答案为: ;
; ;
;
②分离酒精与氢氧化钙混合物应选择蒸馏操作选择a装置;
故答案为:a;
(3)白色的无水硫酸铜与水反应生成蓝色晶体,可以用无水硫酸铜检验酒精中是否含有水;
故答案为:无水硫酸铜.
点评 本题考查了物质分离的方法,熟悉蒸馏与过滤的原理是解题关键,注意蒸馏实验中温度计位置、冷凝水流向,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LH2O含有的分子数为NA个 | |
| B. | 通常状况下,NA 个CO2分子的体积为22.4L | |
| C. | 常温常压下,40gNaOH含有的钠离子个数为NA个 | |
| D. | 物质的量浓度为0.5mol/L的BaCL2溶液中,含有氯离子个数为NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ③⑤⑥ | C. | ②③⑥ | D. | ①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,则转移4NA个电子 | |
| B. | 含有NA个“Cu”微粒的CuO和Cu2S混合物质量为80g | |
| C. | 常温常压下,2.24L CO2和SO2混合气中氧原子数为0.2NA | |
| D. | 100mL0.1mol/L的NaCl溶液中,所含微粒总数为0.02NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 分类标准 | 能导电的物质 | 电解质 | 酸 |
| 属于该类的物质 |
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上学期期中化学试卷(解析版) 题型:填空题
氮及其化合物在工农业生产生活中应用广泛,请解决下列问题。
(1)硫酸铜溶液时白磷引起中毒的一种解毒剂:
P4+CuSO4+H2O Cu3P+H3PO4+H2SO4,若6molH3PO4生成,则被CuSO4氧化的P4的物质的量为 。
Cu3P+H3PO4+H2SO4,若6molH3PO4生成,则被CuSO4氧化的P4的物质的量为 。
(2)氮的化合物合成、应用及氮的固定一直是科学研究的热点。以CO2与NH3为原料合成化肥尿素的主要反应如下:
①2NH3(g)+CO2(g)=NH2CO2NH4(s);ΔH=-159.47 kJ·mol-1
②NH2CO2NH4(s)=CO (NH2)2(s)+H2O(g);ΔH=a kJ·mol-1
③2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g);ΔH=-86.98 kJ·mol-1
则a为 。
(3)右图表示使用新型电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制造出既能提供能量,同时又能实现氮固定的新型燃料电池。请写出该电池的正极反应式 。生产中可分离出的物质A的化学式为 。

(4)常温下,向0.1mol/L氨水中加入少许N2O5,使溶液中c(NH3·H2O):c(NH4+)=5:9,此时溶液的pH= .(25℃时,NH3·H2O的电离常数Kb=1.8×10-5)
(5)SiO2溶于氢氟酸后生成一种极强的二元酸和水,经分析该酸由3种元素组成,其中氟元素的质量分数为79.17%。请写出SiO2溶于氢氟酸的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上学期期中化学试卷(解析版) 题型:选择题
25℃时,下列各溶液中有关微粒的物质的量浓度关系正确的是
A.在0.1mol·L-1Na2S溶液中:2c(Na+)>c(S2-)>c(HS-)>c(OH-)
B.一定量的(NH4)2SO4与NH3·H2O混合所得的酸性溶液中:c(NH4+)<2c(SO42-)
C.向0.1mol·L-1盐酸与0.1mol·L-1K2CO3溶液等体积混合:
c(K+)>c(Cl-)>c(OH-)>c(HCO3-)>c(H+)
D.向0.1mol·L-1Na2CO3溶液和0.1mol·L-1NaHCO3溶液等体积混合:
c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三上学期月考一化学试卷(解析版) 题型:选择题
在100℃时,将0.40mol二氧化氮气体充入2L密闭容器中,每隔一段时间对该容器内的得到数据如下
时间(s) | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
下列说法中正确的是
A.反应开始20s内以二氧化氮表示的平均反应速率为0.00125mol·L-1·s-
B.80s时混合气体的颜色与60s时相同,比40s时的颜色深
C.80s时向容器中加入0.32mol氦气,同时将容器扩大为4L,则平衡将不移动
D.若起始投料为0.20molN2O4,相同条件下达平衡,则各组分含量与原平衡体系对应相等
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com