
| ������� | ��ʼʱ���������ʵ���/mol | ƽ��ʱ��Ӧ�е������仯 | ||
| N2 | H2 | NH3 | ||
| �� | 1 | 3 | 0 | �ų�����a kJ |
| �� | 2 | 3 | 0 | �ų�����b kJ |
| �� | 2 | 6 | 0 | �ų�����c kJ |
| A�� | N2��ת���ʣ��ڣ��٣��� | B�� | ���������ڷ�Ӧ��ƽ�ⳣ�����ۣ��٣��� | ||
| C�� | ƽ��ʱ����������������٣��� | D�� | �ų�������ϵ��2a��c��184.8 kJ |
���� A���ڵ�Ч�ڢ�ƽ��Ļ������ټ���1mol�����������ȣ�������ת���ʼ�С���۵�Ч�ڢ���ƽ��������ټ���3mol������ƽ�������ƶ�������ת���������۵�Ϊ�ڢ���ƽ�������ѹǿ����ƽ�������ƶ�������ת��������
B��ƽ�ⳣ��ֻ���¶��йأ������������ƽ�ⳣ����ȣ�
C���۵�Ϊ�ڢ���ƽ�������ѹǿ����ƽ�������ƶ������������������
D���۵�Ϊ�ڢ���ƽ�������ѹǿ����ƽ�������ƶ�����Ӧ��ת�������ʢ��з�Ӧ�ĵ������ʵ������ڢ��е�2�������ܷ�Ӧ������ȫת������Ӧ�ĵ���С��2mol��
��� �⣺A���ڵ�Ч�ڢ�ƽ��Ļ������ټ���1mol�����������ȣ�������ת���ʼ�С���۵�Ч�ڢ���ƽ��������ټ���3mol������ƽ�������ƶ��������ȣ�����ת���������۵�Ϊ�ڢ���ƽ�������ѹǿ����ƽ�������ƶ�������ת�������ʵ�����ת���ʢۣ��٣��ڣ���A����
B��ƽ�ⳣ����ֻ���¶��йص��������������ʵ�Ũ���أ��¶����ƽ�ⳣ����ȣ���B����
C���۵�Ϊ�ڢ���ƽ�������ѹǿ����ƽ�������ƶ���ƽ��ʱ����������������٣��ۣ���C����
D���۵�Ϊ�ڢ���ƽ�������ѹǿ����ƽ�������ƶ�����Ӧ��ת�������ʢ��з�Ӧ�ĵ������ʵ������ڢ��е�2�������ܷ�Ӧ������ȫת������Ӧ�ĵ���С��2mol�����Ȼ�ѧ����ʽ��֪��2mol������Ӧ�ų�����Ϊ184.8 kJ���ʷų�������ϵ��2a��c��184.8 kJ����D��ȷ��
��ѡ��D��
���� ���⿼�黯ѧƽ����㣬�ʺ����õ�Чƽ��˼���𣬹���ƽ�⽨����;���ǽ���Ĺؼ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ij��ɫ��Һ�м���AgNO3��Һ�ð�ɫ��������ϡ�����������ʧ����ԭ��Һһ������Cl-��CO32- | |
| B�� | ij��ɫ��Һ�еμ�BaCl2��Һ�ð�ɫ��������ϡ����������ܽ⣬��һ������SO42- | |
| C�� | ��ˮ������ʵ��ʱ��Ҫ����ƿ�ڼӼ�����ʯ�Է�ֹ���� | |
| D�� | ij��ɫ��Һ�еμ�CaCl2��Һ�ð�ɫ������������������������ɫ���壬��������ʹ����ʯ��ˮ����ǣ���ԭ��Һ��һ����CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ˮ��Ӧʵ��ʱ��ʣ����Ʋ����ٷ���ԭ�Լ�ƿ | |
| B�� | ����480mLNaOH��Һ��Ҫ����Ҫ������480mL����ƿ�����������ձ�����Ͳ�� | |
| C�� | ������ҩƷ�����������н��и��±��� | |
| D�� | ����������ȴˮ������һ�����¿ڽ�ˮ���Ͽڳ�ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
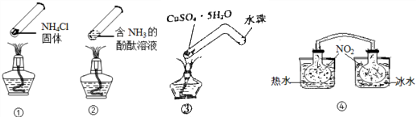
| A�� | ����ʱ�����ϲ��㼯�˹���NH4Cl��˵��NH4Cl������ | |
| B�� | ����ʱ������Һ��ɫ�䣬��ȴ���ָֻ�Ϊԭ������ɫ | |
| C�� | ����ʱ�����й�������ɫ��Ϊ��ɫ����ȴ���ָֻ�Ϊԭ������ɫ | |
| D�� | ���У���������ˮ�е�������������ɫ���˵������ʱ��Ӧ2NO2?N2O4���������ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{1}{4}$��$\frac{n��X��}{n��Y��}$��$\frac{3}{2}$ | B�� | $\frac{1}{4}$��$\frac{n��X��}{n��Y��}$��$\frac{1}{2}$ | C�� | $\frac{1}{4}$��$\frac{n��X��}{n��Y��}$��4 | D�� | $\frac{1}{2}$��$\frac{n��X��}{n��Y��}$��4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ҵ���Ի�����Ϊԭ���������ᣬ������Ҫ��һ���Ǵ������������б��ֺ��º�����������2SO2��g��+O2��g��?2SO3��g����H=-196.6kJ•mol-1
��ҵ���Ի�����Ϊԭ���������ᣬ������Ҫ��һ���Ǵ������������б��ֺ��º�����������2SO2��g��+O2��g��?2SO3��g����H=-196.6kJ•mol-1�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ�к���0.6NA��K+ | |
| B�� | 1L��Һ�к���K+��SO42-����Ϊ0.9NA | |
| C�� | ȡ��10mL����Һ�У�K+Ũ��Ϊ0.3mol/L | |
| D�� | 100mL��Һ�к���SO42-��ĿΪ0.6NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ�����Ʊ����� | |
| B�� | Ba��OH��2•8H2O������NH4Cl����ķ�Ӧ | |
| C�� | ���ȵ�ľ̿��CO2�ķ�Ӧ | |
| D�� | ��������������ĩ��Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com