
【题目】下列物质的分离方法不正确的是
A. 用过滤的方法除去食盐水中的泥沙 B. 用蒸馏的方法除去自来水中的氯离子
C. 用酒精萃取碘水中的碘 D. 用淘洗的方法从沙里淘金
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】如图表示不同温度下水溶液中c(H+)与c(OH﹣)的关系,下列判断正确的是( ) 
A.两条曲线上任意点均有c(H+)×c (OH﹣)=Kw
B.T<25
C.b点和c点pH均为6,溶液呈酸性
D.只采用升温的方式,可由a点变成d点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】油酸甘油酯(相对分子质量884)在体内代谢时可发生如下反应:
C57H104O6(s)+80O2(g)=57CO2(g)+52H2O(l)
已知燃烧1kg该化合物释放出热量3.8×104kJ,油酸甘油酯的燃烧热为( )
A.3.8×104kJmol﹣1
B.﹣3.8×104kJmol﹣1
C.3.4×104kJmol﹣1
D.﹣3.4×104kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去). A ![]() B
B ![]() C
C
(1)若A是一种黄色单质固体,则B→C的化学方程式为 .
(2)若A是一种活泼金属,C是淡黄色固体,试用化学方程式表示C与二氧化碳气体的反应 . 将C长期露置于空气中,最后将变成物质D,D的化学式为 . 现有D和NaHCO3的固体混合物10.0g,加热至质量不再改变,剩余固体质量为9.38g,D的质量分数为 .
(3)若C是红棕色气体,如图是实验室制取A气体的装置,请结合所学知识,回答下列问题: 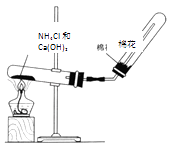
①试写出由A到B的化学方程式 .
②验证A是否已经收集满的方法是(任写一种).
③写出工业上制取A的化学方程式 .
④C与水反应可得到酸X,要使1molC恰好完全转化为X,需通入氧气的物质的量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1.12g铁粉加入2mol/L氯化铁溶液25mL中,充分反应后结果是( )
A.铁有剩余
B.往溶液中滴入无色KSCN溶液,显红色
C.Fe2+和Fe3+物质的量之比为6:1
D.氧化产物与还原产物的物质的量之比为2:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,在一定体积pH=12的Ba(OH)2溶液中逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11.若体积可以加和,则V(Ba(OH)2):V( NaHSO4)为( )
A.1:1
B.1:2
C.1:3
D.1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)将a mol钠和a mol铝一同投入m g足量水中,请用两个离子方程式表示有关生成H2的变化: . 该溶液的溶质质量分数为 .
(2)在标准状况下,22.4升的密闭容器中充入CO2和CO混合气体,其密度为10/7g/L,加入足量Na2O2充分振荡并不断用点火花点燃至完全反应,则容器中存在molO2 , molNa2CO3 .
(3)取一定量的镁铝合金,用足量盐酸溶解后,再加入过量的NaOH溶液,然后滤出沉淀物,加强热灼烧,最后得到白色粉末,干燥后称量,这些粉末与原合金的质量相等,则合金中铝的质量百分含量为 .
(4)已知2Fe2++Br2=2Fe3++2Br﹣ , 2Br﹣+Cl2=2Cl﹣+Br2 . 往100mLFeBr2溶液中缓慢通入2.24升氯气(标准状况),结果溶液中有三分之一的Br﹣被氧化成Br2 . 求原FeBr2的物质的量浓度 .
(5)部分氧化的Fe﹣Cu合金样品(氧化物为Fe2O3、CuO)共5.76g,经如图处理: 
根据题中条件计算V= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色废水中可能含有Fe3+、Al3+、Mg2+、Na+、NO3﹣、Cl﹣、SO42﹣离子中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作和有关现象如图: 
回答下列问题:
(1)焰色反应的操作步骤简记为洗、烧、蘸、烧、洗,洗铂丝的试剂是(写名称),若采用焰色反应检测K+时,观察火焰焰色时必须要透过观察.
(2)实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除烧杯、玻璃棒、托盘天平、量筒、药匙、胶头滴管,还缺少的仪器为 .
(3)实验③中沉淀量由A→B过程中所发生反应的离子方程式为 .
(4)经分析,该溶液中肯定存在的阳离子有 .
(5)现补充第④组实验:另取100mL废水,加入硝酸酸化,再滴入AgNO3溶液,未见白色沉淀生成,则该废水中一定存在的阴离子除SO42﹣还有 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com