
合理利用资源,降低碳的排放,实施低碳经济是今后经济生活主流方向。
⑴下列措施不利于有效减少二氧化碳排放的是 。
A.植树造林,保护森林,保护植被
B.加大对煤和石油的开采,并鼓励使用石油液化气
C.推广使用节能灯和节能电器,使用空调时夏季温度不宜设置过低,冬天不宜过高
D.倡导出行时多步行和骑自行车,建设现代物流信息系统,减少运输工具空驶率
⑵科学家致力于二氧化碳的“组合转化”技术研究,如将CO2和H2以1∶4比例混合通入反应器,适当条件下反应可获得一种能源。完成以下化学方程式:CO2+4H2 +2H2O。
+2H2O。
⑶CO2合成生产燃料甲醇(CH3OH)是碳减排的新方向。进行如下实验:某温度下在1 L的密闭容器中,充2 mol CO2和6 mol H2,发生:CO2(g)+3H2(g ) CH3OH(g)+H2O(g)能判断该反应已达化学反应限度标志的是 (填字母)。
CH3OH(g)+H2O(g)能判断该反应已达化学反应限度标志的是 (填字母)。
A.CO2百分含量保持不变
B.容器中H2浓度与CO2浓度之比为3:1
C.容器中混合气体的质量保持不变
D.CO2生成速率与CH3OH生成速率相等
现测得CO2和CH3OH(g)的浓度随时间变化如左下图所示。从反应开始到平衡,氢气的平均反应速率v(H2)= mol/(L·min)。


⑷CO在催化作用下也能生成甲醇:CO(g)+2H2(g)  CH3OH(g);已知密闭容器中充有10 mol CO与20 mol H2,CO的平衡转化率(α)与温度、压强的关系如右上图所示。
CH3OH(g);已知密闭容器中充有10 mol CO与20 mol H2,CO的平衡转化率(α)与温度、压强的关系如右上图所示。
①若A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tA tC(填“大于”、“小于”或“等于”)。
②若A、B两点表示在某时刻达到的平衡状态,此时在A点时容器的体积为VAL,则A、B两点时容器中,n(A)总︰n(B)总= 。
⑸以KOH为电解质的甲醇燃料电池总反应为:2CH3OH+3O2+4KOH = 2K2CO3+6H2O,通入甲醇的电极为燃料电池的负极,正极发生的电极反应式为 。
⑴B ⑵CH4 ⑶AD 0.375 ⑷①大于 ② 5:4 ⑸ O2+2H2O+4e—=4OH—
【解析】
试题分析:(1)A、植树造林,保护森林,保护植被,可以吸收CO2,减少CO2的排放,A正确;B、石油和煤等均是化石燃料,不可再生,因此加大对煤和石油的开采,并鼓励使用石油液化气是不正确的,B不正确;C、推广使用节能灯和节能电器,使用空调时夏季温度不宜设置过低,冬天不宜过高,有利于节能减排,C正确;D、倡导出行时多步行和骑自行车,建设现代物流信息系统,减少运输工具空驶率,有利于节能减排,D正确,答案选B。
(2)根据原子守恒可知,反应中另外一种生成物是甲烷,即CO2+4H2 CH4+2H2O。
CH4+2H2O。
(3)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,则A、CO2百分含量保持不变可以说明反应达到平衡状态,A正确;B、平衡时浓度不再发生变化,但各物质的浓度之间不一定相等或满足某种关系,因此容器中H2浓度与CO2浓度之比为3:1不能说明反应达到平衡状态,B不正确;C、根据质量守恒定律可知容器中混合气体的质量始终保持不变,不能说明达到平衡状态,C不正确;D、CO2生成速率与CH3OH生成速率相等满足反应速率之比是相应的化学计量数之比,且反应速率是相反的,因此可以说明达到平衡状态,D正确,答案选AD;根据图像可知反应进行到12min时达到平衡状态,此时生成甲醇的浓度是1.5mol/L。所以根据方程式可知消耗氢气的浓度是1.5mol/L×3=4.5mol/L,所以氢气表示的反应速率为4.5mol/L÷12min=0.375 mol/(L·min)。
(4)①升高温度,反应速率增大,反应开始到达平衡状态所需的时间要少,所以反应开始到达平衡状态所需的时间tA 大于tC;
②A点CO的转化率为0.5,则参加反应的CO为10mol×0.5=5mol,则:
CO(g)+2H2(g) CH3OH(g)气体物质的量减少
CH3OH(g)气体物质的量减少
1 2
5mol 10mol
故A点平衡时,混合气体总的物质的量=10mol+20mol-10mol=20mol
B点CO的转化率为0.7,则参加反应的CO为10mol×0.7=7mol,则:
CO(g)+2H2(g) CH3OH(g)气体物质的量减少
CH3OH(g)气体物质的量减少
1 2
7mol 14mol
故B点平衡时,混合气体总的物质的量=10mol+20mol-14mol=16mol
故A、B两点时容器内总气体的物质的量之比n(A):n(B)=20mol:16mol=5:4。
(5)原电池中负极失去电子发生氧化反应,正极得到电子发生还原反应,所以在该原电池中氧气在正极通入,电解质溶液显碱性,则正极电极反应式为O2+2H2O+4e—=4OH—。
考点:考查环境保护、平衡状态判断以及可逆反应的有关计算、电极反应式的书写等


科目:高中化学 来源:2015届江苏省苏州市高三9月学情调研化学试卷(解析版) 题型:选择题
一定温度下,在甲、乙、丙、丁四个恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。下列判断中不正确的是
| 甲 | 乙 | 丙 | 丁 | |
密闭容器体积/L | 2 | 2 | 2 | 2 | |
起始物质的量 | n(SO2)/mol | 0.40 | 0.80 | 0.80 | 0.40 |
n(O2)/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
SO2的平衡转化率% | 80 |
|
|
| |
A.甲中反应的平衡常数小于乙B.该温度下,该反应的平衡常数K为400
C.SO2的平衡转化率: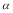 1<
1<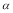 2 =
2 = 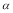 3 D.容器中SO3的物质的量浓度:丙=丁<甲
3 D.容器中SO3的物质的量浓度:丙=丁<甲
查看答案和解析>>
科目:高中化学 来源:2015届江苏省淮安市协作体高二下学期期中考试化学试卷(解析版) 题型:选择题
已知反应2CO(g)=2C(s)+O2(g)的△H为正值,△S为负值。设△H和△S不随温度而变,下列说法正确的是
A、低温下能自发进行
B、高温下能自发进行
C、低温下不能自发进行,高温下能自发进行
D、任何温度下都不能自发进行
查看答案和解析>>
科目:高中化学 来源:2015届江苏省沭阳县高二下学期期中调研测试化学试卷(解析版) 题型:选择题
央视“315特别行动”曝光了河南一些地方“瘦肉精”事件。“瘦肉精”对人体健康会产生危害。已知某种“瘦肉精”含有克伦特罗(Clenbuterol),其结构如下图。下列有关克伦特罗的叙述,正确的是
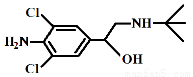
A.该物质的分子式为C12H17ON2Cl
B.该物质不溶于盐酸
C.该物质能与FeCl3溶液发生显色反应
D.该物质分子间都可以形成氢键
查看答案和解析>>
科目:高中化学 来源:2015届江苏省沭阳县高二下学期期中调研测试化学试卷(解析版) 题型:选择题
2007年度诺贝尔化学奖,授予致力于研究合成氨与催化剂表面积大小关系的德国科学家格哈德?埃特尔,表彰他在“固体表面化学过程”研究中作出的贡献。下列说法中正确的是
A.工业生产中,合成氨采用压强越高,温度越低,越有利于提高经济效益。
B.增大催化剂的表面积,能加快合成氨的正反应速率、降低逆反应速率
C.采用催化剂时,反应的活化能降低,使反应易达过渡态,故明显加快
D.增大催化剂的表面积,能增大氨气的产率
查看答案和解析>>
科目:高中化学 来源:2015届江苏省无锡江阴市高二下学期期中考试化学试卷(解析版) 题型:选择题
设NA代表阿伏伽德罗常数的值,则关于反应:C2H2 (g) + 5/2O2(g)=2CO2(g) + H2O(l) △H=-1300 kJ?mol-1的热化学方程式的说法中正确的是
A.有10NA个电子转移时,该反应放出1300kJ的能量
B.有NA个水分子生成且为液体时,吸收1300kJ的能量
C.有2NA个碳氧共用电子对生成时,放出1300kJ的能量
D.有8NA个碳氧共用电子对生成时,放出1300kJ的能量
查看答案和解析>>
科目:高中化学 来源:2015届江苏省无锡江阴市高二下学期期中考试化学试卷(解析版) 题型:选择题
使反应4NH3(g)+3O2(g)=2N2(g)+6H2O(g)在2L的密闭容器中进行,半分钟后N2的物质的量增加了0.6mol。此反应的平均速率v(X)为
A. v(NH3)=0.04mol·L-1·s-1 B. v(O2)=0.015mol·L-1·s-1
C. v(N2)=0.02mol·L-1·s-1 D. v(H2O)=0.02mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高二下学期4月阶段测试化学试卷(解析版) 题型:选择题
一定温度下,在4个容积均为1 L的恒容容器中分别进行反应(各容器中A都足量)A(s)+B(g) C(g)+D(g) ΔH =+100 kJ·mol-1,某时刻测得部分数据如下表:
C(g)+D(g) ΔH =+100 kJ·mol-1,某时刻测得部分数据如下表:
容器编号 | n(B)/mol | n(C)/mol | n(D)/mol | 反应时间/min | 反应速率 |
Ⅰ | 0.06 | 0.60 | 0.10 | t1 | v(正)=v(逆) |
Ⅱ | 0.12 | 1.20 | 0.20 | t2 |
|
Ⅲ | 0.32 | 1.0 | 0 | 0 |
|
Ⅳ | 0.12 | 0.30 |
|
| v(正)=v(逆) |
下列说法正确的是
A.容器Ⅰ中平均反应速率v(B)=0.04/t1 mol·L-1·min-1
B.t2时容器Ⅱ中v(正)>v(逆)
C.容器Ⅲ中反应至平衡时吸热20 kJ
D.容器Ⅳ中c(D)= 0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015届江苏省南京市高三9月学情调研卷化学试卷(解析版) 题型:选择题
下列说法中正确的是()
A.常温下,某难溶物的Ksp为2.5×105
B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈
C.NH3·H2O溶液加水稀释后,溶液中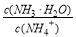 的值增大
的值增大
D.常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com