
| A.NH3经催化氧化生成NO | B.N2和H2在一定条件下合成NH3 |
| C.NO与O2反应生成NO2 | D.由NH3制碳酸氢铵和尿素 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题

| A.高聚氮与氮气互为同位素 |
| B.14g高聚氮含3.01×1023个氮原子 |
| C.高聚氮中氮原子间的化学键为非极性键 |
| D.高聚氮转变成氮气是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
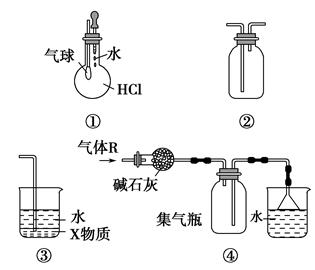
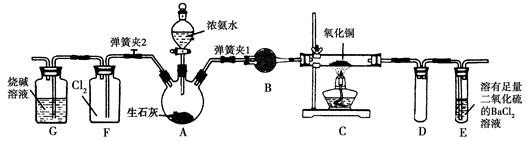
| A.装置①可验证HCl气体在水中的溶解性 |
| B.装置②可用于收集H2、NH3、Cl2、HCl、NO2、NO等 |
| C.装置③中X为四氯化碳,可用于吸收氨气或氯化氢 |
| D.装置④可用于干燥、收集氨气,并吸收多余的氨气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
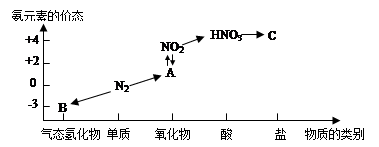
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
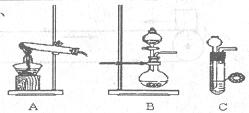
| | 实验装置 | 实验药品 | 制备原理 |
| 甲小组 | A | 氢氧化钙、氯化铵 | 反应的化学方程式为 ① |
| 乙小组 | ② | 浓氨水、氢氧化钠 | 用化学平衡原理分析氢氧化钠的作用: ③ |
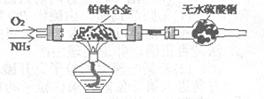
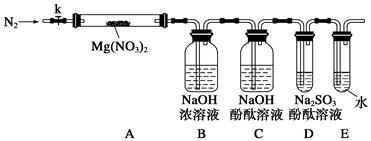
 3Cu+N2+3H2O),而氮气跟镁在高温下反应可得到氮化镁,但氮化镁遇水立即反应生成Mg(OH)2和NH3。乙组提出了如下制备氮化镁的实验方案示意框图(实验前系统内空气已排除;图中箭头表示气体的流向)。你认为此方案是否正确,并说明理由 。
3Cu+N2+3H2O),而氮气跟镁在高温下反应可得到氮化镁,但氮化镁遇水立即反应生成Mg(OH)2和NH3。乙组提出了如下制备氮化镁的实验方案示意框图(实验前系统内空气已排除;图中箭头表示气体的流向)。你认为此方案是否正确,并说明理由 。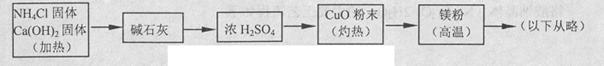
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com