
| A.某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸盐 |
| B.某溶液中滴加BaCl2溶液,生成不溶于稀HNO3的白色沉淀,证明一定含有SO42- |
| C.某无色溶液滴入酚酞试液显红色,该溶液一定是含有大量的H+ |
| D.验证某不纯的烧碱溶液中是否含Cl-,先加过量的稀硝酸除去OH-,再加入AgNO3溶液,有白色沉淀,证明含Cl- |
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源:不详 题型:单选题
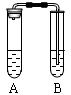
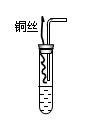
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
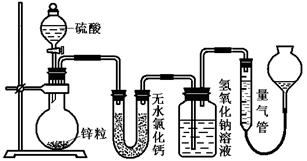
 应后锌有剩余,测得氢氧化钠洗气瓶增重mg,则整个实验过程产生的气体中,n(H2)/n(SO2)=_______________(用含字母的代数式表示)。若撤走盛有无水氯化钙的U型管,n(H2)/n(SO2)的数值将
应后锌有剩余,测得氢氧化钠洗气瓶增重mg,则整个实验过程产生的气体中,n(H2)/n(SO2)=_______________(用含字母的代数式表示)。若撤走盛有无水氯化钙的U型管,n(H2)/n(SO2)的数值将查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B.蒸馏时,温度计水银球应浸没在液体中 |
| C.蒸馏中,冷却水应从冷凝管的下口通入,上口流出。 |
| D.用湿润的红色石蕊试纸检验氨气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用加热的方法分离氯化钠和氯化铵的固体混和物 |
| B.用水鉴别乙醛、苯、硝基苯 |
| C.用核磁共振氢谱鉴定未知物C2H6O的分子结构 |
| D.用10mL量筒量取5.00mL1.00 mol·L-1盐酸配制0.100mol·L-1盐酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
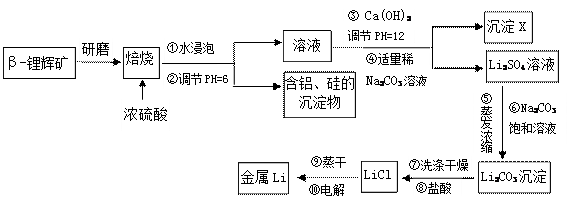
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.稀释浓硫酸时,将蒸馏水沿玻璃棒缓慢注入浓硫酸中 |
| B.用稀硫酸和锌粒反应制氢气时加入少许硫酸铜以加快反应速率 |
| C.用玻璃棒搅拌漏斗中的液体以加快过滤的速度 |
| D.加入盐酸以除去硫酸钠中的少量碳酸钠杂质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 依次通过浓硫酸和浓氢氧
依次通过浓硫酸和浓氢氧 化钠溶液,实验结束后,称得浓硫酸增重10.8g,浓氢氧化钠溶液增重22g。
化钠溶液,实验结束后,称得浓硫酸增重10.8g,浓氢氧化钠溶液增重22g。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com