
| A. | 原子总数 | B. | 摩尔质量 | C. | 分子总数 | D. | 质量 |
分析 同温同压下,气体摩尔体积相等,因为两容器气体体积相同,所以两容器内气体物质的量相同,根据N=nNA、m=nM结合分子构成进行计算.
解答 解:同温同压下,气体摩尔体积相等,因为两容器气体体积相同,所以两容器内气体物质的量相同,
A.根据N=nNA知,气体分子数N与其n成正比,n相等,所以分子数N相等,每个CO2中含有3个原子、每个N2或O2中含有两个原子,所以原子总数不等,故A错误;
B.二氧化碳摩尔质量、氮气和氧气混合气体平均摩尔质量可能相等也可能不等,故B错误;
C.根据A知,其分子总数相等,故C正确;
D.二氧化碳摩尔质量、氮气和氧气混合气体平均摩尔质量不等,根据m=nM知,物质的量相等时其质量不等,故D错误;
故选C.
点评 本题考查阿伏伽德罗定律及其推论,侧重考查物质的量公式的灵活运用,明确各个物理量之间的关系式即可解答,注意气体摩尔体积的适用范围及适用条件,为易错点.


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:实验题
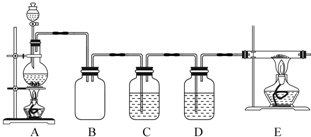
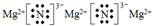 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,下列叙述中正确的是( )
,下列叙述中正确的是( )| A. | 1mol胡椒酚最多可与5molH2发生反应 | |
| B. | 1mol胡椒酚最多可与4mol溴发生反应 | |
| C. | 胡椒酚中所有原子可以共平面 | |
| D. | 胡椒酚在水中的溶解度小于苯酚在水中的溶解度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 试剂A可以是稀硫酸或盐酸 | |
| B. | 加入试剂B除去Mg2+、Fe3+ | |
| C. | 滤渣1的主要成分是SiO2 | |
| D. | 电解氧化铝时在阴极上定期补充炭块 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①不正确 | B. | ②⑤不正确 | C. | 只有③④正确 | D. | 全部正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 不纯物 | 除杂试剂 | 分离方法 |
| A | CH4 (C2H4) | 酸性KMnO4溶液 | 洗气 |
| B | NH4Cl溶液 (FeCl3) | NaOH溶液 | 过滤 |
| C | 乙酸乙酯 (乙酸) | 饱和Na2CO3溶液 | 蒸馏 |
| D | C2H5OH (H2O) | 新制生石灰 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com