

��������������и��⣺
��1����Ӧ�ﵽƽ��ʱ��ƽ�ⳣ������ʽK�� �������¶ȣ�Kֵ �����������С�����䡱����
��2����500�棬�ӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v(H2)��
��3���������������������£��Դ���E�����ϵ���ѹ����ԭ����1/2�������йظ���ϵ��˵����ȷ����
a ������Ũ�ȼ��� b ����Ӧ���ʼӿ죬�淴Ӧ����Ҳ�ӿ�
c �״������ʵ������� d ����ƽ��ʱn(H2)/n(CH3OH)����
��4�����о�����Ӧ������������õ�ΪCu2O����Ӧ��ϵ�к�����CO2������ά�ִ���Cu2O�������䣬ԭ���ǣ� ���û�ѧ����ʽ��ʾ����
��1��K��c(CH3OH)/c(CO)��c2(H2) ��С
��2��2nB/3tB mol��(L��min)��1
��3��b c
��4��Cu2O+CO![]() 2Cu+CO2
2Cu+CO2
���������⿼�黯ѧ��Ӧ�����뻯ѧƽ��֪ʶCO(g)+2H2(g)![]() CH3OH(g)����ͼ���֪�ﵽƽ��������¶ȣ��״������ʵ�����С��ƽ�������ƶ�������ӦΪ���ȷ�Ӧ����Ϊ�����¶�ƽ�������ȷ����ƶ���
CH3OH(g)����ͼ���֪�ﵽƽ��������¶ȣ��״������ʵ�����С��ƽ�������ƶ�������ӦΪ���ȷ�Ӧ����Ϊ�����¶�ƽ�������ȷ����ƶ���
K=![]() �������¶�ƽ�����ƣ�K��С����Ӧ�����õ�λʱ����Ũ�ȵı仯����ʾ������֮�ȵ��ڻ�ѧ������֮�ȡ�V(H2)=
�������¶�ƽ�����ƣ�K��С����Ӧ�����õ�λʱ����Ũ�ȵı仯����ʾ������֮�ȵ��ڻ�ѧ������֮�ȡ�V(H2)=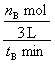 ��2=
��2=![]() mol��(L��min)��1��
mol��(L��min)��1��
����CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
����ѹǿ��ѹ������������淴Ӧ���ʶ�����ƽ�������ƶ����״������ʵ����������������ʵ�����С�����������С��������Ũ������b��c��ȷ��Cu2O+CO![]() 2Cu+CO2����ΪCO��ԭCu2O��ʹCu2O���٣�Ϊ��ά��Cu2O�������䣬��������CO2����Cu2O��CO�ķ�Ӧ��
2Cu+CO2����ΪCO��ԭCu2O��ʹCu2O���٣�Ϊ��ά��Cu2O�������䣬��������CO2����Cu2O��CO�ķ�Ӧ��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 һ�������£������Ϊ3L���ܱ������У�һ����̼��������Ӧ���ɼ״�������ΪCu2O/ZnO����CO��g��+2H2��g��CH3OH��g����������������и��⣺
һ�������£������Ϊ3L���ܱ������У�һ����̼��������Ӧ���ɼ״�������ΪCu2O/ZnO����CO��g��+2H2��g��CH3OH��g����������������и��⣺| 2n(B) |
| 3t(B) |
| 2n(B) |
| 3t(B) |
| 1 |
| 2 |
| n(H2) |
| n(CH3OH) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 һ�������£������Ϊ3L���ܱ������У�һ����̼��������Ӧ���ɼ״�������ΪCu2O/ZnO����CO��g��+2H2��g��?CH3OH��g���������й�˵����ȷ���ǣ�������
һ�������£������Ϊ3L���ܱ������У�һ����̼��������Ӧ���ɼ״�������ΪCu2O/ZnO����CO��g��+2H2��g��?CH3OH��g���������й�˵����ȷ���ǣ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
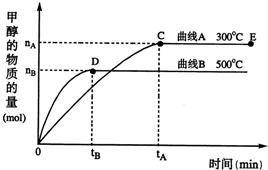 �������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӣ�Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���һ�������£������Ϊ3L���ܱ������У�һ����̼��������Ӧ���ɼ״�������ΪCu2O/ZnO����
�������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӣ�Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���һ�������£������Ϊ3L���ܱ������У�һ����̼��������Ӧ���ɼ״�������ΪCu2O/ZnO����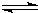 CH3OH��g��
CH3OH��g��| c(CH3OH) |
| c(CO)?c2(H2) |
| c(CH3OH) |
| c(CO)?c2(H2) |
| 2nB |
| 3tB |
| 2nB |
| 3tB |
| 1 |
| 2 |
| n(H2) |
| n(CH3OH) |
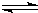 2Cu+CO2
2Cu+CO2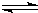 2Cu+CO2
2Cu+CO2| ��ȼ |
| ��ȼ |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 һ�������£������Ϊ3L���ܱ������У�һ����̼��������Ӧ���ɼ״�������ΪCu2O/ZnO������������������и��⣺
һ�������£������Ϊ3L���ܱ������У�һ����̼��������Ӧ���ɼ״�������ΪCu2O/ZnO������������������и��⣺| c(CH3OH) |
| c(CO)c2(H2) |
| c(CH3OH) |
| c(CO)c2(H2) |
| 2nB |
| 3tB |
| 2nB |
| 3tB |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com