
【题目】图表示的是往某Na2CO3溶液中滴入稀盐酸产生CO2气体的过程。
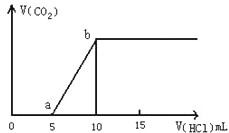
(1)写出a点以前发生反应的离子方程式: 。
(2)写出a点到b点发生反应的离子方程式: 。
(3)若某Na2CO3溶液中含m mol Na2CO3,向其中滴入一定量的稀盐酸,恰好使溶液中Cl-和HCO3-的物质的量之比为2:1,则滴入稀盐酸的物质的量等于 mol(用m表示)。
【答案】(1)CO32-+H+=HCO3-;(2)HCO3-+H+=H2O+CO2↑;(3)![]()
【解析】
试题分析:(1)碳酸钠和少量的盐酸之间反应生成的是碳酸氢钠和氯化钠,即Na2CO3+HCl=NaCl+NaHCO3,离子方程式为CO32-+H+=HCO3-,故答案为:CO32-+H+=HCO3-;
(2)碳酸氢钠和盐酸反应生成的是氯化钠、水以及二氧化碳,实质是:HCO3-+H+=H2O+CO2↑,故答案为:HCO3-+H+=H2O+CO2↑;
(3)设和碳酸氢钠反应的盐酸的物质的量是x,
Na2CO3+HCl=NaCl+NaHCO3
1 1 1 1
m m m m
NaHCO3+HCl=NaCl+H2O+CO2↑
1 1 1
x x x
则Cl-的物质的量为:m+x,HCO3-的物质的量为:m-x,使Cl-和HCO3-的物质的量比是2:1,即![]() =
=![]() ,解得x=
,解得x=![]() mol,加入盐酸的物质的量=
mol,加入盐酸的物质的量=![]() mol+mmol=
mol+mmol=![]() mol,故答案为:
mol,故答案为:![]() mol。
mol。


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】某废催化剂含58.2%的SiO2、21.0%的ZnO、4.50%的ZnS和12.8%的CuS及少量的Fe3O4。某同学用15.0 g该废催化剂为原料,回收锌和铜。采用的实验方案如下:
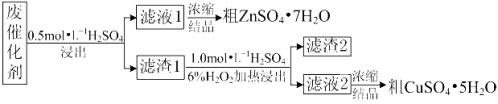
已知:① ZnS与稀硫酸反应时,化合价不变;
② CuS既不溶解于稀硫酸,也不与稀硫酸反应。
回答下列问题:
(1)在下列装置中,第一次浸出必须用________________,第二次浸出应选用______________。(填标号)。第二次浸出时,加热温度不宜过高的原因是 。

(2)滤液1中含有Fe2+,请根据提供的试剂进行检验,则检验方法为: 。
(提供的试剂:稀盐酸、KSCN溶液、KMnO4溶液、NaOH溶液、碘水)
(3)将滤液1、滤液2蒸发浓缩至 时,停止加热,然后冷却结晶得到相应的粗产品。
(4)若滤渣2中含有淡黄色固体,写出第二次浸出的化学反应方程式: 。
(5)某同学在实验完成之后,得到1.50 g CuSO4·5H2O,则铜的回收率为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 热化学方程式中,如果没有注明温度和压强,则表示的反应热是在标准状况下测得的
B. 升高温度或加入催化剂,可以改变化学反应的反应热
C. 据能量守恒定律,反应物的总能量一定等于生成物的总能量
D. 若生成与断裂1 mol H—O键对应放出和吸收的能量分别为a kJ、b kJ,则a=b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一固定容积的密闭容器中进行如下反应N2+3H2![]() 2NH3,下列情况一定能说明反应已达到平衡的是
2NH3,下列情况一定能说明反应已达到平衡的是
①容器内压强不随时间而变化
②单位时间内,有3molH2反应,同时有2molNH3生成
③气体的密度不随时间而变化
④单位时间内,有1molN2生成,同时有2molNH3生成
⑤用N2、H2、NH3表示的该反应的化学反应速率之比为1∶3∶2
⑥气体的平均摩尔质量不随时间而变化
A.①④⑥ B.①②③ C. ②③⑤ D.①②⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液只含下表离子中的几种,且各离子的物质的量浓度相等(不考虑水的电离与离子水解)。
阳离子 | K+、NH4+、Fe2+、Mg2+、Cu2+ |
阴离子 | OH-、Cl-、CO32-、SO42- |
某同学进行了如下实验(必要时可加热):

下列说法正确的是
A. 由沉淀A推断原溶液中一定含有SO42-
B. 原溶液中只含有NH4+、Fe2+、Cl-、SO42-
C. 滤液A中可能含有K+
D. 沉淀B中一定含有Mg(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两个体积相同的容器,一个盛有NO,另一个盛有N2和O2,在同温同压下两容器内的气体一定具有相同的
①原子总数 ②质子总数 ③分子总数 ④质量
A. ①② B. ②③ C. ①③ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.1 mol羟基与1 mol氢氧根离子所含的质子数和电子数均为9NA
B.1 L 0.1 mol·L-1的NaHCO3溶液中![]() 、
、![]() 的离子数之和为0.1NA
的离子数之和为0.1NA
C.0.1 mol·L-1的CuCl2溶液中含有Cl-的数目为0.2 NA
D.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸铵[(NH4)2Cr2O7]受热发生氧化还原反应,下列有关重铬酸铵受热分解的判断符合实际的是( )
A. 分解产物为CrO3+NH3+H2O
B. 分解产物为Cr2O3+N2+H2O
C. 反应中-3价N元素被氧化,+7价Cr元素被还原
D. 反应中-3价N元素被还原,+6价Cr元素被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com